Как создавалась таблица Менделеева, и какие уроки творческого процесса можно извлечь из этой истории?

Любой, кто ходил в школу, помнит, что одним из обязательных для изучения предметов была химия. Она могла нравиться, а могла и не нравиться – это не важно. И вполне вероятно, что многие знания по этой дисциплине уже забыты и в жизни не применяются. Однако таблицу химических элементов Д. И. Менделеева наверняка помнит каждый. Для многих она так и осталась разноцветной таблицей, где в каждый квадратик вписаны определённые буквы, обозначающие названия химических элементов. Но здесь мы не будем говорить о химии как таковой, и описывать сотни химических реакций и процессов, а расскажем о том, как вообще появилась таблица Менделеева – эта история будет интересна любому творчески мыслящему человеку, да и вообще всем тем, кто охоч до интересной и полезной информации.
Небольшая предыстория
В далёком 1668 году выдающимся ирландским химиком, физиком и богословом Робертом Бойлем была опубликована книга, в которой было развенчано немало мифов об алхимии, и в которой он рассуждал о необходимости поиска неразложимых химических элементов. Учёный также привёл их список, состоящий всего из 15 элементов, но допускал мысль о том, что могут быть ещё элементы. Это стало отправной точкой не только в поиске новых элементов, но и в их систематизации.
Сто лет спустя французским химиком Антуаном Лавуазье был составлен новый перечень, в который входили уже 35 элементов. 23 из них позже были признаны неразложимыми. Но поиск новых элементов продолжался учёными по всему миру. И главную роль в этом процессе сыграл знаменитый русский химик Дмитрий Иванович Менделеев – он впервые выдвинул гипотезу о том, что между атомной массой элементов и их расположением в системе может быть взаимосвязь.
Благодаря кропотливому труду и сопоставлению химических элементов Менделеев смог обнаружить связь между элементами, в которой они могут быть одним целым, а их свойства являются не чем-то само собой разумеющимся, а представляют собой периодически повторяющееся явление. В итоге, в феврале 1869 года Менделеев сформулировал первый периодический закон, а уже в марте его доклад «Соотношение свойств с атомным весом элементов» был представлен на рассмотрение Русского химического общества историком химии Н. А. Меншуткиным. Затем в том же году публикация Менделеева была напечатана в журнале «Zeitschrift fur Chemie» в Германии, а в 1871 году новую обширную публикацию учёного, посвящённую его открытию, опубликовал другой немецкий журнал «Annalen der Chemie».
Создание периодической таблицы
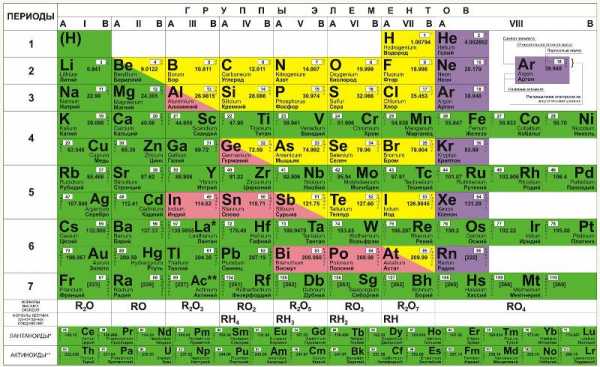
Основная идея к 1869 году уже была сформирована Менделеевым, причём за довольно короткое время, но оформить её в какую-либо упорядоченную систему, наглядно отображающую, что к чему, он долго не мог. В одном из разговоров со своим соратником А. А. Иностранцевым он даже сказал, что в голове у него уже всё сложилось, но вот привести всё к таблице он не может. После этого, согласно данным биографов Менделеева, он приступил к кропотливой работе над своей таблицей, которая продолжалась трое суток без перерывов на сон. Перебирались всевозможные способы организации элементов в таблицу, а работа была осложнена ещё и тем, что в тот период наука знала ещё не обо всех химических элементах. Но, несмотря на это, таблица всё же была создана, а элементы систематизированы.
Легенда о сне Менделеева
Многие слышали историю, что Д. И. Менделееву его таблица приснилась. Эта версия активно распространялась вышеупомянутым соратником Менделеева А. А. Иностранцевым в качестве забавной истории, которой он развлекал своих студентов. Он говорил, что Дмитрий Иванович лёг спать и во сне отчётливо увидел свою таблицу, в которой все химические элементы были расставлены в нужном порядке. После этого студенты даже шутили, что таким же способом была открыта 40° водка. Но реальные предпосылки для истории со сном всё же были: как уже упоминалось, Менделеев работал над таблицей без сна и отдыха, и Иностранцев однажды застал его уставшим и вымотанным. Днём Менделеев решил немного передохнуть, а некоторое время спустя, резко проснулся, сразу же взял листок бумаги и изобразил на нём уже готовую таблицу. Но сам учёный опровергал всю эту историю со сном, говоря: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово». Так что легенда о сне может быть и очень привлекательна, но создание таблицы стало возможным только благодаря упорному труду.
Дальнейшая работа
В период с 1869 по 1871 годы Менделеев развивал идеи периодичности, к которым склонялось научное сообщество. И одним из важных этапов данного процесса стало понимание того, что любой элемент в системе должно располагать, исходя из совокупности его свойств в сравнении со свойствами остальных элементов. Основываясь на этом, а также опираясь на результаты исследований в изменении стеклообразующих оксидов, химику удалось внести поправки в значения атомных масс некоторых элементов, среди которых были уран, индий, бериллий и другие.
Пустые клетки, остававшиеся в таблице, Менделеев, конечно же, хотел скорее заполнить, и в 1870 году предсказал, что в скором времени будут открыты неизвестные науке химические элементы, атомные массы и свойства которых он сумел вычислить. Первыми из них стали галлий (открыт в 1875 году), скандий (открыт в 1879 году) и германий (открыт в 1885 году). Затем прогнозы продолжили реализовываться, и были открыты ещё восемь новых элементов, среди которых: полоний (1898 год), рений (1925 год), технеций (1937 год), франций (1939 год) и астат (1942-1943 годы). Кстати, в 1900 году Д. И. Менделеев и шотландский химик Уильям Рамзай пришли к мнению, что в таблицу должны быть включены и элементы нулевой группы – до 1962 года они назывались инертными, а после – благородными газами.
Организация периодической системы
Химические элементы в таблице Д. И. Менделеева расположены по рядам, в соответствии с возрастанием их массы, а длина рядов подобрана так, чтобы находящиеся в них элементы имели схожие свойства. Например, благородные газы, такие как радон, ксенон, криптон, аргон, неон и гелий с трудом вступают в реакции с другими элементами, а также имеют низкую химическую активность, из-за чего расположены в крайнем правом столбце. А элементы левого столбца (калий, натрий, литий и т.д.) отлично реагируют с прочими элементами, а сами реакции носят взрывной характер. Говоря проще, внутри каждого столбца элементы имеют подобные свойства, варьирующиеся при переходе от одного столбца к другому. Все элементы, вплоть до №92 встречаются в природе, а с №93 начинаются искусственные элементы, которые могут быть созданы лишь в лабораторных условиях.
В своём первоначальном варианте периодическая система понималась только как отражение существующего в природе порядка, и никаких объяснений, почему всё должно обстоять именно так, не было. И лишь когда появилась квантовая механика, истинный смысл порядка элементов в таблице стал понятен.
Уроки творческого процесса
Говоря о том, какие уроки творческого процесса можно извлечь из всей истории создания периодической таблицы Д. И. Менделеева, можно привести в пример идеи английского исследователя в области творческого мышления Грэма Уоллеса и французского учёного Анри Пуанкаре. Приведём их вкратце.
Согласно исследованиям Пуанкаре (1908 год) и Грэма Уоллеса (1926 год), существует четыре основных стадии творческого мышления:
- Подготовка – этап формулирования основной задачи и первые попытки её решения;
- Инкубация – этап, во время которого происходит временное отвлечение от процесса, но работа над поиском решения задачи ведётся на подсознательном уровне;
- Озарение – этап, на котором находится интуитивное решение. Причём, найтись это решение может в абсолютно не имеющей к задаче ситуации;
- Проверка – этап испытаний и реализации решения, на котором происходит проверка этого решения и его возможное дальнейшее развитие.
Как мы видим, в процессе создания своей таблицы Менделеев интуитивно следовал именно этим четырём этапам. Насколько это эффективно, можно судить по результатам, т.е. по тому, что таблица была создана. А учитывая, что её создание стало огромным шагом вперёд не только для химической науки, но и для всего человечества, приведённые выше четыре этапа могут быть применимы как к реализации небольших проектов, так и к осуществлению глобальных замыслов. Главное помнить, что ни одно открытие, ни одно решение задачи не могут быть найдены сами по себе, как бы ни хотели мы увидеть их во сне и сколько бы ни спали. Чтобы что-то получилось, не важно, создание это таблицы химических элементов или разработка нового маркетинг-плана, нужно обладать определёнными знаниями и навыками, а также умело использовать свои потенциал и упорно работать.
Мы желаем вам успехов в ваших начинаниях и успешной реализации задуманного!
4brain.ru
Дмитрий Менделеев – биография, фото, личная жизнь, интересные факты
Дмитрий Менделеев: биография
Менделеев Дмитрий Иванович – русский ученый, гениальный химик, физик, исследователь в области метрологии, гидродинамики, геологии, глубокий знаток промышленности, приборостроитель, экономист, воздухоплаватель, педагог, общественный деятель и оригинальный мыслитель.
Детство и юность
Великий ученый родился в 1834 году, 8 февраля, в Тобольске. Отец Иван Павлович был директором окружных училищ и Тобольской гимназии, происходил из рода священника Павла Максимовича Соколова, русского по национальности.
 Дмитрий Менделеев в детстве и молодости
Дмитрий Менделеев в детстве и молодостиФамилию Иван поменял в детстве, будучи учащимся Тверской семинарии. Предположительно, это было сделано в честь его крестного отца, помещика Менделеева. Позднее неоднократно затрагивался вопрос о национальной принадлежности фамилии ученого. По одним сведениям, она свидетельствовала о еврейских корнях, по другим – о немецких. Сам Дмитрий Менделеев рассказывал о том, что фамилию присвоил Ивану его педагог из семинарии. Юноша произвел удачный обмен и тем прославился среди однокашников. По двум словам – «мену делать» – Иван Павлович был вписан в учебную ведомость.
 Родители Дмитрия Менделеева
Родители Дмитрия МенделееваМать Мария Дмитриевна (в девичестве Корнильева) занималась воспитанием детей и домашним хозяйством, имела репутацию интеллигентной и умной женщины. Дмитрий был в семье самым младшим, последним из четырнадцати детей (по другой информации – последним из семнадцати детей). В 10-летнем возрасте мальчик лишился отца, который ослеп и вскоре умер.
Во время учебы в гимназии способностей Дмитрий не проявил, сложнее всего ему давалась латынь. Любовь к науке прививала мать, она же участвовала в формировании его характера. Мария Дмитриевна увезла сына учиться в Петербург.
 Дмитрий Менделеев в молодости
Дмитрий Менделеев в молодостиВ 1850 году в Петербурге юноша поступает в Главный пединститут на отделение естественных наук физмата. Его преподавателями были профессора Э. Х. Ленц, А. А. Воскресенский и Н. В. Остроградский.
Во время учебы в институте (1850-1855 годы) Менделеев демонстрирует незаурядные способности. Будучи студентом, он публикует статью «Об изоморфизме» и ряд химических анализов.
Наука
В 1855-м Дмитрий получает диплом с золотой медалью и направление в Симферополь. Здесь он работает старшим учителем гимназии. С началом Крымской войны Менделеев перебирается в Одессу и получает должность преподавателя в лицее.
 Ученый Дмитрий Менделеев
Ученый Дмитрий МенделеевВ 1856-м он снова в Петербурге. Учится в университете, защищает диссертацию, преподает химию. Осенью защищает еще одну диссертацию и назначается приват-доцентом университета.
В 1859-м Менделеева отправляют в командировку в Германию. Работает в университете Гейдельберга, обустраивает лабораторию, исследует капиллярные жидкости. Здесь им были написаны статьи «О температуре абсолютного кипения» и «О расширении жидкостей», открыто явление «критическая температура».
 Дмитрий Менделеев
Дмитрий МенделеевВ 1861-м ученый возвращается в Петербург. Создает учебник «Органическая химия», за что удостаивается Демидовской премии. В 1864-м он уже профессор, а спустя два года возглавляет кафедру, преподает и работает над «Основами химии».
В 1869-м представляет периодическую систему элементов, совершенствованию которой посвятил всю жизнь. В таблице Менделеев представил атомную массу девяти элементов, позднее добавил в свод группу благородных газов и оставил место для элементов, которые еще предстояло открыть. В 90-е годы Дмитрий Менделеев внес свой вклад в открытие явления радиоактивности. Периодический закон включал в себя доказательства связи свойств элементов и их атомного объема. Теперь рядом с каждой таблицей химических элементов находится фото первооткрывателя.
 Химик Дмитрий Менделеев в лаборатории
Химик Дмитрий Менделеев в лабораторииВ 1865–1887 годах разрабатывает гидратную теорию растворов. В 1872-м начинает изучать упругость газов, спустя два года выводит уравнение идеального газа. Среди достижений Менделеева этого периода – создание схемы дробной перегонки нефтепродуктов, применение цистерн и трубопровода. При содействии Дмитрия Ивановича сжигание черного золота в топках полностью прекратилось. Фраза ученого «Сжигать нефть — все равно, что топить печку ассигнациями» стала афоризмом.
 Портрет Д.И. Менделеева в мантии доктора права Эдинбургского университета. Илья Репин
Портрет Д.И. Менделеева в мантии доктора права Эдинбургского университета. Илья РепинЕще одной сферой деятельности ученого стали географические исследования. В 1875 году Дмитрий Иванович побывал на Парижском международном географическом конгрессе, где представил на суд свое изобретение – дифференциальный барометр-высотомер. В 1887 году ученый участвовал в путешествии на аэростате в верхние слои атмосферы для наблюдения полного солнечного затмения.
В 1890-м ссора с высокопоставленным чиновником стала причиной ухода Менделеева из университета. В 1892-м химик изобретает методику получения бездымного пороха. Одновременно с этим его назначают хранителем Депо образцовых мер и весов. Здесь он возобновляет прототипы фунта и аршина, занимается вычислениями по сравнению русских и английских эталонов мер.
 Прототипы фунта и аршина
Прототипы фунта и аршинаПо инициативе Менделеева в 1899 году факультативно вводится метрическая система мер. В 1905, 1906 и 1907 годах ученого выдвигают кандидатом на Нобелевскую премию. В 1906-м году Нобелевским комитетом премия присуждается Менделееву, но Королевская академия наук Швеции это решение не подтвердила.
Менделеев, являющийся автором более чем полутора тысяч трудов, имел огромный научный авторитет в мире. За свои заслуги ученый был удостоен многочисленных научных званий, российских и зарубежных наград, был почетным членом ряда научных обществ на родине и за границей.
Личная жизнь
В юности с Дмитрием случился неприятный случай. Ухаживания за девушкой Соней, с которой тот был знаком с детства, закончились помолвкой. Но изнеженная красавица к венцу так и не пошла. Накануне свадьбы, когда подготовка уже шла полным ходом, выходить замуж Сонечка отказалась. Девушка посчитала, что нет смысла что-то менять, если жизнь и так хороша.
 Дмитрий Менделеев
Дмитрий МенделеевДмитрий болезненно переживал разрыв с невестой, но жизнь шла своим чередом. От тяжких дум его отвлекла поездка за границу, чтение лекций и верные друзья. Возобновив отношения с Феозвой Никитичной Лещевой, с которой был знаком ранее, стал с ней встречаться. Девушка была старше Дмитрия на 6 лет, но выглядела молодо, поэтому разница в возрасте была незаметной.
 Дмитрий Менделеев с первой женой Феозвой
Дмитрий Менделеев с первой женой ФеозвойВ 1862-м они стали мужем и женой. Первая дочь Маша родилась в 1863 году, но прожила только несколько месяцев. В 1865-м родился сын Володя, спустя три года – дочь Оля. К детям Дмитрий Иванович был привязан, но времени им уделял мало, так как жизнь была посвящена научной деятельности. В браке, заключенном по принципу «стерпится-слюбится», он не был счастлив.
 Вторая жена Дмитрия Менделеева Анна Попова
Вторая жена Дмитрия Менделеева Анна ПоповаВ 1877-м Дмитрий знакомится с Анной Ивановной Поповой, которая стала для него человеком, способным в трудную минуту поддержать умным словом. Девушка оказалась творчески одаренным человеком: училась в консерватории игре на фортепиано, позже в Академии художеств.
Дмитрий Иванович устраивал у себя молодежные «пятницы», где и познакомился с Анной. «Пятницы» трансформировались в литературно-художественные «среды», завсегдатаями которых были талантливые художники и профессора. Среди них были Илья Репин, Иван Крамской, Архип Куинджи, Иван Шишкин, Николай Вагнер, Николай Бекетов и другие.
 Дочь ученого — Любовь Менделеева
Дочь ученого — Любовь МенделееваЖенитьба Дмитрия и Анны состоялась в 1881 году. Вскоре у них родилась дочь Люба, сын Иван появился в 1883-м, близнецы Василий и Мария – в 1886-м. Во втором браке личная жизнь ученого сложилась счастливо. Позднее зятем Дмитрия Ивановича стал поэт Александр Блок, женившись на дочери ученого Любови.
Смерть
В начале 1907 года в Палате мер и весов проходила встреча Дмитрия Менделеева и нового министра промышленности Дмитрия Философова. После обхода палаты ученый заболел простудой, которая вызвала воспаление легких. Но даже будучи сильно больным, Дмитрий продолжал работу над рукописью «К познанию России», последними написанными им словами в которой стала фраза:
«В заключение считаю необходимым, хоть в самых общих чертах, высказать…».
 Могила Дмитрия Менделеева
Могила Дмитрия МенделееваСмерть наступила в пять часов утра 2 февраля по причине паралича сердца. Могила Дмитрия Менделеева находится на Волковом кладбище Санкт-Петербурга.
Память Дмитрия Менделеева увековечена рядом монументов, документальных фильмов, книгой «Дмитрий Менделеев. Автор великого закона».
Интересные факты
- С именем Дмитрия Менделеева связано множество интересных фактов биографии. Помимо деятельности ученого, Дмитрий Иванович занимался промышленной разведкой. В 70-е годы в США начался расцвет нефтяной промышленности, появились технологии, которые удешевили производство нефтепродуктов. Российские производители стали терпеть убытки на международном рынке из-за неспособности конкурировать по цене.
- В 1876 году по ходатайству министерства финансов России и «Русского технического общества», сотрудничавшего с военным ведомством, Менделеев отправился за океан на выставку технических новинок. На месте химик изучил новаторские принципы изготовления керосина и других нефтепродуктов. А по заказанным отчетам железнодорожных служб Европы Дмитрий Иванович попытался расшифровать метод изготовления бездымного пороха, что ему и удалось.
 Ученый Дмитрий Иванович Менделеев
Ученый Дмитрий Иванович Менделеев- У Менделеева было хобби – изготавливать чемоданы. Ученый шил себе одежду.
- Ученому приписывают изобретение водки и самогонного аппарата. Но на самом деле Дмитрий Иванович в теме докторской диссертации «Рассуждение о соединении спирта с водою» изучил вопрос уменьшения объема смешиваемых жидкостей. В работе ученого не было и слова о водке. А стандарт в 40° был установлен в царской России еще в 1843 году.
- Придумал герметические отсеки для пассажиров и пилотов.
- Существует легенда, что открытие периодической системы Менделеева произошло во сне, но это миф, созданный самим ученым.
- Сам скручивал папиросы, используя дорогой табак. Говорил, что никогда не бросит курить.
Открытия
- Создал управляемый аэростат, который стал неоценимым вкладом в воздухоплавание.
- Разработал периодическую таблицу химических элементов, ставшую графическим выражением закона, установленного Менделеевым в ходе работы над «Основами химии».
- Создал пикнометр – прибор, способный определять плотность жидкости.
- Открыл критическую температуру кипения жидкостей.
- Создал уравнение состояния идеального газа, устанавливающее зависимость между абсолютной температурой идеального газа, давлением и молярным объемом.
- Открыл Главную палату мер и весов – центральное учреждение Министерства финансов, заведовавшее поверочной частью Российской империи, подчинявшееся отделу торговли.
Фото
24smi.org
Менделеев Дмитрий Иванович краткая биография и его открытия
В XIX веке как никогда много было сделано научных открытий и создано технических изобретений. Казалось, что нет ничего необъяснимого или неподвластного науке. Одним из ярчайших представителей того времени стал ученый и изобретатель Менделеев Дмитрий Иванович. Краткая биография и его открытия описаны в данной статье.

Как провел детство Менделеев Д.И.
Будущий ученый родился последним, семнадцатым в семье ребенком 27 января по юлианскому календарю 1834 года в Тобольске.
Мать Дмитрия, Мария Дмитриевна Корнильева, владела мелкой стекольной фабрикой.
А отцом его был директор училищ Тобольского округа Иван Менделеев.
Дмитрий Иванович детство провел в окружении русской интеллигенции.
Его семья часто гостила у брата Марии Дмитриевны, который был управляющим у князей Трубецких.
Нередко у него в гостях бывали литераторы, художники, ученые.
Немало первых жизненных впечатлений будущим химиком было получено также на заводе матери.

Менделеев Дмитрий Иванович краткая биография
В 1850 в возрасте 16 лет Дмитрий начал учебу в Главном Педагогическом институте в Санкт-Петербурге. Через полтора месяца умерла его мать, и юноша остался без родственников и друзей, а также без имущества. Учился он с огромным интересом. Химия и минералогия были его любимыми предметами. Особенно увлекало Дмитрия огромное разнообразие химических превращений и соединений, в основе которых лежат лишь несколько десятков элементов. На последнем курсе, за выпускную диссертацию «Изоморфизм» о химических процессах, сопровождающих образование кристаллов, наградили золотой медалью Менделеева Дмитрия Ивановича. Фото представлено ниже:

Осенью 1856 будущий открыватель Периодического закона стал профессором технологического института и приват-доцентом университета в Петербурге. С 1859 по 1861 работал в Гейдельберге (Германия). Имея собственную лабораторию, он вел научные поиски в пока не определенном направлении. Однако после Международного съезда химиков 1860 года в Карлсруэ ученый пришел к выводу, что работать следует в направлении атомных масс (в то время применялся термин «атомный вес»).
В 1862 изобретатель по уговорам сестры женился на Феозвой Никитичной Лещевой. Так и не ужился со своей первой женой Менделеев. Дети, однако, пользовались особой нежностью отца. Вскоре он купил имение Боблово, напоминающее ему родной Тобольск. Скудные земли тех мест хорошо подходили для его сельскохозяйственных экспериментов. Он занялся анализом удобрений и условий, влияющих на урожай, обучал крестьян эффективному земледелию. В результате количество урожая, учитывая скудность земель, было удивительно большим.

Результаты Менделеевской докторской диссертации о смешивании воды и этилового спирта, которую ученый защитил в 1865, положены в основу алкоголеметрии в Голландии, Австрии, Германии и России.
Дальнейшие научные поиски привели к созданию в начале 1869 года Периодической системы. Большинство академий мира избрали создателя таблицы элементов своим членом, а самые знаменитые университеты – почетным доктором.
Брак великого изобретателя не был счастливым, и весной 1877 он завел роман с 17-летней художницей. Через 3 года ученый, наконец, расстался с семьей, и в апреле 1882 они обвенчались. С тех пор в доме часто стали бывать художники – Репин, Ярошенко, Куинджи.
С 1892 великий химик стал главным хранителем депо мер и весов. И за считанные годы превратил это учреждение в крупный научный центр. Недаром с юных лет он любил точные измерения и чувствительные инструменты.
20 января 1907 года в Санкт-Петербурге от пневмонии умер Менделеев. Краткая биография великого ученого свидетельствует о его подлинной преданности родине и науке. Похоронен Дмитрий Иванович на Волковском кладбище.
Менделеев Дмитрий Иванович интересные факты из жизни
7 августа 1897 уже немолодой химик решил оторваться от Земли на воздушном шаре с опытным аэронавтом для наблюдения солнечного затмения. Перед самым подъемом начался дождь, и очевидно было, что намокший шар не сможет поднять двух человек. Аэронавт выпрыгнул из корзины, а шар неожиданно начал подниматься. Ученому, впервые в жизни взлетевшему на воздушном шаре, ничего не оставалось, как провести задуманное в одиночку. Оказавшись над плотными облаками, он пронаблюдал полное затмение, а затем посадил шар.

Накануне погребения мозг великого химика был изъят для исследования в надежде узнать причину его гениальности, а также гениальности вообще. Через год профессор Бехтерев сообщил, что мозг покойного ученого отличается особой развитостью и избытком извилин. Не считал себя гениальным, пожалуй, только сам Менделеев. Интересные факты из жизни великого химика, впрочем, не ограничиваются этими двумя.
Что изобрел Дмитрий Иванович Менделеев для нужд армии
В 1890—1892 годах Дмитрий Иванович вместе с И. М. Чельцовым работал над созданием бездымного пороха. В декабре 1890 им была получена растворимая нитроклетчатка – продукт взаимодействия целлюлозы с азотной кислотой. А в январе 1891 — особый ее вид, названный создателем «пироколлодий». Ученый разработал на основе пироколлодия собственный рецепт бездымного пороха, который оказался лучше заграничного.
Частый вопрос, задаваемый в кроссвордах и викторинах, звучит примерно так: «Всем известен Менделеев Дмитрий Иванович. Что изобрел для нужд армии (5 букв) этот ученый?». Разумеется, ответ прост, но не слишком внимательные люди отвечают: «бездымный пироколлоидный порох», когда в действительности порох является пироколлодийным.

Менделеев Дмитрий Иванович достижения в химии и науке
За свою сознательную жизнь ощутимый вклад в самые разные научные сферы внес Д. И. Менделеев. Открытия ученого принесли огромную пользу миру и особенно России. Далее перечислены и кратко пояснены его основные научные достижения:
- Открытие Периодического закона – одного из фундаментальных законов мироздания, неотъемлемого для всего естествознания.
- Вывод уравнения идеального газа. Это уравнение выражает взаимозависимость между объемом, давлением и температурой любого газа, если пренебречь размерами и потенциальной энергией его молекул, а также временем, которое занимают их столкновения.
- Предложение ввести термодинамическую шкалу температур.
- Создание Учения о растворах, где показана связь свойств и химического состава растворов.
- Создание пироколлодийного бездымного пороха.
- Внедрение новых методов перегонки нефти, идеи постройки нефрепроводов. В итоге, Россия была превращена из импортера в экспортера нефтепродуктов.
- Создание точной теории весов.
Менделеев Дмитрий Иванович: таблица Менделеева
Между свойствами тех или иных химических элементов обнаруживалось как сильное сходство, так и резкий контраст. Предпринимавшиеся попытки классификации элементов были далеки от совершенства.
Гениальный химик обнаружил, что если элементы с похожими свойствами расположить в порядке возрастания массы атома, то они оказываются расположенными и в порядке изменения выраженности общих свойств. Если же расположить по возрастанию веса атома все известные элементы, то в этом случае ряд окажется разделенным на отрезки, внутри которых соблюдается закономерное изменение характеристик элементов. Отсюда следует закон: характеристики химических элементов состоят в периодической зависимости от массы их атома.
Для наглядности систематизации элементов целесообразно представлять их в виде таблицы. Где строки образуют периоды – отрезки, о которых было сказано только что. А столбцы составляют группы сходных элементов, расположенных по убыванию или возрастанию выраженности их общих свойств.
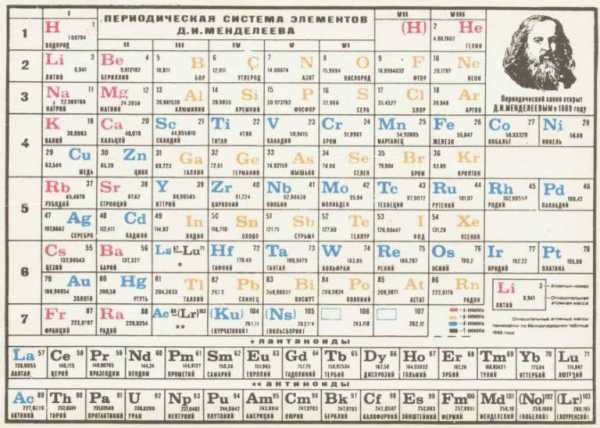
С помощью Периодической системы удалось предсказать существование еще не известных элементов и даже детально определить свойства некоторых из них. Что и сделал Менделеев Дмитрий Иванович. Таблица его до настоящего времени остается наиболее удачной классификацией элементов химии.
Самое важное в жизни рассмотрено у такого ученого, как Менделеев Дмитрий Иванович (краткая биография). И его открытия оставили заметный след в науке России. А вы как считаете – эти достижения важны? Оставьте свое мнение или отзыв для всех на форуме.
womaninc.ru
Дмитрий Иванович Менделеев, открытие периодического закона. Таблица Менделеева
Менделеев жил и творил в эпоху бурного расцвета естествознания, когда наука одну за другой открывала тайны природы. Эта эпоха дала миру много славных имен. Среди них особое место занимало и занимает имя великого русского химика, который, смело бросив взор на десятилетия вперед, своим открытием намного опередил эпоху.
Детство
Детство Менделеева прошло в Сибири. Он был младшим в многочисленной семье директора Тобольской гимназии — Ивана Павловича Менделеева.
Дети развивались под сильным влиянием матери, Марии Дмитриевны Менделеевой. Великий ученый всегда говорил о своей матери с чувством глубокой любви и уважения.
Мария Дмитриевна воспитывала детей строго, приучала их к труду и старалась в каждом развить его природные дарования. Она собрала довольно большую библиотеку и много читала детям. Маленький Менделеев — живой одаренный мальчик — был любимцем матери. Наделенный отличной памятью, которую он не утратил до конца жизни, мальчик жадно усваивал и то, что прочитывала ему мать, и то, что он наблюдал вокруг.
До поступления в гимназию мальчик жил в тридцати верстах от Тобольска. Здесь Мария Дмитриевна управляла стекольным заводом, переданным ей богатым ее братом. На этом заводе будущий великий химик впервые увидел превращение смеси из песка, известняка и соды в прозрачное, тонкое стекло. Он наблюдал, как рабочие с помощью трубок выдували из расплавленной массы «холявы» — длинные цилиндры, которые потом развертывали в листы оконного стекла. Он видел, как делали бутылки, стаканы, банки. Несомненно, что эти детские наблюдения не прошли бесследно для будущего химика.
В гимназию Менделеева отдали рано, на год раньше, чем следовало по возрасту. Вся семья снова переехала в Тобольск, который покинула после того, как Иван Павлович, потеряв зрение, вышел на пенсию.
|
|
Юность
В гимназические годы Менделеев много читал. В Тобольске тогда жили ссыльные декабристы. Они бывали у Менделеевых, и общение с ними, конечно, оказало влияние на вдумчивого, впечатлительного юношу. Ведь декабристы были образованнейшими людьми своего времени.
Быстро пролетели гимназические годы. Надо было подумать о том, чтобы продолжить образование. К тому времени умер отец Менделеева. Завод, которым управляла Мария Дмитриевна, сгорел. Большая семья была сильно стеснена в средствах, потому что существовала на скромную пенсию. Несмотря на это, Мария Дмитриевна решила обязательно дать своему младшему сыну высшее образование и выехала с ним в Москву. Поступить в Московский университет Менделееву не удалось. В те годы существовал закон, по которому в университет принимали только тех, кто окончил гимназию в том же учебном округе. А Тобольская гимназия, которую окончил Менделеев, причислена была к Казанскому округу.
В Петербургский университет Менделееву поступить было нельзя по той же причине, что и в московский. Мария Дмитриевна решила определить сына в Главный педагогический институт, который когда-то окончил Иван Павлович Менделеев. После долгих хлопот Менделеев был принят. Мария Дмитриевна осталась в Петербурге. Мужественная женщина готова была перенести всякие лишения ради любимого сына. Она сняла, из экономии, дешевый угол и отказывала себе во всем. Вскоре после поступления сына в институт, осенью 1850 года, Мария Дмитриевна заболела и умерла.
Менделеев остался один в чужом огромном городе.
 Н. А. Ярошенко. Д. И. Менделеев. 1886. Масло.
Н. А. Ярошенко. Д. И. Менделеев. 1886. Масло.Главный педагогический институт
Главный педагогический институт был закрытым учебным заведением с очень строгим режимом. Студенты жили в казенном помещении и уже в седьмом часу утра должны были в полной форме являться в классы для самостоятельных занятий. Студентам младшего курса даже не раз-решали выходить на прогулки без сопровождающих.
Менделеева такой режим тяготил меньше, чем других. С первых же дней своей студенческой жизни будущий химик проявил редкостную усидчивость и упорство в занятиях. Он глубоко изучал не только химию и физику, но и другие родственные науки. Его интересовали все отрасли естествознания. Сохранился до наших дней гербарий, собранный Менделеевым еще в студенческие годы.
Терпеливо искать научную правду, добывать ее упорным. постоянным трудом — таков был девиз великого химика. Этого девиза он придерживался всю жизнь.
Учителями Менделеева в Главном педагогическом институте были выдающиеся ученые: физик Э. X. Ленц, математик М. В. Остроградский, химик А. А. Воскресенский.
Интерес к химии проявился у Менделеева уже с первого курса. Неудивительно, что А. А. Воскресенский оценил способности одного из лучших своих учеников и уделял ему много внимания.
Еще на студенческой скамье Менделеевым была написана исследовательская работа, которая привлекла всеобщее внимание. Она была посвящена изучению кристаллических форм минералов. Уже в этой работе Менделеев подчеркивает черты сходства в поведении различных элементов. Эти важные наблюдения были как бы отправным пунктом для больших поисков, которые впоследствии привели ученого к великим открытиям.
Менделеев окончил институт с золотой медалью. Его учителя, профессора Воскресенского, поздравляли с блестящей подготовкой выпускника. Работа о минералах стала кандидатской диссертацией, которую Дмитрий Иванович защитил при выпуске.
 Илья Репин. Портрет Д. И. Менделеева в мантии доктора права Эдинбургского университета. 1885; акварель
Илья Репин. Портрет Д. И. Менделеева в мантии доктора права Эдинбургского университета. 1885; акварельНаучная деятельность
Менделеев вступил на путь самостоятельного научного творчества. Молодой химик не знал устали в труде. В 1856 году он защитил магистерскую диссертацию. Как и в предыдущей студенческой работе, так и в этом исследовании, посвященном удельным объемам твердых, жидких и газообразных тел, Менделеева особенно интересовала повторяемость свойств простых тел при возрастании их атомного веса. Эти его первые работы имели немалое значение для открытия периодического закона.
В том же году молодой магистр физики и химии, которому пошел лишь двадцать третий год, защитил вторую диссертацию — «О строении кремнеземистых соединений», дающую право читать лекции студентам.
Получив научное звание магистра, Менделеев стал доцентом Петербургского университета. Помимо чтения лекций и научной работы, молодой ученый развил кипучую общественную деятельность. В своих статьях, заметках, отзывах на книги Менделеев доказывает необходимость развития отечественной русской промышленности, особенно химической. Уже тогда в Менделееве определилась одна важная черта, — он никогда не был ученым-затворником, а всегда сочетал науку с практикой.
 Весы, сконструированные Д. И. Менделеевым для взвешивания газообразных и твёрдых веществ
Весы, сконструированные Д. И. Менделеевым для взвешивания газообразных и твёрдых веществВ 1859 году Менделеев отправился в первую свою заграничную поездку. Он проработал несколько лет в немецком университетском городе Гейдельберге. В квартире, где жил Менделеев, он организовал собственную лабораторию и провел ряд выдающихся исследований свойств жидкостей. Вернувшись на родину в 1861 году, молодой ученый сразу окунулся в работу. В Петербургском университете он читал лекции по органической химии. Но, кроме того, он преподавал и в других учебных заведениях, писал для студентов курс «Органической химии», выступал в журналах со статьями.
На тридцать первом году жизни, после блестящей защиты докторской диссертации «О соединениях спирта с водой», Менделеев был избран профессором Петербургского университета. В этой работе Д. И. Менделеев изложил основы созданной им химической теории растворов.
Периодический закон и таблица Менделеева
Еще несколько лет прошли в упорном, неустанном труде. В 1869 году Менделеев должен был выступить с докладом на очередном заседании Русского химического общества. Но сам докладчик на это заседание, ставшее историческим, явиться не мог. Болезнь приковала Дмитрия Ивановича к постели. Вместо Менделеева на кафедру взошел его товарищ — профессор Н. А. Меншуткин — и показал собранию таблицу, которая называлась: «Опыт системы элементов, основанный на их атомном весе и химическом сходстве». Вслед за тем Меншуткин огласил доклад, написанный автором таблицы — Дмитрием Ивановичем Менделеевым. Это и была обошедшая потом весь мир «Таблица Менделеева».
Так стало известно об открытии закона, составляющего основу всей современной химии.

www.alto-lab.ru
Дмитрий Иванович Менделеев и периодическая таблица элементов — доклад
Химия — наука непростая, а в 19 веке — ещё и опасная! Масса неописанных веществ и неисследованных соединений, законы естествознания ещё не раскрыты. Именно в это время в Тобольске в 1834 году родился будущий химик Д.И. Менделеев. Биография учёного — это настоящее противоречие и работа над собой.
Что интересно, будущий гениальный химик в школе считался редкой посредственностью. В институт поступил со второй попытки и то по просьбе матери. Но закончил учёбу с дипломом и золотой медалью.
В 1864 году — Д.И. Менделеев уже профессор химии в Петербургском технологическом университете. В это же время Дмитрий Иванович защищает диссертацию о «О соединении спирта с водой». Позднее некоторые пытливые умы припишут ему изобретение водки. Но самое известное его открытие — периодическая система элементов — ещё в будущем.

Периодическая система Д.И. Менделеева. Гениально и просто!
Многие известные открытия происходят случайно. В 1866 году Дмитрий Иванович возглавляет кафедру неорганической химии Петербургского технологического университета.
На своих занятиях учёный понимает, что у студентов нет доступного раздаточного материала для работы. И он начинает разработку собственного наглядного пособия, которое в дальнейшем получило название «Периодическая система» и прославило своего изобретателя.
В чем гениальность таблицы Менделеева?
В середине 19 века было известно уже много химических элементов и описаны их свойства. Но единой системы не существовало. Были отдельные попытки создать некоторую классификацию известных элементов, но ни к чему хорошему это не привело.
Дмитрий Иванович решил просто выстроить известные химические элементы по возрастанию их молекулярной массы. Он замечает некоторую закономерность — периодически повторяется цикл — щелочной металл, затем щёлочно-земельный, затем переходные вещества, затем неметаллы и заканчивается благородными газами. И снова все начинается со щелочного металла.
Таким образом, Д.И. Менделеев отметил, что все элементы образуют некие группы с повторяющимися физико-химическими свойствами. Это позволило предугадать открытие новых веществ — галлия, скандия, астата, франция. В 1869 году доклад о периодических свойствах элементов был представлен Русскому химическому обществу.
В 20 веке учёные смогли заглянуть в мельчайшую частицу вещества — атом. И вот тут и стало ясно, что периодическая система — это гениальное открытие!
- Дело в том, что ядро атома состоит из протонов и нейтронов. И количество положительных частиц — протонов — в любом веществе равно номеру этого элемента в таблице Менделеева.
- Вокруг ядра вращаются электроны, и их количество также соответствует порядковому номеру элемента. Отрицательные частицы вращаются по орбиталям. И количество электронных орбиталей равно номеру периода таблицы, в котором находится тот или иной элемент.
- На последней орбитали вращается разное число электронов. Но их количество соответствует порядковому номеру ряда, в котором находится элемент.
- В настоящее время периодический закон звучит иначе, чем задумывал его автор. Но это отнюдь не умаляет заслуг автора.
Деятельность Д.И Менделеева — это череда гениальных открытий и изобретений. Но они меркнут перед главным его детищем — периодической системой химических элементов.
Если это сообщение тебе пригодилось, буда рада видеть тебя в группе ВКонтакте. А ещё — спасибо, если ты нажмёшь на одну из кнопочек «лайков»:
Вы можете оставить комментарий к докладу.
www.doklad-na-temu.ru
Периодическая система Дмитрия Ивановича Менделеева и её значение для естествознания
Периодическая система Дмитрия Ивановича Менделеева и её значение для естествознания
Введение
Открытие Д.И.Менделеевым закономерностей в строении материи оказалась очень важной вехой в развитии мировой науки и мысли. Гипотеза о том, что все вещества во Вселенной состоят лишь из нескольких десятков химических элементов в 19 веке казалась совершенно невероятной, но она была доказана «Периодической системой элементов» Менделеева.
Открытие периодического закона и разработка периодической системы химических элементов Д. И. Менделеевым явились вершиной развития химии в XIX веке. Обширная сумма знаний о свойствах 63 элементов, известных к тому времени, была приведена в стройный порядок.
Периодическая система элементов
Д. И. Менделеев считал, что основной характеристикой элементов являются их атомные веса, и в 1869 г. впервые сформулировал периодический закон.
Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов.
Весь ряд элементов, расположенных в порядке возрастания атомных масс, Менделеев разбил на периоды, внутри которых свойства элементов изменяются последовательно, разместив периоды так, чтобы выделить сходные элементы.
Однако, несмотря на огромную значимость такого вывода, периодический закон и система Менделеева представляли лишь гениальное обобщение фактов, а их физический смысл долгое время оставался непонятным. Лишь в результате развития физики XX века — открытия электрона, радиоактивности, разработки теории строения атома — молодой, талантливый английский физик Г. Мозле установил, что величина зарядов ядер атомов последовательно возрастает от элемента к элементу на единицу. Этим открытием Мозле подтвердил гениальную догадку Менделеева, который втрех местах периодической таблицы отошел от возрастающей последовательности атомных весов.
Так, при ее составлении Менделеев поставил 27Со перед 28Ni, 52Ti перед 5 J, 18Аг перед 19К, несмотря на то, что это противоречило формулировке периодического закона, то есть расположению элементов в порядке увеличения их атомных весов.
Согласно закону Мозле заряды ядерданных элементов соответствовали положению их в таблице.
В связи с открытием закона Мозле современная формулировка периодического закона следующая:
свойство элементов, а так же формы и свойства их соединений находятся в периодической зависимости от заряда ядра их атомов.
Итак, главной характеристикой атома является не атомная масса, а величина положительного заряда ядра. Это более общая точная характеристика атома, а значит, и элемента. От величины положительного заряда ядра атома зависят все свойства Элемента и его положение в периодической системе. Таким образом, порядковый номер химического элемента численно совпадает с зарядом ядра его атома. Периодическая система элементов является графическим изображением периодического закона и отражает строение атомов элементов.
Теория строения атома объясняет периодическое изменение свойств элементов. Возрастание положительного заряда атомных ядер от 1-до 110 приводит к периодическому повторению у атомов элементов строения внешнего энергетического уровня. А поскольку от числа электронов на внешнем уровне в основном зависят свойства элементов; то и они периодически повторяются. В этом физический смысл периодического закона.
В качестве примера рассмотрим изменение свойств у первых и последних элементов периодов. Каждый период в периодической системе начинается элементами атомы, которых на внешнем уровне имеют один s-электрон (незавершенные внешние уровни) и потому проявляют сходные свойства — легко отдают валентные электроны, что обуславливает их металлический характер. Это щелочные металлы — Li, Na, К, Rb, Cs.
Заканчивается период элементами, атомы которых на внешнем уровне содержат 2 (s2) электрона (в первом периоде) или 8 (s1p6)электронов (во всех последующих), то есть имеют завершенный внешний уровень. Это благородные газы Не, Ne, Ar, Kr, Xe, имеющие инертные свойства.
Именно вследствие сходства строения внешнего энергетического уровня похожи их физические и химические свойства.
В каждом периоде с возрастанием порядкового номера элементов металлические свойства постепенно ослабевают и возрастают неметаллические, заканчивается период инертным газом. В каждом периоде с возрастанием порядкового номера элементов металлические свойства постепенно ослабевают и возрастают неметаллические, заканчивается период инертным газом.
В свете учения о строении атома становится понятным разделение всех элементов на семь периодов, сделанное Д. И. Менделеевым. Номер периода соответствует числу энергетических уровней атома,то есть положение элементов в периодической системе обусловлено строением их атомов. В зависимости от того, какой подуровень заполняется электронами, все элементы делят на четыре типа.
1. s-элементы. Заполняется s-подуровень внешнего уровня (s1 — s2). Сюда относятся первые два элемента каждого периода.
2. р-элементы. Заполняется р-подуровень внешнего уровня (р1 — p6)-Сюда относятся последние шесть элементов каждого периода, начиная со второго.
3. d-элементы. Заполняется d-подуровень последнего уровня (d1 — d10), а на последнем (внешнем) уровне остается 1 или 2 электрона. К ним относятся элементы вставных декад (10) больших периодов, начиная с 4-го, расположенные между s- и p-элементами (их также называют переходными элементами).
4. f-элементы. Заполняется f-подуровень глубинного (треть его снаружи) уровня (f1 —f14),а строение внешнего электронного уровня остается неизменным. Это лантаноиды и актиноиды, находящиеся в шестом и седьмом периодах.
Таким образом, число элементов в периодах (2-8-18-32) соответствует максимально возможному числу электронов на соответствующих энергетических уровнях: на первом — два, на втором — восемь, на третьем — восемнадцать, а на четвертом — тридцать два электрона. Деление групп на подгруппы (главную и побочную) основано на различии в заполнении электронами энергетических уровней. Главную подгруппу составляют s— и p-элементы, а побочную подгруппу — d-элементы. В каждой группе объединены элементы, атомы которых имеют сходное строение внешнего энергетического уровня. При этом атомы элементов главных подгрупп содержат на внешних (последних) уровнях число электронов, равное номеру группы. Это так называемые — валентные электроны.
У элементов побочных подгрупп валентными являются электроны не только внешних, но и предпоследних (вторых снаружи) уровней, в чем и состоит основное различие в свойствах элементов главных и побочных подгрупп.
Отсюда следует, что номер группы, как правило, указывает число электронов, которые могут участвовать в образовании химических связей. В этом заключается физический смысл номера группы.
С позиций теории строения атома легко объясняется возрастание металлических свойств элементов в каждой группе с ростом заряда ядра атома. Сравнивая, например, распределение электронов по уровням в атомах 9F (1s2 2s2 2р5) и 53J(1s2 2s2 2р6 3s2 Зр63d104s2 4р6 4d105s2 5p5) можно отметить, что у них по 7 электронов на внешнем уровне, что указывает на сходство свойств. Однако внешние электроны в атоме йода находятся дальше от ядра и поэтому слабее удерживаются. По этой причине атомы йода могут отдавать электроны или, иными словами, проявлять металлические свойства, что нехарактерно для фтора.
Итак, строение атомов обуславливает две закономерности:
а) изменение свойств элементов по горизонтали — в периоде слева направо ослабляются металлические и усиливаются неметаллические свойства;
б) изменение свойств элементов по вертикали — в группе с ростом порядкового номера усиливаются металлические свойства и ослабевают неметаллические.
Таким образом: по мере возрастания заряда ядра атомов химических элементов периодически изменяется строение их электронных оболочек, что является причиной периодического изменения их свойств.
Структура периодической Системы Д. И. Менделеева.
Периодическая система Д. И. Менделеева подразделяется на семь периодов – горизонтальных последовательностей элементов, расположенных по возрастанию порядкового номера, и восемь групп – последовательностей элементов обладающих однотипной электронной конфигурацией атомов и сходными химическими свойствами.
Первые три периода называются малыми, остальные – большими. Первый период включает два элемента, второй и третий периоды – по восемь, четвёртый и пятый – по восемнадцать, шестой – тридцать два, седьмой (незавершённый) – двадцать один элемент.
Каждый период (исключая первый) начинается щелочным металлом и заканчивается благородным газом.
Элементы 2 и 3 периодов называются типическими.
Малые периоды состоят из одного ряда, большие – из двух рядов: чётного (верхнего) и нечётного (нижнего). В чётных рядах больших периодов расположены металлы, и свойства элементов слева направо изменяются слабо. В нечётных рядах больших периодов свойства элементов изменяются слева направо, как у элементов 2 и 3 периодов.
В периодической системе для каждого элемента указывается его символ и порядковый номер, название элемента и его относительная атомная масса. Координатами положения элемента в системе является номер периода и номер группы.
Элементы с порядковыми номерами 58-71, именуемыми лантаноидами, и элементы с номерами 90-103 — актиноиды – помещаются отдельно внизу таблицы.
Группы элементов, обозначаемые римскими цифрами, делятся на главные и побочные подгруппы. Главные подгруппы содержат 5 элементов (или более). В побочные подгруппы входят элементы периодов, начиная с четвёртого.
Химические свойства элементов обуславливаются строением их атома, а точнее строением электронной оболочки атомов. Сопоставление строения электронных оболочек с положением элементов в периодической системе позволяет установить ряд важных закономерностей:
1. Номер периода равен общему числу энергетических уровней, заполняемых электронами, у атомов данного элемента.
2. В малых периодах и нечётных рядах больших периодов с ростом положительного заряда ядер возрастает число электронов на внешнем энергетическом уровне. С этим связано ослабление металлических и усиление неметаллических свойств элементов слева направо.
Номер группы, указывает число электронов, которые могут участвовать в образовании химических связей (валентных электронов).
В подгруппах с ростом положительного заряда ядер атомов элементов усиливаются их металлические и ослабляются неметаллические свойства.
История создания Периодической системы
Дмитрий Иванович Менделеев в октябре 1897 году писал в статье «Периодическая законность химических элементов»:
— После открытий Лавуазье понятие о химических элементах и простых телах так укрепилось, что их изучение положено в основу всех химических представлений, а вследствие того взошло и во все естествознание. Пришлось признать, что все вещества, доступные исследованию, содержат очень ограниченное число материально разнородных элементов, друг в друга не превращающихся и обладающих самостоятельною весомою сущностью и что все разнообразие веществ природы определяется лишь сочетанием этих немногих элементов и различием или их самих, или их относительного количества, или при одинаковости качества и количества элементов — различием их взаимного положения, соотношения или распределения. «Простыми» телами должно при этом назвать вещества, содержания лишь один какой-либо элемент, «сложными» — два или более. Но для данного элемента могут существовать многие видоизменения простых тел, ему отвечающих, зависящие от распределения («строения») его частей или атомов, т.е. от того вида изомерии, который называется «аллотропией». Так углерод, как элемент, является в состоянии угля, графита и алмаза, которые (взятые в чистом виде) дают при сжигании один и тот же углекислый газ и в том же количестве. Для самих же «элементов» ничего подобного не известно. Они видоизменениям и взаимным превращениям не подвергаются и представляют, по современным воззрениям, неизменную сущность изменяющегося (химически, физически и механически) вещества, входящую как в простые, так и в сложные тела.
Весьма, в древности и до ныне, распространенное представление о «единой или первичной» материи, из которой слагается все разнообразие веществ, опытом не подтверждено, и все попытки, к сему направленные, оказались его опровергающими. Алхимики верили в превращение металлов друг в друга, доказывали это разными способами, но при поверке все оказалось или обманом (особенно в отношении к производству золота из других металлов), или ошибкой и неполнотой опытного исследования. Однако, нельзя не заметить, что если бы завтра оказалось, что металл А превращается целиком или отчасти в другой металл В, то из этого вовсе не будет еще следовать, что простые тела способны друг в друга превращаться вообще, как, например, из того, что долгое время закись урана считали за простое тело, а она оказалась содержащей кислород и действительный металлический уран — вовсе не следует делать никакого общего заключения, а можно только в частности судить о бывшей и современной степенях знакомства с ураном, как самостоятельным элементом. С этой точки зрения должно взглянуть и на оповещенное Емменсом (Stephen — Н. Emmeus) превращение мексиканского серебра отчасти в золото (май—июнь 1897 г.), если справедливость наблюдений оправдается и Argentaurum не окажется подобным алхимистическим оповещением подобного же рода, не раз бывшим и также прикрывавшемся покровом секрета и денежного интереса. Что холод и давление могут содействовать перемене строения и свойств — давно известно, хотя бы по примеру олова Фрицше, но нет фактов, позволяющих предполагать, что изменения эти идут столь глубоко и доходят не до строения частиц, а до того, что ныне считается атомами и элементами, а потому утверждаемое Емменсом превращение (хотя бы и постепенно) серебра в золото будет оставаться сомнительным и мaлозначущим даже в отношении к серебру и золоту, пока, во-первых, «секрет» не будет на столько раскрыт, что опыт может быть всеми воспроизведен, и во-вторых, пока обратный переход (при накаливании и уменьшении давления?) золота в серебро не будет установлен, или пока не будет установлена фактическая его невозможность или трудность. Легко понять, что переход спирта углекислоты в сахар труден, хотя обратный идет легко, потому что сахар бесспорно сложнее спирта и углекислоты. И мне кажется очень мало вероятным переход серебра в золото, если обратно — золото не будет переходить в серебро, потому что атомный вес и плотность золота чуть не в два раза более, чем серебра, из чего должно, по всему известному в химии, заключить, что если серебро и золото произошли из одного материала, то золото сложнее серебра и должно превращаться в серебро легче, чем обратно. Поэтому я думаю, что г. Емменсу для убедительности не только следовало бы раскрыть «секрет», но и попробовать, да и показать, если можно, превращение золота в серебро, тем более, что при получении из дорогого металла другого, в 30 раз более дешевого, денежные интересы будут, очевидно, на далеком плане, а интересы правды и истины окажутся явно на первом, теперь же дело представляется, на мой взгляд, с обратной стороны.
При таком представлении о химических элементах — они оказываются чем-то отвлеченным, так как в отдельности мы их не видим и не знаем. К такому почти идеалистическому представлению столь реалистическое знание, как химия, пришло по совокупности всего доныне наблюденного, и если это представление можно отстаивать, то лишь как предмет глубоко укоренившегося убеждения, доныне оказавшегося совершенно согласным с опытом и наблюдением. В этом смысле понятие о химических элементах имеет глубоко реальное основание во всей науке о природе, так как, например, углерод нигде, никогда, никем и нисколько не превращен в какой-либо другой элемент, тогда как простое тело — уголь превращено в графит и алмаз и, быть может, когда-нибудь можно будет превратить его и в вещество жидкое или газообразное, если удастся найти условия упрощения сложнейших частиц угля. Главное понятие, с которым возможно приступить к объяснению П. законности, состоит именно в коренном различии представлений об элементах и о простых телах. Углерод — элемент, нечто неизменное, содержащееся, как в угле, так и в углекислом газе или в светильном, как в алмазе, так и в массе изменчивых органических веществ, как в известняке, так и в дереве. Это — не конкретное тело, а весомое (материальное) вещество с суммой свойств. Как в парах воды или в снеге нет конкретного тела — жидкой воды, а есть то же весомое вещество с суммой ему одному принадлежащих свойств, так во всем углеродистом содержится материально-однородный углерод: не уголь, а именно углерод. Простые тела суть вещества, содержащие только один какой-либо элемент, и понятие о них становится прозрачно-ясным только тогда, когда признается укрепившееся представление об атомах и частицах или молекулах, из которых слагаются однородные вещества; причем понятию об элементе отвечает атом, а простому телу — частица. Простые тела, как и все тела природы, составлены из частиц: вся их разница от сложных тел состоит лишь в том, что частицы сложных тел содержат разнородные атомы двух или многих элементов, а частицы простых тел — однородные атомы данного элемента. Все, что излагается далее, должно относить именно к элементам, т.е. напр. к углероду, водороду и кислороду, как составным частям сахара, дерева, воды, угля, кислородного газа, озона и т.п., но не простым телам, элементами образуемыми. При этом, очевидно, является вопрос: как же можно находить какую-либо реальную законность в отношении к таким предметам, как элементы, существующие лишь как представления современных химиков, и что же реально осуществимое можно ожидать, как следствие из расследования каких-то отвлеченностей? Действительность отвечает на подобные вопросы с полною ясностью: отвлечения, если они правдивы (содержат элементы истины) и соответствуют реальности, могут служить предметом точно такого же исследования, как и чисто материальные конкретности. Так химические элементы, хотя суть отвлеченности, подлежат расследованию совершенно такому же, как простые или сложные тела, которые можно накалить, взвесить и вообще подвергать прямому наблюдению. Сущность дела здесь в том, что у химических элементов, на основании опытного исследования простых и сложных тел, ими образуемых, открываются свои индивидуальные свойства и признаки, совокупность которых и составляет предмет исследования. Мы и обратимся теперь к перечислению некоторых из особенностей, принадлежащих химическим элементам, чтобы затем показать П. законность химических элементов.
Свойства химических элементов должно разделить на качественные и количественные, хотя бы первые из них и сами по себе подлежали измерению. К числу качественных прежде всего принадлежит свойство образовать кислоты и основания. Хлор может служить образцом первых, так как и с водородом, и кислородом образует явные кислоты, способные с металлами и основаниями давать соли, начиная с первообраза солей — поваренной соли. Натрий же поваренной соли NaCl может служить образцом элементов, дающих только основания, так как кислотных окислов с кислородом он не дает, образуя или основание (окись натрия), или перекись, обладающую характерными признаками типической перекиси водорода. Все элементы суть более или менее кислотные или основные, с явными переходами от первых ко вторым. Это качественное свойство элементов электрохимики (с Берцелиусом во главе) выразили, отличив сходных с натрием, на основании того, что первые при разложении током являются на аноде, а вторые на катоде. Тоже качественное различие элементов выражается отчасти и в различении металлов и металлоидов, так как основные элементы относятся к числу таких, которые в виде простых тел дают настоящие металлы, а кислотные элементы образуют в виде простых тел металлоиды, не имеющие вида и механических свойств настоящих металлов. Но во всех этих отношениях не только невозможно прямое измерение, позволяющее устанавливать последовательность перехода от одних свойств к другим, но и нет резких различий, так что есть элементы в том или ином отношении переходные или такие, которые можно отнести и в тот, и в другой разряд. Так алюминий, по внешнему виду явный металл, отлично проводящий гальв. ток, в своем единственном окисле Аl2O3 (глинозем) играет роль то основную, то кислотную, так как соединяется и с основаниями (напр. Na2O, MgO и др.), и с кислотными окислами, например образуя серноглиноземную соль A12(SO4)3=Al2O33O3; и в том, и в другом случае он обладает слабо выраженными свойствами. Сера, образуя несомненный металлоид, во множестве химических отношений сходна с теллуром, который по внешним качествам простого тела всегда относился к металлам. Такие случаи, очень многочисленные, придают всем качественным признакам элементов некоторую степень шаткости, хотя и служат к облегчению и, так сказать, оживлению всей системы знакомства с элементами, указывая в них признаки индивидуальности, позволяющей предугадывать еще не наблюденные свойства простых и сложных тел, образующихся из элементов. Эти сложные индивидуальные особенности элементов придавали чрезвычайный интерес открытию новых элементов, не позволяя никоим образом сколько-нибудь предвидеть сумму физических и химических признаков, свойственных веществам, ими образуемым. Все, чего можно было достигать при изучении элементов, ограничивалось сближением в одну группу наиболее сходных, что уподобляло все это знакомство с систематикою растений или животных, т.е. изучение было рабским, описательным и не позволяющим делать какие-либо предсказания по отношению к элементам, еще не бывшим в руках исследователей. Ряд иных свойств, которые мы назовем количественными, выступил в надлежащем виде для химических элементов только со времени Лорана и Жерара, т.е. с 50-х годов текущего столетия, когда была подвергнута исследованию и обобщению способность взаимного реагирования со стороны состава частиц и укрепилось представление о двуобъемных частицах, т.е. о том, что в парообразном состоянии, пока нет разложения, всякие частицы (т.е. количества веществ, вступающие в химическое взаимодействие между собою) всех тел занимают такой же объем, какой занимают два объема водорода при той же температуре и том же давлении. Не входя здесь в изложение и развитие начал, укрепившихся при этом, ныне общепринятом представлении, достаточно сказать, что с развитием унитарной или частичной химии в последние 40 или 50 лет получилась твердость, прежде не существовавшая, как в определении атомных весов элементов, так и в определении состава частиц простых и сложных тел, ими образуемых, и стала очевидною причина различия свойств и реакций обыкновенного кислорода О2 и озона O3, хотя оба содержат только кислород, как и разность маслородного газа (этилена) C2H4 от жидкого цетена С16Н32, хотя оба содержат на 12 весовых частей углерода по 2 весовых части водорода. В эту многознаменательную эпоху химии выступило в ней для каждого хорошо обследованного элемента два более или менее точных количественных признака или свойства: вес атома и тип (форма) состава частиц соединений, им образуемых, хотя ничто не указывало еще ни на взаимную связь этих признаков, ни на соотношение их с другими, особенно качественными, свойствами элементов. Вес атома, свойственный элементу, т.е. неделимое, наименьшее относительное количество его, входящее в состав частиц всех его соединений, особенно был важен для изучения элементов и составлял их индивидуальную характеристику, пока чисто эмпирического свойства, так как для определения атомного веса элемента надобно узнать не только эквивалент или относительный весовой состав некоторых его соединений с элементами, вес атома которых известен из иных определений, или условно принят известным, но и определить (по реакциям, плотностям паров и т.п.) частичный вес и состав хоть одного, а лучше многих из соединений, им образуемых. Этот путь опыта столь сложен, длинен и требует такого совершенно очищенного и тщательно изученного материла из числа соединений элемента, что для многих, особенно для редких в природе элементов, при отсутствии особо понудительных причин, оставалось много сомнений относительно истинной величины атомного веса, хотя весовой состав (эквивалент) некоторых соединений их и был установлен; таковы, напр., были уран, ванадий, торий, бериллий, церий и др. При чисто эмпирическом значении веса атома не было и особого интереса углубляться в этот предмет для элементов, редко подвергаемых исследованию, тем не менее для большой массы обыкновеннейших элементов величины атомных весов можно было уже в начале 60-х годов считать твердо установленными, особенно после того, как Канницаро твердо установил для многих металлов, напр. Са, Ва, Zn, Fe, Сu и т.п. явное их отличие от К, Na, Ag и т.п., показав, что частицы напр. хлористых соединений первых из них содержат вдвое более хлора, чем вторых, т.е. что Са, Ва, Zn и т.д. дают CaCI2, BaCI2 и т.д., т.е. двуатомны (двуэквивалентны или двувалентны), тогда как K, Na и т.п. одноатомны (одноаквивалентны), т.е. образуют KCI, NaCI и т.п. В эпоху около середины текущего столетия вес атома элементов послужил уже одним из признаков, по которым стали сличать сходственные элементы групп.
Другой из важнейших количественных признаков элементов представляет состав частиц высших соединений, им образуемых. Здесь более простоты и ясности, потому что Дальтонов закон кратных отношений (или простоты и цельности числа атомов, входящих в состав частиц) уже заставляет ждать только немногих чисел и разобраться в них было легче. Обобщение выразилось в учении об атомности элементов или их валентности. Водород есть элемент одноатомный, ибо дает по одному соединению HX с другими одноатомными же элементами, представителем которых считался хлор, образуя НСl. Кислород двуатомен, потому что дает H2O или соединяется вообще с двумя X, если под Х подразумевать одноатомные элементы. Так получают НСlO, Сl2О и т.д. В этом смысле азот считается трехатомным, так как дает NH3, NCl3; углерод четырехатомным, потому что образует СН4, СО2 и т.д. Сходные элементы одной группы, напр. галоиды, дают и сходные частицы соединений, т.е. имеют одну и ту же атомность. Через все это изучение элементов очень сильно двинулось вперед. Но было немало трудностей разного рода. Особую трудность представили соединения кислорода, как элемента двуатомного, способного замещать и удерживать X2, в силу чего совершенно понятно образование Cl2O, HClO и т.п. соединений с одноатомными элементами. Однако, тот же кислород дает не только НСlO, но и HClO2, НСlO3 и НСlO4 (хлорная кислота), точно также как не только H2O, но и H2O2 (перекись водорода). Для объяснения пришлось признать, что кислород, в силу своей двуатомности, обладая двумя сродствами (как говорят), способен втиснуться в каждую частицу и встать между всякими двумя атомами, в нее входящими. Трудностей при этом получилось много, но остановимся на двух, по-моему, важнейших. Во-первых, оказалась как бы грань О4 для числа кислородных атомов, входящих в частицу, а этой грани нельзя ждать на основании допущенного. При том, приближаясь к грани, получались часто соединения не менее, а более прочные, чего уже вовсе нельзя допустить при представлении о втиснутых атомах кислорода, так как чем более их взойдет, тем вероятнее было иметь непрочность связей. А между тем НСlO4 прочнее НСlO3, эта последняя прочнее НСlO2 и НСlO, тогда как НСl опять тело химически очень прочное. Грань же О4 выступает в том, что водородным соединениям разной атомности:
НСl, H2S, Н3Р и H4Si
отвечают высшие кислородные кислоты:
НСlO4, H2SO4, Н3РО4 и H4SiO4,
в которых одинаково содержатся четыре атома кислорода. Из этого даже выходит тот неожиданный вывод, что считая Н — одно-, а О — двуатомными элементами, по кислороду способность к соединению выходит обратная, чем по водороду, т.е. по мере того как у элементов увеличивается свойство удерживать атомы водорода или возрастать в атомности, уменьшается способность удерживать кислород; хлор, так сказать, одноатомен по водороду и семиатомен по кислороду, а фосфор или аналогический с ним азот трехатомен в первом смысле, а во втором — пятиатомен, что видно и по другим соединениям, например NH4CI, POCl3, РСl5 и т.п. Во-вторых, все, что знаем, явно указывает на глубочайшее различие в присоединении кислорода (втискивании его, судя по представлению об атомности элементов) в том случае, когда образуется перекись водорода, от того, когда происходит напр. из H2SO4 (сернистая кисл.) серная кислота H2SO4, хотя H2O2 отличается от Н2O точно также атомом кислорода, как H2SO4 от H2SO3, и хотя раскислители в обоих случаях переводят высшую степень окисления в низшую. Разность в отношении к реакциям, свойственным H2O2 и H2SO4, особенно выступает по той причине, что серной кислоте отвечает своя перекись (надсерная кислота, аналог которой надхромовая недавно изучена Wiede и содержит, по его данным, H2CrO5), обладающая совокупностью свойств перекиси водорода. Значит, есть существенная разность в способе присоединения кислорода в «солеобразных» окислах и настоящих перекисях и, значит, простым втискиванием атомов кислорода между другими выражать все случаи присоединения кислорода недостаточно, а если выражать, то скорее всего это следует применять к перекисям, а не к образованию, так сказать, нормальных соединений кислорода, приближающихся к RHnО4, где n, число атомов водорода, не бывает более 4, как и число атомов кислорода в кислотах, содержащих один атом элементов R. Приняв сказанное во внимание и означая вообще через R атом элементов, вся совокупность сведений о солеобразных окислах приводится к тому выводу, что число самостоятельных форм или видов окислов очень не велико и ограничивается следующими восемью:
R2O, напр. K2O, Ag2O.
R2O2 или RO, напр. CaO, FeO.
R2O3, напр. Al2O3, N2O3.
R2O4 или RO2, напр. CO2, SiO2.
R2O5, напр. N2O5, P2O5.
R2O6 или RO3, напр. SO3, CrO3.
R2O7, напр. Cl2O7, Mn2O7.
R2O8 или RO4, напр. OsO4, RuO4.
Эта стройность и простота форм окисления вовсе не вытекает из учения об атомности элементов в его обычной форме (при определении атомности по соединению с Н или Сl) и есть дело прямого сличения кислородных соединений самих по себе. Вообще учение о постоянной и неизменной атомности элементов заключает в себе трудности и несовершенства (не насыщенные соединения, подобные СО, пересыщенные, подобные JCl3, соед. с кристаллизационною водою и т.п.), но оно в двух отношениях имеет и поныне важное значение, а именно с ним достигнута простота и стройность выражения состава и строения сложных органических соединений, и в отношении к выражению аналогии сродственных элементов, так как атомность, по чему бы ее не считали (или состав частиц сходственных соединений), в таком случае оказывается одинаковою. Так напр. сходные между собою во многом ином галоиды или же металлы данной группы (щелочные, напр.) оказываются всегда обладающими одинаковою атомностью и образующими целые ряды сходных соединений, так что существование этого признака есть уже до некоторой степени указатель аналогии.
Чтобы не усложнять изложения, мы оставим перечисление других качественных и количественных свойств элементов (напр. изоморфизма, теплот соед., показ, преломления и т.п.) и прямо обратимся к изложению П. закона, для чего остановимся: 1) на сущности закона, 2) на его истории и приложении к изучению химии, 3) на его оправдании при помощи вновь открытых элементов, 4) на приложении его к определению величины атомных весов и 5) на некоторой неполноте существующих сведений.
Сущность П. законности. Так как из всех свойств химических элементов атомный их вес наиболее доступен для численной точности определения и для полной убедительности, то исходом для нахождения законности химических элементов всего естественнее положить веса атомов, тем более, что в весе (по закону сохранения масс) мы имеем дело с неуничтожаемым и важнейшим свойством всякой материи. Закон есть всегда соответствие переменных, как в алгебре функциональная их зависимость. Следовательно, имея для элементов атомный вес как одну переменную, для отыскания закона элементов следует брать иные свойства элементов, как другую переменную величину, и искать функциональной зависимости. Взяв многие свойства элементов, напр. их кислотность и основность, их способность соединяться с водородом или кислородом, их атомность или состав их соответственных соединений, теплоту, выделяемую при образовании соответственных, напр. хлористых соединений, даже их физические свойства в виде простых или сложных тел сходного состава и т.п., можно подметить периодическую последовательность в зависимости от величины атомного веса. Для того, чтобы это выяснить, приведем сперва простой список всех, хорошо ныне известных определений атомного веса элементов, руководясь недавним сводом, сделанным F.W. Clarke («Smithsonian Miscellaneous Collections», 1075: «A recalculation of the atomic weights», Вашингтон, 1897, стр. 34), так как его ныне должно считать наиболее достоверным и содержащим все лучшие и новейшие определения. При этом примем, вместе с большинством химиков, условно атомный вес кислорода равным 16. Подробное исследование «вероятных» погрешностей показывает, что примерно для половины приведенных результатов погрешность чисел менее 0,1%, но для остальных она доходит до нескольких десятых, а для иных, быть может, и до процентов. Все атомные веса приведены по порядку их величины.
Заключение
Периодическая система Дмитрия Ивановича Менделеева имела громадное значение для естествознания и всей науки в целом. Она доказала, что человек способен проникнуть в тайны молекулярной структуры материи, а впоследствии – и в строении атомов. Благодаря успехам теоретической химии была совершена целая революция в промышленности, создано огромное количество новых материалов. Была наконец найдена взаимосвязь неорганической и органической химии – и в первой и во второй были обнаружены одни и те же химические элементы.
textarchive.ru
Интересные факты о Менделееве (9 фото)
≡ 14 Март 2015 · Рубрика: Интересные факты1 марта 1869 года считается днем рождения Периодической таблицы Менделеева. Ее «отцу» было на тот момент всего 35 лет. Мы решили рассказать вам самые интересные факты Дмитрии Ивановиче.

1. Семнадцатый ребенок в семье
Дмитрий Иванович Менделеев родился 8 февраля 1834 года в Тобольске — первой столице Сибирского края. Он был последним в семье — семнадцатым ребёнком. Семья, впрочем, была не такой большой: из 17 детей восемь умерли еще в младенчестве.
Отец Дмитрия — Иван Павлович Менделеев — занимал почетную должность директора Тобольской гимназии. Он скончался, когда Дмитрию исполнилось 13 лет, поэтому содержать большую семью пришлось матери — Марии Дмитриевне, которая приложила много усилий для того, чтобы ее дети получили достойное образование. Благодаря ей Дмитрий смог поступить в Главный педагогический институт (ныне Санкт-Петербургский государственный университет).
2. Непокорный учитель
Дмитрий Менделеев имел впечатляющий педагогический опыт. Он работал старшим учителем естественных наук в Симферопольской мужской гимназии (1855 год) и Ришельевском лицее в Одессе (1855-56), а с 1857 года стал преподавать в Императорском Санкт-Петербургском университете, где проработал в общей сложности около 30 лет. Однако из-за конфликта с министром народного просвещения Иваном Деляновым Менделеев покинул университет в 1890 году. Причиной конфликта стал отказ министра принять петицию студентов. Родные и друзья вспоминают Дмитрия Ивановича как человека упорного, который не желал уступать. Так случилось и в случае с петицией. Менделеев пользовался огромным авторитетом в студенческой среде. Когда в марте 1890 года в университете начались студенческие волнения, его пригласили на одно из обсуждений и попросили подать петицию Правительству, в которой студенты изложили свои пожелания, среди которых, в частности, была свобода слова и печати. На отказ Делянова Дмитрий Иванович отреагировал кардинально. Свою последнюю лекцию, которую ученый прочитал 22 марта 1890 года, он завершил словами: “Покорнейше прошу не сопровождать моего ухода аплодисментами по множеству различных причин”.
3. «Изобретатель» водки
Существует мнение, что Дмитрий Иванович Менделеев изобрел водку. Однако этот алкогольный напиток, конечно же, существовал задолго до 1865 года, когда он защитил докторскую диссертацию на тему «Рассуждение о соединении спирта с водою». Именно эта работа породила легенду, согласно которой он «принимал участие в разработке производства водки». В своей книге «Национальная легенда: был ли Менделеев создателем русской «монопольной» водки» доктор химических наук и директор музея-архива Д.И. Менделеева при ЛГУ Дмитриев Игорь Сергеевич опровергает этот факт. В частности, он утверждает, что «диссертация была посвящена изучению удельных весов спиртоводных растворов в зависимости от концентрации последних и температуры, а самого Менделеева интересовали в первую очередь совсем другие области концентраций, выше 40% по весу».
4. О сне, которого не было
Существует мнение, что однажды во сне Менделеев увидел периодическую таблицу химических элементов, после чего он ее изобрел. Однако ученый опроверг эту легенду, ответив следующее: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово». К слову, открытие периодического закона произошло в феврале 1869 года. 17 февраля Дмитрий Менделеев, собираясь в дорогу, начертил набросок таблицы на обратной стороне неприметного письма, в котором его приглашали приехать и помочь производству. Ученый позже скажет, что тогда «невольно зародилась мысль о том, что между массой и химическими свойствами должна быть связь». Так, он написал на отдельных карточках названия всех известных элементов, их атомный вес и свойства, а потом расположил их по порядку. Поездку пришлось отложить — ученый с головой погрузился в работу, в результате которой был открыт периодический закон химических элементов. Стоит заметить, что в то время около 60 химических элементов было изучено, а свыше тридцати еще ожидали своего времени. В 1870 году Менделеев вычислил атомные массы элементов, которые в его таблице оставались «пустыми» неизученными местами. Так ученым было предсказано существование «экаалюминия» (галлий), «экабора» (скандий), «экасилиция» (германий) и других элементов.
5. Чемоданных дел мастер
Великий ученый занимался не только научной работой. В свободное время он любил изготавливать…чемоданы. Это ремесло Менделеев освоил в Симферополе, когда из-за Крымской войны была закрыта гимназия, в которой он преподавал. Сидеть без дела ученый не любил, поэтому нашел себе увлекательное занятие: стал переплетать книги и склеивать всевозможные подручные предметы, такие как рамки и столики. Особенно ему нравилось возиться с дорожными сумками. Так у Менделеева появилось интересное занятие – изготовление чемоданов, которое он довел до совершенства. Даже когда ученый ослеп в 1895 году, он продолжал клеить чемоданы на ощупь. Однажды во время очередной покупки кожи один покупатель поинтересовался у купца, кто этот человек, на что получил ответ: “Это известный, знаменитый чемоданных дел мастер Менделеев!”

Чемодан, изготовленный Менделеевым
6. Не нобелевский лауреат
Дмитрий Менделеев был выдвинут на Нобелевскую премию несколько раз, но так и не получил ее. В первый раз это случилось в 1905 году. Тогда лауреатом стал немецкий химик-органик Адольф Байер. Через год ученый был объявлен победителем премии, но Шведская королевская академия наук отменила это решение в пользу французского учёного Анри Муассана за открытие фтора. В 1907 году прозвучало предложение разделить премию с итальянским химиком Станислао Канниццаро, однако в этот раз вмешалась судьба. 2 февраля 1907 года в возрасте 72 лет Менделеев ушел из жизни. Возможно, причиной, почему ученый так и не стал обладателем долгожданной премии, являлся конфликт между Дмитрием Ивановичем и братьями Нобель. К концу 19-го века предприимчивые шведы разбогатели на бакинской нефти и стали контролировать более 13% российских месторождений. В 1886 году, когда цена на нефть резко упала, братья Нобель предложили правительству поднять налог, аргументируя это быстрым истощением месторождения. Таким образом, повышение цен в размере 15 копеек с пуда нефти обеспечивало им избавление от конкурентов. При Министерстве государственных имуществ была образована специальная комиссия, в состав которой вошел Менделеев. Ученый был противником введения налога и опроверг слух об истощении нефти, чем и разгневал Нобелей.
7. Полеты на аэростатах
Дмитрий Менделеев работал также над конструкцией летательных аппаратов, с помощью которых он планировал исследовать температуру, давление и влажность в верхних слоях атмосферы. В 1875 году он предложил проект стратостата объёмом 3600 м³. Им же был разработан проект управляемого аэростата с двигателями. В 1878 году ученый совершил полет на привязном аэростате Анри Жиффара на Всемирной выставке в Париже. Через 9 лет он опять поднялся в воздух. В этот раз местом для эксперимента был выбран пустырь на северо-западе города Клин. 7 августа 1887 года на предоставленном Военным министерством воздушном шаре «Русский» (объём 700 м³) Менделеев в одиночку поднялся на высоту более 3000 метров. Полет продолжался три часа. За это время ученый измерил давление и температуру, а также стал свидетелем полного солнечного затмения. Этот полет был отмечен медалью французской Академии аэростатической метеорологии.

8. Пионер ледоколостроения
Интересно, что из всего количества трудов ученый посвятил химии около 10 %. Кроме всего прочего, Менделеев уделял внимание кораблестроению и освоению арктического мореплавания, о чем написал около 40 работ. Он принимал непосредственное участие в проекте строительства первого в мире арктического ледокола «Ермак», который был впервые спущен на воду 29 октября 1898 года. За большой вклад в освоение Арктики именем ученого был назван подводный хребет в Северном Ледовитом океане, открытый в 1949 году.

9. Тесть Блока
Менделеев говорил, что «много испытал в жизни, но не знает ничего лучше детей». Знающие его люди рассказывали, что он часто угощал сладостями детей сторожей в Палате мер и весов, где он работал, а также устраивал для них новогоднюю елку за свой счет. Дмитрий Иванович был отцом шестерых детей: двое родились от первого брака с Феозвой Лещёвой, четверо – от второго брака с Анной Поповой.
Старший сын Владимир был морским офицером. Ему посчастливилось плавать на фрегате «Память Азова», на котором Николай II должен был отправиться в путешествие на Дальний Восток. После свадьбы с дочерью художника-передвижника Варварой Кирилловной Лемох он скоропостижно умер. О старшей дочери Ольге известно, что она разводила породистых охотничьих собак, а после революции была вынуждена переехать в Москву, где по протекции Дзержинского работала консультантом питомника служебных собак. Ее младшая сестра Мария Дмитриевна Кузьмина также занималась собаками, однако после войны стала заведовать музеем своего отца при Ленинградском государственном университете. Интересно сложилась судьба дочери Любы. Она работала артисткой в труппе Мейерхольда и вышла замуж за Александра Блока. По стопам отца пошел Иван, который работал в институте метрологии. А вот судьба младшего сына Василия сложилась весьма загадочно. Он учился на кораблестроительном отделении Кронштадтского морского инженерного училища, но так и не закончил учебу. Говорят, что Василий пошел против родительской воли, женившись на простонародной Фене, после чего ушел из дома. О нем долго ничего не было слышно, но позже выяснилось, что он умер в 1922 году в Краснодаре, заразившись от жены брюшным тифом.

Н. А. Ярошенко. Д. И. Менделеев. 1886. Масло.



vizitron.ru

 Мария Дмитриевна Менделеева (урождённая Корнильева), мать Д. И. Менделеева
Мария Дмитриевна Менделеева (урождённая Корнильева), мать Д. И. Менделеева Иван Павлович Менделеев — отец Д. И. Менделеева.
Иван Павлович Менделеев — отец Д. И. Менделеева.