Японские ученые разработали новую таблицу элементов — Российская газета
Сообщение о создании учеными Киотского университета новой периодической системы химических элементов сразу облетело мировые СМИ. Что и понятно. Ведь когда-то таблица Менделеева стала одним из величайших открытий в химии. Она внесла удивительный порядок в, казалось бы, хаотическое нагромождение разнообразных элементов. Наш великий соотечественник расположил элементы так, чтобы соседи по столбцу имели схожие химические свойства.
Что же нового придумали японцы? Здесь важно подчеркнуть, что, создавая свою таблицу, Менделеев ничего не знал ни о строении атома, ни о его ядре, ни о том, что электроны расположены на оболочках. А самое главное, что в одном столбце его таблицы находятся элементы с одним и тем же числом электронов на последней электронной оболочке. Все это было открыто через много лет. Можно сказать, что Менделеев совершил свое открытие не только во сне, но с завязанными глазами. И очередной раз можно только поразиться его предвидению.
У японцев ситуация принципиально иная. У них глаза широко раскрыты. Их таблица создана на основе уже имеющихся знаний о ядре атомов, состоящих из протонов и нейтронов. Еще в 1963 году была присуждена Нобелевская премия за модель, согласно которой протоны и нейтроны в ядре тоже расположены на оболочках. Ядро, у которого последняя протонная нейтронная оболочка полностью заполнена, особенно устойчиво, не вступает в ядерные реакции. Но практически не вступают в химические реакции и инертные газы, у которых полностью заполнена последняя электронная оболочка.
Аналогия очевидна. Именно на ней японские ученые и построили свою периодическую таблицу, взяв за основу не электронные, а протонные оболочки атомных ядер. И подход очевиден: надо «плясать от печки» — от ядер с полностью заполненными протонными оболочками. Это гелий, кислород, кальций, никель, олово, свинец и флеровий. Число протонов в их ядрах составляет 2, 8, 20, 28, 50, 82 и 114, соответственно. Эти числа называют магическими за ту особую устойчивость, которую они придают ядрам.
Именно эти элементы японские ученые расположили в одном столбце, аналогичном столбцу инертных газов в таблице Менделеева. На основе такого столбца они и создали свою таблицу, расположив в строках элементы слева направо по мере заполнения оболочек.
Великий Менделеев создал свою таблицу, когда наука вообще не имела никакого представления ни о строении атома, ни об электронах
Исследователи надеются, что предложенный ими альтернативный способ представления химических элементов даст возможность другим ученым по-новому взглянуть на уже известные химические и физические закономерности и приведет к новым открытиям.
Описание новой таблицы японские ученые опубликовали в журнале Foundations of Chemistry.
Комментарий
Алексей Хохлов, академик РАН:
Некоторые СМИ уже сравнивают эту таблицу с той, что была создана великим Менделеевым. Говорят,что она может привести к новым открытиям.
Алексей Хохлов: Подобные заявления могут делать только те, кто плохо в школе учил химию.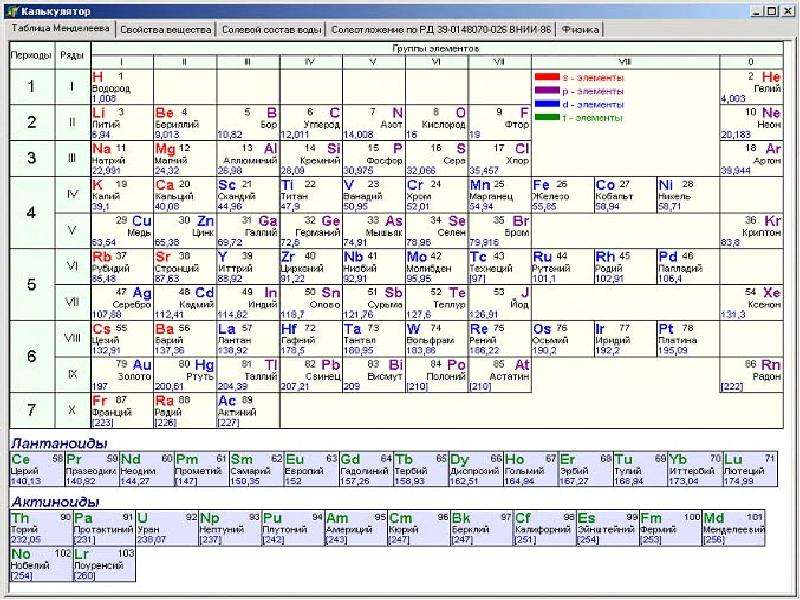 Таблица Менделеева связана не с ядром атома, а с электронами. Они определяют практически все химические связи и химические закономерности. Японские ученые проиллюстрировали некоторые уже известные факты, связанные со строением атомного ядра. Но особенности строения ядра на химические свойства почти не влияют, это не та епархия. Разве что имеют отношение к радиоактивному распаду.
Таблица Менделеева связана не с ядром атома, а с электронами. Они определяют практически все химические связи и химические закономерности. Японские ученые проиллюстрировали некоторые уже известные факты, связанные со строением атомного ядра. Но особенности строения ядра на химические свойства почти не влияют, это не та епархия. Разве что имеют отношение к радиоактивному распаду.
Если для химиков эта работа не имеет значения, может, для физиков она станет откровением, даже стимулирует на озарения?
Алексей Хохлов: Вряд ли. Ведь структура атомного ядра давно известна, известны различные ядерные модели, авторам которых присуждена Нобелевская премия. А тем, кто сравнивает эту работу японских ученых и Дмитрия Ивановича Менделеева, хочу напомнить, что он создал свою таблицу, когда наука вообще не имела никакого представления ни о строении атома, ни об электронах. Только через 50 с лишним лет появилась квантовая механика, которая все это объяснила, в том числе строение атома и электронных оболочек.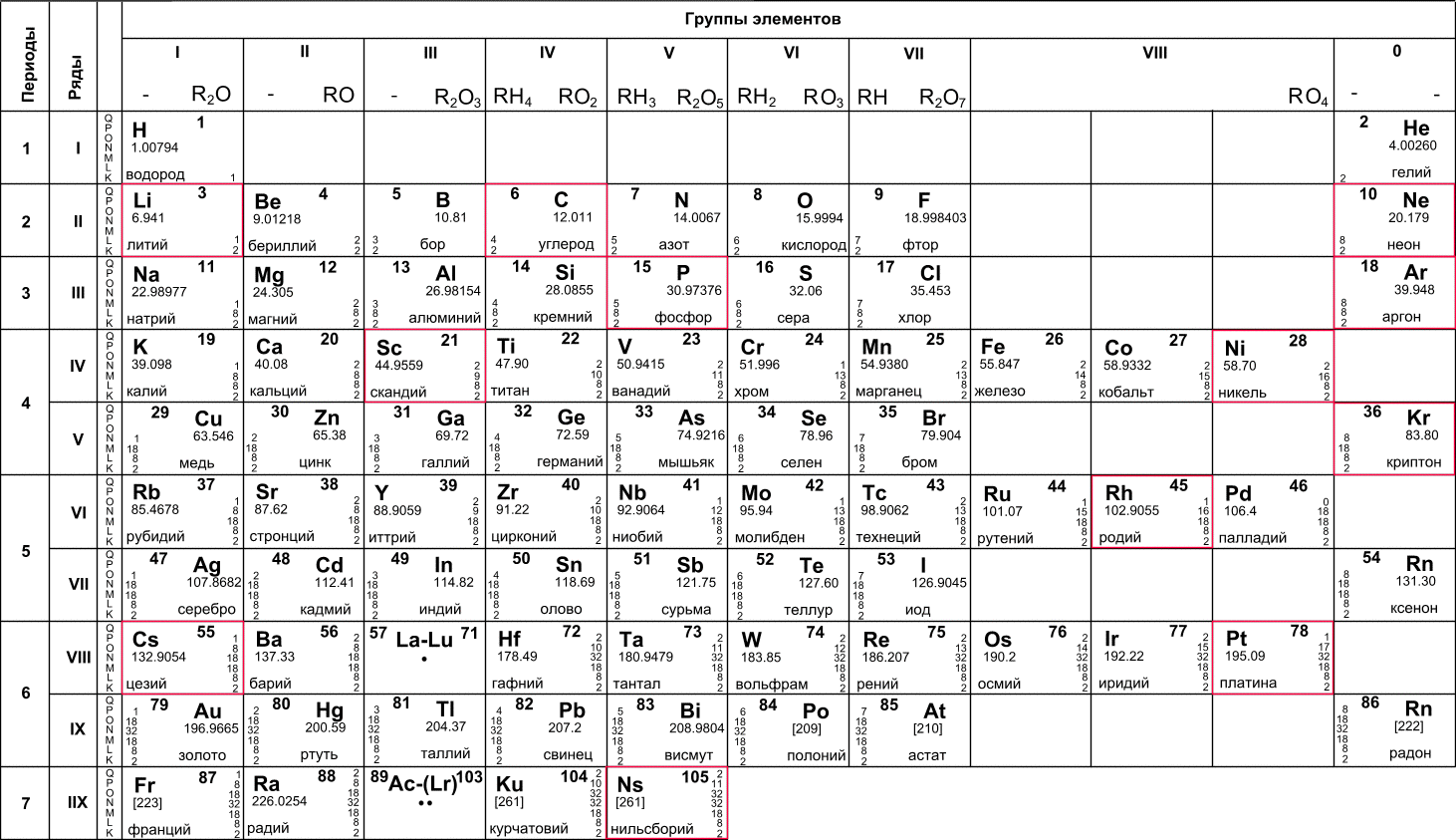 Периодический закон следует из квантовой физики. Так что если бы в то время таблицы Менделеева не было, то она могла бы быть предложена просто как следствие фундаментальных квантовых законов.
Периодический закон следует из квантовой физики. Так что если бы в то время таблицы Менделеева не было, то она могла бы быть предложена просто как следствие фундаментальных квантовых законов.
Именно это сейчас произошло с таблицей японских ученых. Если есть желание и время, можно ее использовать в педагогических целях, но ничего нового вы не узнаете. Так что эту таблицу элементов можно назвать изящной игрушкой. Но, повторяю, для обучения студентов она может быть вполне полезна.
что это такое и как ей пользоваться
Как пользоваться таблицей Менделеева? Для непосвященного человека читать таблицу Менделеева – всё равно, что для гнома смотреть на древние руны эльфов. А таблица Менделеева может рассказать о мире очень многое.
Помимо того, что сослужит вам службу на экзамене, она еще и просто незаменима при решении огромного количества химических и физических задач. Но как ее читать? К счастью, сегодня этому искусству может научиться каждый. В этой статье расскажем, как понять таблицу Менделеева.
В этой статье расскажем, как понять таблицу Менделеева.
Периодическая система химических элементов (таблица Менделеева) – это классификация химических элементов, которая устанавливает зависимость различных свойств элементов от заряда атомного ядра.
История создания Таблицы
Дмитрий Иванович Менделеев был не простым химиком, если кто-то так думает. Это был химик, физик, геолог, метролог, эколог, экономист, нефтяник, воздухоплаватель, приборостроитель и педагог. За свою жизнь ученый успел провести фундаментально много исследований в самых разных областях знаний. Например, широко распространено мнение, что именно Менделеев вычислил идеальную крепость водки – 40 градусов.
Не знаем, как Менделеев относился к водке, но точно известно, что его диссертация на тему «Рассуждение о соединении спирта с водой» не имела к водке никакого отношения и рассматривала концентрации спирта от 70 градусов. При всех заслугах ученого, открытие периодического закона химических элементов – одного их фундаментальных законов природы, принесло ему самую широкую известность.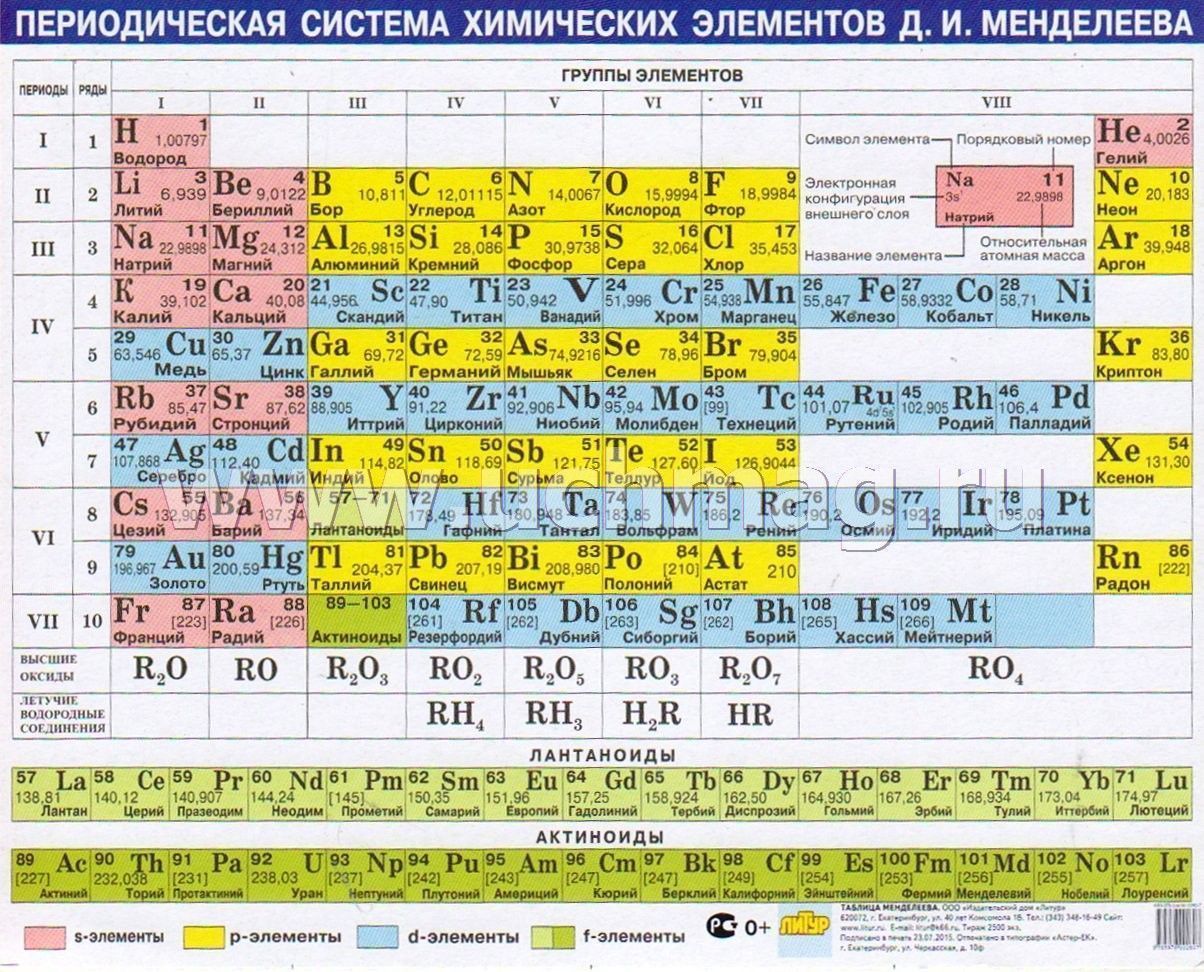
Существует легенда, согласно которой периодическая система приснилась ученому, после чего ему осталось лишь доработать явившуюся идею. Но, если бы все было так просто.. Данная версия о создании таблицы Менделеева, по-видимому, не более чем легенда. На вопрос о том, как была открыта таблица, сам Дмитрий Иванович отвечал: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово»
В середине девятнадцатого века попытки упорядочить известные химические элементы (известно было 63 элемента) параллельно предпринимались несколькими учеными. Например, в 1862 году Александр Эмиль Шанкуртуа разместил элементы вдоль винтовой линии и отметил циклическое повторение химических свойств.
Химик и музыкант Джон Александр Ньюлендс предложил свой вариант периодической таблицы в 1866 году. Интересен тот факт, что в расположении элементов ученый пытался обнаружить некую мистическую музыкальную гармонию. В числе прочих попыток была и попытка Менделеева, которая увенчалась успехом.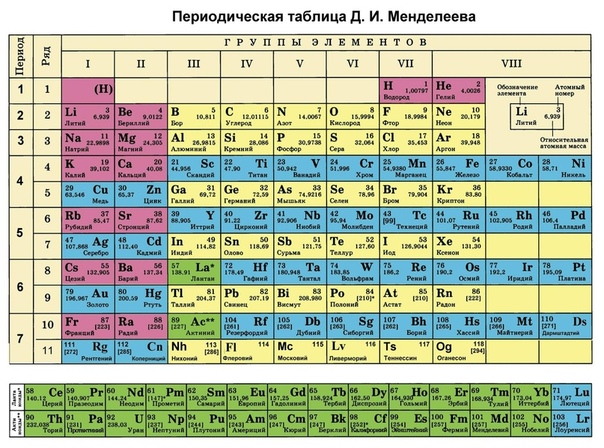
В 1869 году была опубликована первая схема таблицы, а день 1 марта 1869 года считается днем открытия периодического закона. Суть открытия Менделеева состояла в том, что свойства элементов с ростом атомной массы изменяются не монотонно, а периодически.
Первый вариант таблицы содержал всего 63 элемента, но Менделеев предпринял ряд очень нестандартных решений. Так, он догадался оставлять в таблице место для еще неоткрытых элементов, а также изменил атомные массы некоторых элементов. Принципиальная правильность закона, выведенного Менделеевым, подтвердилась очень скоро, после открытия галлия, скандия и германия, существование которых было предсказано ученым.
Современный вид таблицы Менделеева
Ниже приведем саму таблицу
Сегодня для упорядочения элементов вместо атомного веса (атомной массы) используется понятие атомного числа (числа протонов в ядре). В таблице содержится 120 элементов, которые расположены слева направо в порядке возрастания атомного числа (числа протонов)
Столбцы таблицы представляют собой так называемые группы, а строки – периоды. В таблице 18 групп и 8 периодов.
В таблице 18 групп и 8 периодов.
- Металлические свойства элементов при движении вдоль периода слева направо уменьшаются, а в обратном направлении – увеличиваются.
- Размеры атомов при перемещении слева направо вдоль периодов уменьшаются.
- При движении сверху вниз по группе увеличиваются восстановительные металлические свойства.
- Окислительные и неметаллические свойства при движении вдоль периода слева направо увеличиваются.
Что мы узнаем об элементе по таблице? Для примера, возьмем третий элемент в таблице – литий, и рассмотрим его подробно.
Первым делом мы видим сам символ элемента и его название под ним. В верхнем левом углу находится атомный номер элемента, в порядке которого элемент расположен в таблице. Атомный номер, как уже было сказано, равен числу протонов в ядре. Число положительных протонов, как правило, равно числу отрицательных электронов в атоме (за исключением изотопов).
Атомная масса указана под атомным числом (в данном варианте таблицы).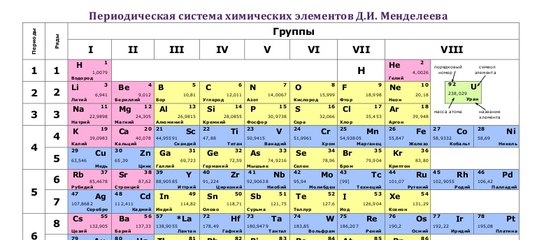
Вот и закончился наш курс «Таблица Менделеева для чайников». В завершение, предлагаем вам посмотреть тематическое видео, и надеемся, что вопрос о том, как пользоваться периодической таблицей Менделеева, стал вам более понятен. Напоминаем, что изучать новый предмет всегда эффективнее не одному, а при помощи опытного наставника. Именно поэтому, никогда не стоит забывать о студенческом сервисе, который с радостью поделится с вами своими знаниями и опытом.
Истории, скрытые в периодической таблице
Краткое введение
Прошлый, 2019 год, войдет в историю науки, как объявленный ООН и ЮНЕСКО Международный Год Периодической Таблицы (IYPT2019).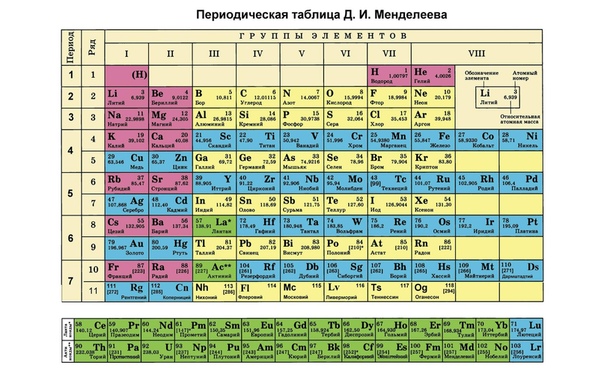 С тех дальних пор, когда 35-летний профессор по кафедре химии Санкт-Петербургского университета Д. И. Менделеев сдал свою рукопись «Опыт системы элементов, основанной на их атомном весе и химическом сходстве» в набор (1 марта 1869 г.) прошло 150 лет. По сути, это был первый вариант Периодической таблицы элементов. Окончательная формулировка Периодического закона, фундаментального закона природы, была дана им в июле 1871 г.
С тех дальних пор, когда 35-летний профессор по кафедре химии Санкт-Петербургского университета Д. И. Менделеев сдал свою рукопись «Опыт системы элементов, основанной на их атомном весе и химическом сходстве» в набор (1 марта 1869 г.) прошло 150 лет. По сути, это был первый вариант Периодической таблицы элементов. Окончательная формулировка Периодического закона, фундаментального закона природы, была дана им в июле 1871 г.
IYPT2019
Начав свое открытие 29 января, церемонией в ЮНЕСКО и закончив его 5 декабря в Токио, юбилейный Год был встречен повсюду с невероятным энтузиастом не только научным миром, но и широкой общественностью («Периодическая Таблица через 150 лет»). Всплеск интересных работ в области ядерной физики, химии, атомной физики, астрофизики, истории науки — все посвященные 150-летию открытия Периодической Таблицы; научные съезды, конференции, симпозиумы, собрания научных обществ, Академий Наук разных стран, везде по-разному, но всегда одухотворенно и очень интересно.
NEW YORKER
В этом потоке информации, 27 декабря 2019 на сайте журнала NEW YORKER появилась статья журналиста Нейма Джахроми (Neima Jahromi) с названием:
«Истории, скрытые в периодической таблице»
Здесь следовало бы сказать, что еженедельник NEW YORKER один из старейших (основан 95 лет тому назад), несколько старомодный по нынешним понятиям, но очень популярный журнал в Нью-Йорке и во всех США. В нем работают прекрасные иллюстраторы (поверьте мне) и талантливые журналисты (оцените сами). Журнал публикует все, что актуально прямо сейчас (на этой неделе) для жителя Нью-Йорка, знает и чувствует своих читателей, преподносит свой материал так, чтобы он был для них понятным и привлекательным.
Пояснения нашему читателю
Оригинальную cтатью Нейма Джахроми в журнале NEW YORKER можно найти на сайте:
Ознакомиться со статьей на сайте журнала NewYorker
Мне показалось, однако, что она не проста в чтении на английском, и я попытался ее сначала перевести на русский, а потом получить впечатление о ее содержании. В моем переводе, как и в любом, к тому же не профессиональном, статья, конечно, что-то теряет. Некоторые ситуации, описанные в «историях», и мне неясны. В каких-то случаях я догадался, о чем хотел рассказать автор и дал пояснение.
Впрочем, судите сами.
Юрий Оганесян
NEW YORKER
ИСТОРИИ, СКРЫТЫЕ В ПЕРИОДИЧЕСКОЙ ТАБЛИЦЕ
От отравленных монахов и ядерных бомб до «трансфермиевых войн».
Картография атомного мира было нелегкой.
Нейма Джахроми
27 декабря 2019 г.
Иллюстрация Ильи Милштейна / Illustration by Ilya Milstein
Поскольку искатели элементов стали создателями элементов, сам смысл таблицы Менделеева изменился. Теперь он описывает, что возможно, в дополнение к тому, что просто существует.
История пятнадцатого элемента началась в Гамбурге в 1669 году. Стеклодув-неудачник, алхимик Хенниг Брандт, пытался найти философский камень, мифическое вещество, которое могло бы превратить основные металлы в золото. Вместо этого он выделил что-то новое. Это «что-то» было пенистым и, в зависимости от используемого препарата, желтого или черного цвета. Брандт назвал его «холодным огнем», потому что он светился в темноте. Окружающие смотрели с большим интересом; некоторые чувствовали, что они присутствуют при каком-то чуде. «Если бы кто-то потер себя этим, — заметил один из наблюдателей, — вся его фигура сияла бы, как когда-то Моисей, когда он спустился с горы Синай». Роберт Бойл, отец современной химии, положил немного этого вещества на свою руку и отметил, насколько «мягким и невинным» оно казалось. Другой ученый видел частицы в нем, мерцающие «как маленькие звезды».
Брандт назвал его «холодным огнем», потому что он светился в темноте. Окружающие смотрели с большим интересом; некоторые чувствовали, что они присутствуют при каком-то чуде. «Если бы кто-то потер себя этим, — заметил один из наблюдателей, — вся его фигура сияла бы, как когда-то Моисей, когда он спустился с горы Синай». Роберт Бойл, отец современной химии, положил немного этого вещества на свою руку и отметил, насколько «мягким и невинным» оно казалось. Другой ученый видел частицы в нем, мерцающие «как маленькие звезды».
Сначала никто не мог понять, что похитил Прометей Гамбургский. После того, как один из доверенных Брандту лиц подсказал ему, что основным ингредиентом было «что-то, что принадлежало человеческому телу», — Бойл пришел к выводу, что он и его собратья смазывали себя обработанной мочой. Как объясняет кембриджский химик Питер Уотерс (Peter Wothers) в своей новой истории об элементах «Сурьма, золото и Волк Юпитера» (издательство – Оксфорд-пресс), рецепт Брандта требовал тонны мочи. Ее оставляли в ведрах достаточно долго, чтобы привлечь личинок, затем перегоняли в горячих печах, собирая сто двадцать граммов «холодного огня». Брандт полагал, что, если он сможет собрать достаточное количество этого вещества, то сможет создать философский камень.
Ее оставляли в ведрах достаточно долго, чтобы привлечь личинок, затем перегоняли в горячих печах, собирая сто двадцать граммов «холодного огня». Брандт полагал, что, если он сможет собрать достаточное количество этого вещества, то сможет создать философский камень.
В 1678 году герцог Саксонский просил его собрать сто тонн мочи гарнизона солдат и перевести ее в то, что Бойл и другие вскоре стали называть фосфором — по-латыни «носитель-света».
Мыльный фосфор, который приготовил Брандт, был любопытным материалом. Но в Англии Бойль начал производить его в более чистой, более твердой форме, которая оказалась легко воспламеняемой. Другой ученый, играющий с фосфором Бойля, обнаружил, что «под действием Тайных Сил, он будет воспламеняться и некоторое время гореть». Бойл, со своей стороны, задавался вопросом, можно ли использовать его как стартер для пороха, (его помощник, аптекарь Амброуз Годфри, подпалил голову и прожег «две или три большие дыры в своих штанах», исследуя это вещество.![]() ) Фосфорная промышленность в восемнадцатом веке быстро развивалась, отчасти благодаря тому, что врачи ошибочно полагали, что фосфор лекарственная ценность. Вместе с тем, тысяча восемьсот производителей спичек обнаружили, что деревянные палочки с фосфором были менее опасны, чем их предшественники с серным покрытием. Вскоре, открытия того, что электрические печи могут извлекать фосфор из руды в больших масштабах, привело к разработке взрывчатых веществ. Во время Второй мировой войны, по выражению Уотерса «трагического поворота судьбы», Гамбург, родной город Брандта, был разрушен бомбардировщиками союзников, сбрасывавшими фосфорные боеприпасы.
) Фосфорная промышленность в восемнадцатом веке быстро развивалась, отчасти благодаря тому, что врачи ошибочно полагали, что фосфор лекарственная ценность. Вместе с тем, тысяча восемьсот производителей спичек обнаружили, что деревянные палочки с фосфором были менее опасны, чем их предшественники с серным покрытием. Вскоре, открытия того, что электрические печи могут извлекать фосфор из руды в больших масштабах, привело к разработке взрывчатых веществ. Во время Второй мировой войны, по выражению Уотерса «трагического поворота судьбы», Гамбург, родной город Брандта, был разрушен бомбардировщиками союзников, сбрасывавшими фосфорные боеприпасы.
Уотерс находит много таких поворотов в историях, скрытых за квадратиками Периодической таблицы. Сурьма (элемент № 51) — блестящий минерал; четыре тысячи лет назад люди вырезали из него вазы, они появляются в украшениях, описанных в Ветхом Завете. Согласно отчету, представленному аптекарем и алхимиком XVII века Пьером Пометом (возможно, сомнительному, по мнению Уотерса) сурьма получила свое название от истории немецкого монаха, который скармливал ею своих собратьев. Монах давал сурьму нескольким свиньям, которых сначала рвало, но потом они выздоравливали и толстели. К сожалению, каждый принявший сурьму монах умер. «Именно по этой причине минерал был назван Сурьмой, — писал Помет, — как истребитель Монахов». (В менее фатальных эпизодах, доктор XIX века и его друзья потребляли по пятнадцать миллиграммов теллура каждый: они выдыхали чесночным запахом в течение восьми месяцев).
Монах давал сурьму нескольким свиньям, которых сначала рвало, но потом они выздоравливали и толстели. К сожалению, каждый принявший сурьму монах умер. «Именно по этой причине минерал был назван Сурьмой, — писал Помет, — как истребитель Монахов». (В менее фатальных эпизодах, доктор XIX века и его друзья потребляли по пятнадцать миллиграммов теллура каждый: они выдыхали чесночным запахом в течение восьми месяцев).
Названия элементов уже давно являются источником раздоров и непонимания. Водород, как указывает Уотерс, в переводе с греческого означает «образующий воду», а кислород в переводе с греческого означает «образующий кислоту»; на самом деле, водород, который связывается вместе с другими элементами, образует кислоты, а кислород, который связывает водород, образует воду. «Алюминий», — писал Чарльз Диккенс в 1856 году, — «окаменелая часть латинской речи, примерно столь же подходящая для людских уст, как котлета ихтиозавров или костный мозг динорниса». (В латыни корень такой же как «горькая соль», из которой был извлечен некогда драгоценный металл; предложения Диккенса — «суглинок-серебро» и «глеб-золото» — не намного лучше). Французский химик Маргарита Перей, протеже Марии Кюри, открыла свой собственный элемент в 1939 году. Она хотела назвать его «катиум», чтобы отметить сильное притяжение частицы к катодам, устройствам, используемым для передачи электричества через химическое вещество. А дочь Марии Кюри, Ирен Жолио-Кюри, была обеспокоена тем, что носители английского языка ассоциируют этот элемент с домашними кошками. Перей, будучи француженкой, решила вместо этого назвать его францием.
Французский химик Маргарита Перей, протеже Марии Кюри, открыла свой собственный элемент в 1939 году. Она хотела назвать его «катиум», чтобы отметить сильное притяжение частицы к катодам, устройствам, используемым для передачи электричества через химическое вещество. А дочь Марии Кюри, Ирен Жолио-Кюри, была обеспокоена тем, что носители английского языка ассоциируют этот элемент с домашними кошками. Перей, будучи француженкой, решила вместо этого назвать его францием.
Многие историки датируют изобретение периодической таблицы публикацией сто пятьдесят лет тому назад учебника русского химика Дмитрия И. Менделеева. Но автор книги «Периодическая Таблицы: ее история и ее значение» (Оксфорд-пресс) философ химии Калифорнийского университета в Лос-Анжелесе, Эрик Шерри (Eric Scerri) который изучает историю таких вопросов, как «Что такое элемент, на самом деле?» считает, что Менделеев произвел революцию в науке, когда привел химическую периодичность в ясную форму.
Периодичность – идея о том, что более крупные атомы чередуются с меньшими атомами в определенном порядке, как ноты на клавиатуре. Что периодичность не возникла как гром среди ясного неба, утверждает Шерри. Это стало предметом внимания благодаря работе множества ученых; при этом идеи, которые к тому времени были, долгое время забыты, такие как алхимия, оказались в некоторых отношениях правильными, а по существу неправильные идеи, такие как несовместимость элементов, оказались все-таки полезными для размышлений. Некоторые из химиков восемнадцатого и девятнадцатого веков, которые начали замечать закономерности среди определенных элементов, фактически прослеживали пути древнегреческих атомщиков, таких как Демокрит и Левкипп, которые в пятом веке до нашей эры утверждали, что невидимые и неделимые частицы составляют все, что мы можем видеть и трогать. Атомисты полагали, что эти частицы были несметным числом по форме и размеру, и что их ощутимые свойства проистекали из структур, которые они образовывали, когда они соединялись вместе.
Что периодичность не возникла как гром среди ясного неба, утверждает Шерри. Это стало предметом внимания благодаря работе множества ученых; при этом идеи, которые к тому времени были, долгое время забыты, такие как алхимия, оказались в некоторых отношениях правильными, а по существу неправильные идеи, такие как несовместимость элементов, оказались все-таки полезными для размышлений. Некоторые из химиков восемнадцатого и девятнадцатого веков, которые начали замечать закономерности среди определенных элементов, фактически прослеживали пути древнегреческих атомщиков, таких как Демокрит и Левкипп, которые в пятом веке до нашей эры утверждали, что невидимые и неделимые частицы составляют все, что мы можем видеть и трогать. Атомисты полагали, что эти частицы были несметным числом по форме и размеру, и что их ощутимые свойства проистекали из структур, которые они образовывали, когда они соединялись вместе.
В средние века атомистические идеи в основном затмевались теорией Аристотеля о том, что четыре основных элемента — огонь, земля, вода и воздух — объединяются, образуя различные объекты во Вселенной. Но атомизм никогда не исчезал полностью. Ученые эпохи Возрождения верили во множество элементарных схем. Книга Уотерса перепечатывает некоторые диаграммы до периодической таблицы, как смесь этих идей. Гравюра семнадцатого века «семи металлов» изображает семь римских богов, размахивающих древними химическими символами (божества напомнили зрителям, что железо было с Марса, а медь с Венеры) другой показывает семь металлов и четыре элемента Аристотеля в треугольном расположении. На всей схеме изображен латинский девиз: «Хотя я невидимка, тем не менее, я отец и мать всех видимых земных тел».
Но атомизм никогда не исчезал полностью. Ученые эпохи Возрождения верили во множество элементарных схем. Книга Уотерса перепечатывает некоторые диаграммы до периодической таблицы, как смесь этих идей. Гравюра семнадцатого века «семи металлов» изображает семь римских богов, размахивающих древними химическими символами (божества напомнили зрителям, что железо было с Марса, а медь с Венеры) другой показывает семь металлов и четыре элемента Аристотеля в треугольном расположении. На всей схеме изображен латинский девиз: «Хотя я невидимка, тем не менее, я отец и мать всех видимых земных тел».
Конечно, вам не нужно быть ученым, чтобы верить в мир, состоящий из более чем четырех элементов. Шахтеры семнадцатого века, пишет Уотерс, различают разные виды воздуха: они называли более легкий воздух, который кружился наверху пещер, «влажным от огня», потому что он легко загорался, и тяжелые облака, нависавшие у земли «удушье», потому что им было трудно дышать. В восемнадцатом веке местные жители окрестили пещеру возле Неаполя, как Грот-дель-Кане: собаки, которые забредали в пещеру, не в силах были поднять головы над газом, просачивающимся из Земли. Они вскоре начинали задыхаться; однако, вернувшись на открытый воздух, животные оживали.
Они вскоре начинали задыхаться; однако, вернувшись на открытый воздух, животные оживали.
По мере распространения этих наблюдений росло и убеждение в том, что должно быть много разных элементов. К концу восемнадцатого века ученые, комбинируя вещества, начали понимать, что определенные материалы всегда реагировали в одинаковых пропорциях, что указывало на то, что они имели в основе разные массы. (Казалось, что для нейтрализации того же количества серной кислоты аммиаком всегда требовалось немного больше аммиака, чем магния) В 1803 году английский ученый Джон Дальтон предположил, что в таких реакциях работают атомы; он призвал своих сотрудников помочь ему определить, сколько весят эти невидимые существа. Началось то, что Шерри называет «увлечением поиска численных закономерностей». Вскоре химики заметили закономерности, когда сгруппировали элементы в наборы по три атомных веса. (Литий, натрий и калий, например, все шипят или взрываются в воде; оказалось, что атомный вес натрия является средним от лития и калия. ) Такие эксперименты показали проблески порядка в элементарной Вселенной. Но работа была разочаровывающей. В 1836 году химик Жан Батист Андре Дюма, ученик Дальтона, в отчаянии вскинул руки.
«Что осталось от амбициозной экскурсии, когда мы позволили себе войти в область атомов?» — писал он. «Если бы я был мастером, я бы вычеркнул слово «атом» из науки».
) Такие эксперименты показали проблески порядка в элементарной Вселенной. Но работа была разочаровывающей. В 1836 году химик Жан Батист Андре Дюма, ученик Дальтона, в отчаянии вскинул руки.
«Что осталось от амбициозной экскурсии, когда мы позволили себе войти в область атомов?» — писал он. «Если бы я был мастером, я бы вычеркнул слово «атом» из науки».
Другие химики, наоборот, настаивали. По мере того, как атомные веса становились все более точными, появлялись новые закономерности. В 1864 году немецкий химик Юлиус Лотар Мейер опубликовал таблицу из двадцати восьми элементов. Элементы Мейера, расположенные, в основном, в порядке увеличения веса, также были выстроены в соответствии с их общими химическими свойствами, которые повторялись через равные интервалы. Пять лет спустя Менделеев опубликовал свою собственную периодическую таблицу, которая постоянно развивалась в версию, которую мы используем сегодня. Подобно Мейеру, Менделеев поместил свои частицы в грубую сетку, в ряды которой входили элементы со схожими свойствами. Но он также украсил свою таблицу многими заманчивыми вопросительными знаками и пустыми местами и сделал явные элементарные пророчества. Менделеев точно предсказал существование тогда еще не открытых элементов, таких как галлий и германий, и предсказал их взаимодействие с другими элементами.
Но он также украсил свою таблицу многими заманчивыми вопросительными знаками и пустыми местами и сделал явные элементарные пророчества. Менделеев точно предсказал существование тогда еще не открытых элементов, таких как галлий и германий, и предсказал их взаимодействие с другими элементами.
Предсказания Менделеева были неверны столь же часто, как и были правильными. Но, объясняет Шерри, русский химик был главным толкователем и, по сравнению с Мейером и другими конкурентами, более эффективным евангелистом для периодической системы. Менделеев пользовался любой возможностью, чтобы время от времени настойчиво утверждать, что характеристики элементов повторяются упорядоченным и предсказуемым образом. Он был неутомим и негибок, по крайней мере, до тех пор, пока волна научного мнения не повернулась против него. В конце пятидесятых годов девятнадцатого века ученые обнаружили, что элементный состав данного вещества может быть определен из света, который он испускает, когда горит. В 1868 году французский астроном Жюль Янссен использовал эту технику для обнаружения гелия (элемент № 2) на поверхности Солнца во время полного солнечного затмения. Сначала Менделеев утверждал, что гелий не может существовать; это не находило места в периодической таблице. Но на рубеже двадцатого века, после того, как были обнаружены другие благородные газы и они продемонстрировали свойства схожие с гелием, и другие ученые создали колонку именно для них, Менделеев встал в очередь. (Колонна проходит по правой стороне, гелий выскакивает сверху).
Сначала Менделеев утверждал, что гелий не может существовать; это не находило места в периодической таблице. Но на рубеже двадцатого века, после того, как были обнаружены другие благородные газы и они продемонстрировали свойства схожие с гелием, и другие ученые создали колонку именно для них, Менделеев встал в очередь. (Колонна проходит по правой стороне, гелий выскакивает сверху).
Способность Таблицы к адаптации помогла ей выстоять. В двадцатом веке ученые поняли, что периодичность не определяется атомным весом; вместо этого важным было число протонов, которые каждый атом содержал в своем ядре. Но это открытие не сломало Таблицу, она, после нескольких перестановок, стала точнее. За последние полтора столетия наши представления о вселенной радикально изменились. Но основной формат периодической таблицы сохранился.
Но это вовсе не означает, что никто не пытался ее пересмотреть: Шерри отмечает, что, начиная с 1860-х годов, было предложено более тысячу альтернативных периодических таблиц, часто с целью охвата других периодических моделей, оставленных вне оригинала. Они включают с 1990 года трехмерную рождественскую елку Фернандо Дюфура; с 1964 года спиральный узор Теодора Бенфея, напоминающий голову утки; скульптуру в форме кренделя XIX века Уильяма Крукса, сейчас она находится в Музее науки в Лондоне. Эта последняя модель поместила уран в его основу, предполагая, что химия никогда не столкнется с более тяжелым атомом. Но потолок элементов продолжал расти. Истории о тридцати или около того элементах, обнаруженных в прошлом столетии — некоторые из которых Менделеев и Мейер не могли себе представить, — составляют основную часть книги «Сверхтяжелые: создание и разрушение периодической таблицы» (Блумсбери-пресс) научного журналиста Кита Чапмена (Kit Chapman).
Они включают с 1990 года трехмерную рождественскую елку Фернандо Дюфура; с 1964 года спиральный узор Теодора Бенфея, напоминающий голову утки; скульптуру в форме кренделя XIX века Уильяма Крукса, сейчас она находится в Музее науки в Лондоне. Эта последняя модель поместила уран в его основу, предполагая, что химия никогда не столкнется с более тяжелым атомом. Но потолок элементов продолжал расти. Истории о тридцати или около того элементах, обнаруженных в прошлом столетии — некоторые из которых Менделеев и Мейер не могли себе представить, — составляют основную часть книги «Сверхтяжелые: создание и разрушение периодической таблицы» (Блумсбери-пресс) научного журналиста Кита Чапмена (Kit Chapman).
 Подобные события в корне изменили наши отношения к материи. Обнаружение элемента было похоже на нахождение доктора Ливингстона в Восточной Африке: вы знали, что он где-то там был. Теперь грань между открытием и созданием размыта.
Подобные события в корне изменили наши отношения к материи. Обнаружение элемента было похоже на нахождение доктора Ливингстона в Восточной Африке: вы знали, что он где-то там был. Теперь грань между открытием и созданием размыта.А элементы, созданные в лаборатории, могут не существовать больше нигде.
Современная эра охоты на элементы началась в тридцатых годах, когда физик Эрнест Лоуренс поручил ученым из Калифорнийского университета в Беркли разработать серию устройств, называемых циклотронами. Они используют электричество для вбивания протонов в мишень – фольгу, установленную внутри металлической камеры. Вскоре исследователи обнаружили, что некоторые из заряженных ядерных частиц будут попадать на атомы (лучше сказать, на атомные ядра. Ю.О) в мишенях и создавать более крупные и тяжелые элементы. Частицы были бесконечно малы, и их вероятность столкновения была незначительной. «Это похоже на стрельбу по птицам в темноте в стране, где есть только несколько птиц», — сказал Альберт Эйнштейн в 1934 году. Тем не менее, циклотроны Лоуренса позволили охотникам за элементами делать триллионы выстрелов, и к 1937 году одно из его устройств создало технеций (элемент № 43), атом, предсказанный Менделеевым. Как и все элементы, впервые родившиеся в циклотронах, технеций был радиоактивным. Лоуренс получил Нобелевскую премию за свое изобретение в 1939 году; В том же году Эйнштейн рекомендовал президенту Рузвельту начать работу над ядерным оружием.
Тем не менее, циклотроны Лоуренса позволили охотникам за элементами делать триллионы выстрелов, и к 1937 году одно из его устройств создало технеций (элемент № 43), атом, предсказанный Менделеевым. Как и все элементы, впервые родившиеся в циклотронах, технеций был радиоактивным. Лоуренс получил Нобелевскую премию за свое изобретение в 1939 году; В том же году Эйнштейн рекомендовал президенту Рузвельту начать работу над ядерным оружием.
Взрывы этих бомб еще больше заполняли периодическую таблицу. Начиная с 1952 года, Соединенные Штаты взрывали водородные бомбы около Маршалловых островов. Затем исследователи отправили летчиков-истребителей F-84, в облако взрывов. (Огненные шары, отмечает Чапмен, были столь горячими, что «имитировали сильное пекло Солнца».) Ученые оснастили концы крыльев F-84 фильтрами, способными улавливать атомы, возникшими в результате взрыва. Пробиваясь сквозь ножки грибовидных облаков, пытаясь удержать самолеты от грохота, пилоты, пишет Чапмен, собрали «элементы, обычно присутствующие только в сливающихся нейтронных звездах». (Один пилот, Джимми Робинсон, убегающий от ядерной пыльной бури, обнаружил, что его двигатели заглохли; он погиб при попытке приземления на воду.) Позже в лаборатории в Беркли химик Гленн Сиборг и его коллеги обнаружили в фильтре, извлеченном из одного из самолетов, двести атомов того, что станет элементом № 99,. Потребовались годы споров, чтобы рассекретить их открытие, но ученые Беркли публично описали этот элемент в 1954 году. Они выпили «много коктейлей» прежде чем назвать, в конце концов, свою новую частицу эйнштейниумом в честь человека, который предложил бомбу.
(Один пилот, Джимми Робинсон, убегающий от ядерной пыльной бури, обнаружил, что его двигатели заглохли; он погиб при попытке приземления на воду.) Позже в лаборатории в Беркли химик Гленн Сиборг и его коллеги обнаружили в фильтре, извлеченном из одного из самолетов, двести атомов того, что станет элементом № 99,. Потребовались годы споров, чтобы рассекретить их открытие, но ученые Беркли публично описали этот элемент в 1954 году. Они выпили «много коктейлей» прежде чем назвать, в конце концов, свою новую частицу эйнштейниумом в честь человека, который предложил бомбу.
Даже в лабораторных условиях охота на новые элементы может быть опасной. В 1959 году Ал Гиорсо, физик из Беркли с железными нервами, как известно, бил теннисные мячи, наполненные радиоактивным материалом в поисках элемента № 102 (непонятно, зачем он это делал? Ю.О.). Однажды, около обеда, он перегружал камеру гелием через фильтр во время облучения мишени из кюрия. Чапмен пишет, что фильтр набух, а потом лопнул как «воздушный шар, наполненный радиоактивным блеском». Гиорсо нырнул под облако, но здание было эвакуировано. И все-таки, несмотря на трудности, Гиорсо, возможно, не первым обнаружил этот элемент. Шведская команда, используя элементарное оборудование, утверждала, что нашла его первым; они хотели назвать это нобелием, в честь шведского изобретателя динамита.
Гиорсо нырнул под облако, но здание было эвакуировано. И все-таки, несмотря на трудности, Гиорсо, возможно, не первым обнаружил этот элемент. Шведская команда, используя элементарное оборудование, утверждала, что нашла его первым; они хотели назвать это нобелием, в честь шведского изобретателя динамита.
Между тем советские ученые поставили под сомнение результаты, полученные как из Стокгольма, так и из Беркли. Наименование элементов № 100 и № 101, фермия и менделевия, вызвало слабое волнение. Но это относительное спокойствие вскоре нарушилось. В период, который теперь называется «трансфермиевыми войнами», цикл открытий и сомнений стал лейтмотивом исследований элементов во времена холодной войны. (В конце концов, Международный союз чистой и прикладной химии признал заслуги Советов в открытии этого элемента, оставив при этом название «нобелиум»).
К 1970 году в периодической таблице было, как минимум, два основных варианта. Американцы назвали элемент № 104 в честь Эрнеста Резерфорда, отца ядерной науки; Советы назвали его в честь Игоря Курчатова, отца советского ядерного оружия.
Трансфермиевые войны продолжались, но возникла ироническая ситуация: исследователи атомщики искали стабильные (бессмертные) элементы, а обнаружили те, которые быстро исчезали. Для производства «сверхтяжелых» требовалось огромное количество энергии; но, затем, они имели тенденцию распадаться, превращаясь в более легкие элементы, часто в течение наносекунд. Ученые в Соединенных Штатах и Советском Союзе пытались выяснить, как продлить их жизнь. Экспериментируя с элементами, созданными в рамках Манхэттенского проекта, исследователи поняли, что они могут создать две разные версии или два изотопа прометия, шестьдесят первого атома в периодической таблице. Один изотоп прометия, имеющий восемьдесят восемь нейтронов, имеет период полураспада в несколько дней; другой, имеющий восемьдесят шесть нейтронов, имеет период полураспада в несколько лет. По-видимому, правильное «магическое» число нейтронов и протонов могло бы удерживать гиперзаряженное ядро сверхтяжелого элемента как целое. Исследователи начали задаваться вопросом, могут ли эти более длительные гигантские атомы встречаться в природе. Чапмен представляет эскиз 1978 года одного ученого, под названием «Карта изотопов». Он показывает «море нестабильности», в котором простирается полуостров. На конце полуострова маленькая фигура покоится в гигантской рогатке. Рогатка направлена на «Волшебный остров», охраняемый грозной птицей «ядерной вязкости» с распростертыми крыльями.
Чапмен представляет эскиз 1978 года одного ученого, под названием «Карта изотопов». Он показывает «море нестабильности», в котором простирается полуостров. На конце полуострова маленькая фигура покоится в гигантской рогатке. Рогатка направлена на «Волшебный остров», охраняемый грозной птицей «ядерной вязкости» с распростертыми крыльями.
Мечта о волшебном острове стабильных атомов, спрятанном во многих рядах периодической таблицей, положила начало тому, что Чапмен называет сверхтяжелой «золотой лихорадкой». Вместо создания сверхтяжелых элементов в ускорителях частиц исследователи начали искать их в природе. Одна теория заключалась в том, что, если бы существовали стабильные сверхтяжелые элементы, их было бы легче обнаружить дальше от поверхности Земли, которая бомбардируется радиоактивными космическими лучами, они могут создавать сильный фон чувствительным детекторам. Другая теория состояла в том, что сверхтяжелые элементы (или свидетельства их) могут быть найдены внутри материалов, изготовленных из элементов в том же периодическом столбце. Ученые путешествовали вглубь океана, копали соляные шахты, изучали золотые самородки, высылали воздушные шары для наблюдений, путешествовали пешком по туннелям метро, собирали рассол из Каспийского моря, собирали зубы акул, шестидесяти миллионов летней давности и входили в соборы для анализа витражей. (Они надеялись, что свинцовая прокладка между стеклами могла бы на этих стеклах сохранить свидетельство древней ядерной реакции спонтанного деления в виде латентных треков осколков). Но после двух десятилетий поисков в природе не было обнаружено никаких сверхтяжелых элементов. Казалось, это могут сделать только ускорители частиц и ничто другое.
Ученые путешествовали вглубь океана, копали соляные шахты, изучали золотые самородки, высылали воздушные шары для наблюдений, путешествовали пешком по туннелям метро, собирали рассол из Каспийского моря, собирали зубы акул, шестидесяти миллионов летней давности и входили в соборы для анализа витражей. (Они надеялись, что свинцовая прокладка между стеклами могла бы на этих стеклах сохранить свидетельство древней ядерной реакции спонтанного деления в виде латентных треков осколков). Но после двух десятилетий поисков в природе не было обнаружено никаких сверхтяжелых элементов. Казалось, это могут сделать только ускорители частиц и ничто другое.
В последние годы, вместо того, чтобы открыть остров стабильности, ученые, кажется, сделали нечто противоположное: они создали сверхтяжелые элементы, которые угрожают разрушить периодическую таблицу. В 1998 году российские ученые создали новый элемент, который исчез из жизни спустя чуть больше секунды. Главный русский охотник за стихиями Юрий Оганесян назвал его в честь своего покойного наставника Георгия Флерова. В 2016 году Оганесян получил свое имя на атоме другого элемента. Его элемент, который в настоящее время является последним в таблице Менделеева, был также вспышкой в машине. Чапмен считает, что такие элементы, как флеровий и оганессон (элементы № 114 и № 118 соответственно) могут означать «конец химии, какой мы ее знаем». Оганессон сидит в нижней части колонны благородных газов, но некоторые статьи от 2017 года предполагают, что он может не принадлежать им. Скорости его внутренних электронов, вероятно, приближаются настолько к скорости света, что химическое поведение элемента может отличаться от благородных газов, с которыми он сгруппирован. Вместо этого оганессон и его соседи могут следовать теории относительности; время и пространство могут оказаться искривленными внутри них, и их свойства могут последовать их примеру.
В 2016 году Оганесян получил свое имя на атоме другого элемента. Его элемент, который в настоящее время является последним в таблице Менделеева, был также вспышкой в машине. Чапмен считает, что такие элементы, как флеровий и оганессон (элементы № 114 и № 118 соответственно) могут означать «конец химии, какой мы ее знаем». Оганессон сидит в нижней части колонны благородных газов, но некоторые статьи от 2017 года предполагают, что он может не принадлежать им. Скорости его внутренних электронов, вероятно, приближаются настолько к скорости света, что химическое поведение элемента может отличаться от благородных газов, с которыми он сгруппирован. Вместо этого оганессон и его соседи могут следовать теории относительности; время и пространство могут оказаться искривленными внутри них, и их свойства могут последовать их примеру.
Шерри не верит, что периодической таблице серьезно угрожают такие элементы, как оганессон. Он указывает, что некоторые электроны в атомах золота вращаются со скоростями, которые также чувствуют, хотя и слабее, приближение к скорости света. Вполне возможно, что даже относительность соответствует шаблону — «еще одно свидетельство», пишет он, «фундаментальной природе периодического закона». («Коперниум», № 112, стоит ниже уровня золота и, похоже, также содержит релятивистский эффект) И все же Шерри утверждает, что такие элементы дестабилизируют периодическую таблицу по-другому. Первоначально предполагалось, что таблица описывает строительные блоки природы.
Вполне возможно, что даже относительность соответствует шаблону — «еще одно свидетельство», пишет он, «фундаментальной природе периодического закона». («Коперниум», № 112, стоит ниже уровня золота и, похоже, также содержит релятивистский эффект) И все же Шерри утверждает, что такие элементы дестабилизируют периодическую таблицу по-другому. Первоначально предполагалось, что таблица описывает строительные блоки природы.
Но поскольку охотники за элементами стали создателями элементов, значение таблицы изменилось. Теперь она описывает, что возможно, а также то, что просто существует.
Даже если существует остров атомной стабильности, сверхтяжелые элементы, которые живут на нем, вероятно, будут чрезвычайно редки. Атомы водорода, сгорающие в одной звезде, имеют тенденцию становиться столь тяжелыми, как железо (элемент № 26 из ста семидесяти двух или ста семидесяти трех возможных элементов, которые, по мнению некоторых ученых, могут существовать). Астрофизики полагают, что более крупные атомы, которые возникают в коллапсирующих звездах, могут, преодолев огромные расстояния в космосе, приземлиться в котлах других солнц и продолжать расти. Но Земле четыре с половиной миллиарда лет — намного больше, чем период полураспада даже самых стабильных предсказанных сверхтяжелых элементов — и здесь обнаружено мало их следов. (Поскольку сверхтяжелые элементы могут быстро распадаться, охотники за элементами исследуют метеориты, которые могли возникнуть в результате более недавних звездных взрывов.) В ближайшие несколько лет ученые-атомщики с ускорителями частиц легко создадут элементы № 119 и № 120. Они никогда не могут быть видны за пределами лаборатории.
Но Земле четыре с половиной миллиарда лет — намного больше, чем период полураспада даже самых стабильных предсказанных сверхтяжелых элементов — и здесь обнаружено мало их следов. (Поскольку сверхтяжелые элементы могут быстро распадаться, охотники за элементами исследуют метеориты, которые могли возникнуть в результате более недавних звездных взрывов.) В ближайшие несколько лет ученые-атомщики с ускорителями частиц легко создадут элементы № 119 и № 120. Они никогда не могут быть видны за пределами лаборатории.
Похоже, что в США стихийная лихорадка остыла, но в других странах она продолжает кипеть. В 2004 году Япония обнаружила свой первый элемент, нихоний № 113, и Чапмен сообщает, что японские дети читают мангу, драматизируя работу главного физика-ядерщика страны Косуке Мориты. Когда нихониум был официально добавлен в периодическую таблицу, в 2016 году наследный принц Нарухито был глубоко взволнован: На специальной церемонии он вспомнил о том, как копировал эту таблицу вручную, когда был мальчиком. Тем временем в Женеве ученые в ЦЕРНе расширили охоту на другие части космоса. «Некоторые люди считают, что могут быть разные формы темной материи», — сказал мне Ин Вун Ивонн Нг, физик элементарных частиц. «Кто знает», — сказала она. «Это может потенциально заполнить большую периодическую таблицу».
Тем временем в Женеве ученые в ЦЕРНе расширили охоту на другие части космоса. «Некоторые люди считают, что могут быть разные формы темной материи», — сказал мне Ин Вун Ивонн Нг, физик элементарных частиц. «Кто знает», — сказала она. «Это может потенциально заполнить большую периодическую таблицу».
Технеций, первый искусственный элемент, все еще используется в лечении рака во всем мире. Теоретически, более новые элементы могут быть аналогичным образом полезными: согласно Чапмену, ученые предположили, что образец флеровия размером с горошину «мог бы обеспечить город энергией», если бы его можно было стабилизировать. По правде говоря, похоже, что упорные охотники за стихиями охотятся по причинам, превосходящим даже научную славу. В своих «Сверхтяжелых» Чапмен посещает Оганесяна в его лаборатории в России, чтобы спросить его, почему он все еще охотится, особенно теперь, когда у него есть элемент, который носит его имя. «Если у вас есть способ и устройство, которые могут это сотворить, — отвечает Оганесян, — почему бы и нет? Вы строите машину, чтобы найти новые атомы; и вы можете делать атомы, потому что у вас есть такая машина. «Это как ящик Пандоры», — говорит Оганесян, поглаживая компонент циклотрона, который в настоящее время строится (уже построен и запущен Ю.О.). «Новый объект. Новый ускоритель». Находите элементы, и повесть об этом никогда не закончится.
«Это как ящик Пандоры», — говорит Оганесян, поглаживая компонент циклотрона, который в настоящее время строится (уже построен и запущен Ю.О.). «Новый объект. Новый ускоритель». Находите элементы, и повесть об этом никогда не закончится.
Школьники узнали секреты таблицы Менделеева на Всероссийском открытом уроке по химии
7 февраля прошел Всероссийский открытый урок «Менделеев? Элементарно!». Мероприятие, организованное Министерством просвещения РФ совместно с порталом «ПроеКТОриЯ», было посвящено Международному году Периодической таблицы химических элементов Д.И. Менделеева.
Во время урока ребята познакомились с человеком-легендой Юрием Оганесяном. В честь Юрия Цолаковича назван 118-ый химический элемент периодической таблицы — оганесон. Научный руководитель лаборатории ядерных реакций им. Г.Н. Флёрова Объединенного института ядерных исследований в Дубне объяснил зрителям, как получают новые элементы и отметил значимость открытия Менделеева: «Меня часто спрашивают: „Периодический закон на самом деле такой фундаментальный?“. Да! Природа создавала всё другим способом, мы это делаем в лаборатории тоже другим. Но если это атом, он должен быть сконструирован по вполне определенному закону. Именно по этому знаменитому Периодическому закону, которому сегодня исполняется 150 лет».
Да! Природа создавала всё другим способом, мы это делаем в лаборатории тоже другим. Но если это атом, он должен быть сконструирован по вполне определенному закону. Именно по этому знаменитому Периодическому закону, которому сегодня исполняется 150 лет».
Специальным гостем урока стал Григорий Трубников, первый заместитель Министра науки и высшего образования РФ. Он рассказал школьникам, кто такой — современный учёный:
«Это очень разносторонние люди: и в литературе, и в музыке, и в языках. Но самая главная черта, которая движет ученым — быть первым там, где никто никогда не был». И пригласил ребят в науку, потому что мы знаем об окружающем мире лишь 4% тайн природы.
Вице-президент Российского химического общества им. Д.И. Менделеева Юлия Горбунова рассказала школьникам, в чем уникальность таблицы Менделеева и как химия изменилась за 150 лет:
«Гениальность заключается в том, что Дмитрий Иванович не просто объединил их по сходству свойств, а ещё и предсказал появление новых элементов.
И на сегодняшний день 118 элементов располагаются по той самой структуре, которую придумал Менделеев».
Спикеры уделили внимание и самой сложной биохимической лаборатории — человеку. Степан Калмыков, декан химического факультета МГУ им. М.В.Ломоносова поделился с аудиторией «формулами» любви, рассказал, какие вещества отвечают за наши эмоции, и развеял миф о том, что хорошее образование можно получить только в столице.
«У нас появилось много хороших университетов не только в Москве и Санкт-Петербурге. Качественное образование вы можете получить далеко за их пределами — в Тюмени, Новосибирске, Красноярске, Томске», — добавил Степан Николаевич.
О новых материалах в современном протезировании рассказал научный сотрудник Центра композиционных материалов НИТУ «МИСиС» Фёдор Сенатов. Школьники из Тобольска поинтересовались, можно ли печатать элементы костной ткани на 3D-принтере и как быстро эта технология распространится по стране.
«Аддитивные технологии огромными шагами двигаются по всей России. Хорошие 3D-принтеры, способные напечатать костную ткань, есть во многих городах. Просто у каждого своя задача: можно печатать металлами, а можно — целыми клетками. Эти технологии есть, они активно развиваются, и это наше будущее», — ответил Фёдор.
Прямая трансляция урока была организована на портале «ПроеКТОриЯ» и в группах проекта в социальных сетях ВКонтакте и Одноклассники. К эфиру из Центра прототипирования высокой сложности «Кинетика» НИТУ «МИСиС» в режиме телемоста подключились ребята из Тобольска (родина Д.И.Менделеева), Чебоксар, Новокузнецка и Тюмени. Видеосвязь с точками подключения обеспечила компания «Ростелеком».
В конце урока модератор, известный теле—, радиоведущий Антон Комолов предложил педагогам и школьникам стать соавторами следующих открытых уроков и записать видео для рубрик «Просто о сложном» и «Поставь вопросом в тупик». А также объявил старт опроса «Кто из известных людей увлекался химией?». Правильные ответы зрители смогут узнать в группах «ПроеКТОрии» в социальных сетях.
Правильные ответы зрители смогут узнать в группах «ПроеКТОрии» в социальных сетях.
Следующий Всероссийский открытый урок состоится 21 февраля в 13:00 (мск) и будет посвящен градостроению и умным городам.
A Game of the Elements) — настольная игра Crowd Games
В 2019 году исполнилось 150 лет со дня открытия периодического закона химических элементов великим русским учёным Д. И. Менделеевым. В связи с этим Генеральная ассамблея ООН объявила 2019 год годом Периодической таблицы химических элементов. Мы не могли пройти мимо такого знаменательного события, а потому издали настольную игру «Таблица Менделеева»!
Издательство Genius Games уже 6 лет занимается созданием игр, в которых сложные физические и химические процессы (например, синтез белка) представлены очень просто, а главное — интересно. Получилось ли у них и в этот раз? Давайте разберёмся.
К середине XIX века было открыто 63 химических элемента, и учёные всего мира не раз предпринимали попытки определить закономерности, которые позволили бы создать систему, помогающую расположить химические элементы в удобном и логичном порядке.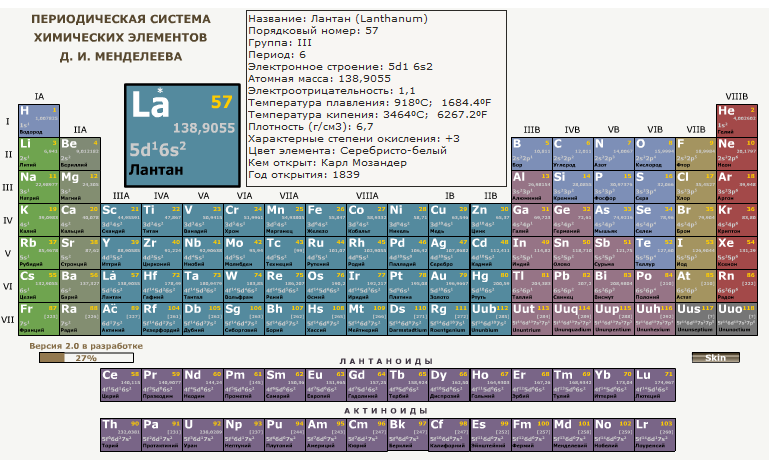 Удалось это только в 1869 году русскому химику Дмитрию Ивановичу Менделееву.
Удалось это только в 1869 году русскому химику Дмитрию Ивановичу Менделееву.
Суть открытия Менделеева заключается в том, что ему удалось обнаружить взаимосвязь свойств элементов с их атомной массой и их периодичность. Это означает, что после определённого количества разных по свойствам элементов, свойства начинают повторяться. Так, калий похож на натрий, фтор — на хлор, а золото похоже на серебро и медь. Учёный также предсказал открытие нескольких новых химических элементов и описал их химические свойства. В будущем его догадки подтвердились.
Одна из известнейших легенд (помимо, наверное, только байки об изобретении им водки) гласит, что Менделеев открыл таблицу химических элементов во сне. Однако сам химик только смеялся над этим: «Я над ней, может быть, двадцать лет думал, а вы говорите: сидел, и вдруг <…> готово!» Существует ещё более любопытная история о том, что открытию периодической таблицы поспособствовала любовь Менделеева к пасьянсам: он записывал свойства элементов на игральных картах и раскладывал их по стопкам, а это помогало ему визуализировать свои предположения об их природе. Так что Дмитрий Иванович был в некотором роде нашим коллегой — ему тоже нравились настольные игры.
Так что Дмитрий Иванович был в некотором роде нашим коллегой — ему тоже нравились настольные игры.
В коробке с игрой вы обнаружите познавательный буклет, из которого можно узнать много интересного о химии и роли таблицы Менделеева в науке и нашей жизни.
«Таблица Менделеева» — это настольная игра, построенная вокруг периодической таблицы элементов, а также некоторых принципов химии. В ней игроки будут изучать группы химических элементов, перемещаясь для этого по самой таблице. Элементы могут находиться далеко друг от друга, но тем не менее у них обязательно есть что-то общее, в соответствии с реальными химическими законами. В итоге получаем увлекательную гонку, в которой для победы вам придётся эффективно расходовать накопленную энергию и грамотно планировать свой маршрут, чтобы опередить остальных игроков, не забывая о собственных целях, полученных в начале игры.
Размер и количество карт: 63 × 88 мм — 20 шт., 110 × 70 мм — 32 шт.
Давайте заглянем в коробку игры вместе с Сергеем Рябухиным:
|
youtube.com/embed/CQdHhrnPtMg» frameborder=»0″ allowfullscreen=»allowfullscreen»/> |
Подготовка к игре представлена в этом видео:
В свой ход вы выбираете между двумя действиями:
- Вы можете заплатить энергию, чтобы переместить свою фишку колбы по таблице элементов. Первое выбранное вами периодическое свойство стоит одну единицу энергии, а каждое последующее — две единицы энергии. Они дают вам возможность переместить вашу фишку колбы в определённом направлении.
- Или вы можете забрать себе всю энергию, которая находится на одном из периодических свойств, и затем активировать его. Это действие позволяет вам совершить только одно перемещение, но собранную энергию вы сможете потратить в следующем ходу.

После каждого перемещения вы получаете возможность «открыть» элемент, на котором вы остановились.
Элементы, доступные для исследования, показаны на картах целей. На каждой из них перечислены элементы, которые имеют что-то общее. Например, все они крайне ядовиты или все очень редко встречаются в природе. На игровом поле эти элементы отмечаются соответствующей фишкой.
Существует три способа получения очков:
- Исследование семейства (вы остановились на нужном элементе).
- Выполнение целей.
- Выполнение карт задач.
Игрок, набравший наибольшее количество очков, считается победителем.
Подробнее с игровым процессом вы можете ознакомится в этом видео:
Авторами игры являются Джон Ковью, основатель издательства Genius Games, и Пол Саломон, учитель математики и заядлый игрок в настольные игры, для которого «Таблица Менделеева» — первый большой проект.
Джон же на данный момент разработал шесть научных игр, и ещё несколько готовятся к выпуску в ближайшем году. Его игры были высоко оценены школьными учителями и родителями учеников, а статьи о них публиковались в таких изданиях, как The Wall Street Journal, Popular Science, Scientific American и Gizmodo, и получили одобрение Национальной ассоциации преподавателей естественных наук США. За достоверностью игр следят не только авторы, но и многочисленные консультанты из академических кругов, а сам Джон имеет степень магистра технических наук в Вашингтонском университете.
«Моя цель — вдохновить следующее поколение на изучение науки, и я надеюсь, что наши игры будут побуждать подростков рассматривать возникающие перед ними трудности как вызовы, которые они могут преодолеть, а не как проблемы, о которых позаботятся другие».
Обычно в этом разделе можно узнать, что думают об этой игре Том Вэсел, Ричард Хэм и другие известные критики, но в этот раз здесь будут отзывы людей, которые оценивали «Таблицу Менделеева» на сайте BoardGameGeek.
Мне нравится подход, который Genius Games использовали в «Таблице Менделеева». Если сформулировать просто, то вы перемещаетесь по игровому полю и собираете элементы, чтобы выполнить карточки целей. Но есть и другие способы получать очки, поэтому вам необходимо следить не только за целями, что делает игровой процесс сложным и увлекательным.
sfarrell, 8/10
Очень забавная игра! Простая в освоении, достаточно сложная, чтобы поддерживать интерес, и настолько веселая, что хочется играть снова и снова!
Kalli4na, 8/10
Ещё один шедевр от одного из моих любимых издателей, всегда приятно видеть на полках магазинов новую игру Genius Games. Весело и познавательно, эта игра прокачает ваше мышление!
CaptSwissCheese, 10/10
Я оцениваю её исключительно как настольную игру, не за её образовательную ценность. Крепкие механики, интересный игровой процесс. Мне кажется, будто бы кто-то предложил, вот периодическая таблица, что мы можем сделать, чтобы можно было передвигаться по ней и зарабатывать очки?
borisgreggs, 7/10
Правила настольной игры «Таблица Менделеева» и буклет «Научные аспекты игры» на русском языке от Crowd Games.
Страница игры на сайте BoardGameGeek.
Страница игры на сайте «Тесера».
Страница игры на сайте Kickstarter.
Год таблицы Менделеева: как это будет?
Каким будет год периодической таблицы, сколько всего пройдет мероприятий в его рамках, как школьнику попасть на экскурсию в новый технопарк и как оставаться ученым, будучи ректором РХТУ, рассказал в интервью Indicator.Ru Александр Мажуга.
— Александр Георгиевич, 2019 год был объявлен годом таблицы Менделеева. Однако сегодня таблицу Менделеева проходят в школе, и каждый пятиклассник хотя бы визуально помнит, как она выглядит. Как вы считаете, зачем объявлять год этой таблицы, в чем главный посыл?
— Это мероприятие не только российское, это мероприятие международное. Российского химическое общество им. Д.И. Менделеева и Российская академия наук выступили в ЮНЕСКО, ООН с инициативой проведения года Периодической таблицы химических элементов. История открытия таблицы достаточно запутанная: есть английские ученые, американские, французские, которые внесли свой вклад. Но исторические данные, публикации, по которым легко определить первенство, указывают, что открытие было сделано в России, Дмитрием Ивановичем 150 лет назад. До этого в публикациях приведены данные о том, что элементы можно расположить в определенном порядке.
Дмитрий Иванович — первый, кто в этом порядке нашел закон периодичности, и в этом весь смысл. Таблица — не просто удобный способ расположения элементов. Это закон периодичности, который гласит, что свойства элементов повторяются в рядах и в периодах. На самом деле, только в России, на пространстве союзных республик и бывших социалистических стран таблица носит имя Менделеева. В других странах она не имеет имени. Задача Российской Федерации и химиков нашей страны — сделать так, чтобы на международной арене таблице официально присвоили имя Менделеева. Для этого наша страна должна приложить все усилия. Это научная дипломатия, способ еще раз показать, что наша наука, в первую очередь, естественно-научный блок, имеет вес на международной арене. Если вы помните, открытие новых трех тяжелых элементов было сделано либо в нашей стране (в Дубне), либо в сотрудничестве с российскими учеными. Сделать так, чтобы к концу года таблице присвоили имя Менделеева — наша основная задача.
— А какие мероприятия планируются в рамках этого года? Кто их организует?
— Надо разделять две категории мероприятий: те, которые будут проходить в мире, и те, которые будут проходить на территории Российской Федерации. У вас была публикация, что председатель правительства Дмитрий Анатольевич Медведев подписал приказ о проведении года Периодической таблицы Химических элементов и об организации оргкомитета, который как раз возглавил Дмитрий Анатольевич. Наш университет, РХТУ, стал соорганизатором, головной организатор, естественно — Российская академия наук, Российское химическое общество, Министерство науки и высшего образования. РХТУ, как подведомственная организация Минобра, выступает соорганизатором-оператором проведения года – не только в России, но и за рубежом.
— Кстати, про главу российского оргкомитета. Как вам работается под таким руководством?
— Дмитрий Анатольевич возглавляет «большой» оргкомитет. Туда входят представители правительства, министерств, представители химического бизнеса. Я вхожу в рабочую группу при Министерстве науки и высшего образования, но могу сказать, что очень комфортно, очень хорошо. У нас много мероприятий, много идей. Одна из важных задач — найти под них финансирование. А так — оргкомитет работает в штатном рабочем режиме. К организации открытия года в Париже и Москве привлекается команда, которая занимается Фестивалем науки «Наука 0+».
Открытие планируется грандиозным. Международная часть торжества пройдет 29 января в Париже, в ЮНЕСКО. На торжественной части мероприятия будут присутствовать около 1500 человек. Большая представительская делегация Российской Федерации — около 200 человек, среди которых будут и студенты профильных вузов. Конечно же, среди вузов — наш университет и МГУ. Параллельно с торжественным открытием три дня, начиная с 28 января, будет проходить выставка, которая будет посвящена Периодическому закону. Будет представлена история и факты, подтверждающие, что открытие было сделано Дмитрием Ивановичем Менделеевым, также будет экспозиция об истории открытия разных элементов.
— А на открытии будет большая делегация от вашего университета?
— Порядка 20 человек. Учитывая, что вся делегация от России будет около 200 человек, это составит 10%. Самая большая делегация от университетов, насколько я знаю. Также будет большая делегация от МГУ. Кстати, еще из важных моментов: в прошлом году наш университет впервые вошел в Шанхайский рейтинг вузов. Кроме него только три наших вуза туда попали: МГУ, Новосибирский государственный университет и РГУ нефти и газа имени Губкина. Это хорошая победа. И мероприятие в Париже тоже поможет продвинуться на международной арене. У нас будет стенд своего университета, который носит имя Менделеева (по-английски мы называемся Mendeleev University).
— Получается, выставкой в Париже вы рассчитываете привлечь больше иностранных студентов?
— Да, у нас уже увеличилось количество иностранных студентов. Для нас важно заниматься экспортом нашего образования. Тем более, что оно у нас достойное — особенно в области естественнонаучных дисциплин и, в частности, химической технологии. Так что популяризация вуза на международной арене тоже очень важная цель мероприятий года. Как и популяризация химии, даже для школьников.
— И что вы подготовили для школьников к торжественному открытию?
— Для школьников во время выставки будут проходить химические мастер-классы. Наш университет будет делать VR-зону, которая будет демонстрировать интерактивный практикум по неорганической химии и интерактивный химический завод. Можно будет побродить по нефтеперерабатывающему заводу, посмотреть, как он устроен. На выставке будет много студентов и школьников, большей частью, конечно, из Франции, но и из других европейских стран тоже. И наш университет везет туда интерактивный практикум по химии, настоящую химическую лабораторию. Ребенок сможет надеть очки, почувствовать себя настоящим ученым, узнать некоторые новые вещи о химических элементах и Периодическом законе.
— А какие задания там будут?
— Мы сделали такую новую задачу, которая показывает, как щелочные металлы в одном ряду имеют особые свойства, и как эти свойства меняются в ряду сверху вниз.
Еще одна важная для нас дата — 6 февраля, официальное открытие года в Москве, в Российской академии наук. Будет проходить выставка, пройдет торжественная часть, на которой запланировано выступление представителей нашего академического сообщества, один из открывателей элементов — Юрий Цолакович Оганесян из Дубны — прочитает лекцию. Приедет известный химик Мартин Полякофф из Великобритании, из Ноттингема. У профессора корни в России. Пройдет выставка, будет интерактив, представят экспозицию, где показывает химические элементы в различных областях: в космонавтике, в экологических аспектах, в «зеленой» химии, в здравоохранении, в химической технологии.
Дальше, в течение года, как в России, так и во всем мире, будут проходить разные мероприятия. Это съезды ассоциации химиков (самая большая ассоциация — ИЮПАК). В России самым большим мероприятием будет Менделеевский съезд осенью. Это самое большое собрание, конференция химиков нашей страны с международным участием. Что касается популяризации таблицы, наследия нашей страны, будет проведен ряд открытых уроков по химии на базе вузов и на базе школ. Наш университет планирует провести ряд выездных лекций. Ведь в каждом кабинете химии висит таблица, но не все знают ее суть, ее секреты. Почему были названы элементы, как они открывались. У каждого элемента есть своя история. Есть элемент, названный в честь России…
— Рутений.
— Да. Много элементов названы в честь ученых: мендеелевий, кюрий. Много элементов названы в честь городов: дубний, московий. Эти факты мы также хотим рассказать. В прошлом году наш университет проводил первый Химический диктант. Химический факультет МГУ также проводил. Я думаю, в этом году мы сделаем вместе Химический диктант на всю страну, когда в любой точке страны можно будет через компьютер подсоединиться дистанционно, оценить свои знания по химии и узнать новое о Периодической таблице, Периодическом законе.
Из мероприятий, которые планирует провести наш университет — осенью, — у нас запланировано открытие первого химического технопарка «Mendeleev Центр». Сергей Семенович Собянин подписал соответствующее распоряжение. Это будет четыре лаборатории. Первая лаборатория «Химия. Старт» — химия для самых маленьких, начиная с 3-4 класса, когда ребята могут прийти осуществить безопасные химические эксперименты. В школе у них такой предмета еще нет, а к нам они могут прийти и понять, что такое химия, для чего нужно становиться химиком. Остальные лаборатории — для ребят более старшего возраста – начиная с восьмого класса, когда химия изучается в школе. Одна лаборатория будет посвящена материаловедению, материалам для фотоники, композитные материалы; одна лаборатория посвящена неорганической химии, одна — проблемам органической химии. Помимо этого, в технопарке будет экспозиция, посвященная наследию и творчеству Дмитрия Ивановича Менделеева, и развитию химии и химической технологии в нашей стране, плюс будет ряд экспонатов, где можно будет пощупать, потрогать, посмотреть, что такое химия.
— А где будет находиться технопарк?
— Он будет располагаться на нашей площадке, для этого у нас есть трехэтажное здание с отдельным входом с улицы, которое мы сейчас начали переоборудовать.
— А как можно будет попасть на экскурсию? Это право школьник должен заслужить, или билеты будут продаваться свободно?
— У нас будут заключаться договоры со школами, чтобы классы могли приезжать, заниматься экспериментами, делать свои проекты. В выходные мы планируем, что технопарк будет работать как интерактивный музей, куда можно будет просто приходить и смотреть. Но мы еще подумаем о музейной концепции, как мы будем приглашать, привлекать ребят. Я думаю, что это должно быть доступно максимальному числу школьников и их родителей.
— Вы упомянули открытые уроки – а как вы выбирали школы для участия в этой программе?
— У нас есть обширная сеть школ Москвы и Московской области, которые с нами сотрудничают. Мы хотим расширять географию и выезжать в другие в регионы. Помимо этого, мы сотрудничаем с Ивановским химико-технологическим университетом с Казанским национально-исследовательским технологическим университетом. Мы будем передавать дидактические материалы им, и они могут ими пользоваться.
— Представим, что где-то в соседнем регионе есть какая-то школа, которая хочет с вами сотрудничать. Что они должны сделать?
— Нужно написать нам письмо. Мы рассмотрим заявку. Мы готовы сотрудничать, взаимодействовать с новыми школами, приезжать и читать лекции. И приглашаем к себе: мы уже в конце прошлого года открыли лабораторию (при финансовой поддержке DOW Chemicals). Это лабораторный практикум для работы со школьниками – отдельное помещение, хорошо оборудованное.
— Вернемся к празднованию года Периодической системы химических элементов. Будут ли мероприятия в России согласованы с тем, что проходит за рубежом? Или они отличаются?
— Есть план, утвержденный оргкомитетом. Оргкомитет есть в России и за рубежом. В планах около 60 мероприятий. Истории развиваются параллельно, где-то они пересекаются. В основном это научные конференции, и только в России делается акцент на популяризацию. Среди таких мероприятий – издание юбилейных марок, написание книги про Дмитрия Ивановича Менделеева. Сейчас есть только одна книга из серии «Жизнь замечательных людей».
Всего в России пройдет около 600 мероприятий, и если за рубежом подавляющее большинство (кроме открытия) – это научные конференции, мы делаем чуть больший упор на популяризацию.
— Тогда давайте поговорим об итогах года для РХТУ. В прошлом интервью Indicator.Ru вы говорили, что собираетесь сделать РХТУ первым проектным вузом в сфере химической технологии. Есть ли какие-то успехи?
— 2018 год был для нашего университета удачным. Во-первых, в области образования, а образование и подготовка высококвалифицированных кадров – все-таки наша первостепенная задача. К нам пришли очень хорошие ребята в этом году. Средний балл ЕГЭ сильно возрос. Если до этого он составлял 72 балла, во время приемной кампании 2018 он составил 80 баллов. Это очень большой подъем.
Мы активно пересматриваем учебные программы. И действительно, мы хотим сделать так, чтобы наш вуз готовил кадры для конкретной отрасли. Мы отвечаем за химическую технологию, химическую промышленность, и должны отвечать на запросы химпрома. Прошлый год был удачным с точки зрения развития инфраструктуры. В нашем университете давно не было ремонта и обновления материально-технической базы, оборудования. В этом году нам удалось за счет привлеченных средств и заработанных денег отремонтировать все внешние корпуса, крыши, помещения изнутри. В этом году запланировано много ремонтных работ внутри зданий, что тоже очень важно. Когда ты приходишь на работу, и университет выглядит красиво и хорошо, всегда приятно приходить пораньше и уходить попозже. Социокультурная среда для работы сотрудников и учебы студентов тоже очень важна. Мы выиграли достаточно много проектов, которые были объявлены в прошлом году, и много проектов продолжается. Были подписаны соглашений, которые должны перейти в более тесное взаимодействие с нашим бизнесом. Я думаю, это большая заслуга, что мы стали ближе к работодателям и нашей промышленности. Мы подписали соглашение о создании научно-образовательного центра с компаниями «Уралхим», «Уралкалий» и ИРЕА «Курчатовский институт» в рамках предстоящего конкурса на НОЦы. Мы наладили взаимодействия с представителями фармацевтической отрасли, где очень много химии, тонкого органического синтеза фармсубстанций, и подписали ряд соглашений по разработке технологий получения важных препаратов.
— Можете привести конкретные примеры?
— Один из примеров — препарат Лопинавир, предназначенный для лечения вирусных заболеваний, прежде всего ВИЧ. Мы помогаем решить одну из проблем национальной безопасности – проблему импортозамещения. Много говорят о том, что санкции – это угроза потери лекарственных субстанций.
Наш университет готов включиться в работу и помогать стране создавать отечественные субстанции. Такая же ситуация сейчас и с композитными материалами. Сейчас громкая история — импортозамещение материалов для МС-21 (новый российский пассажирский авиалайнер – прим. Indicator.Ru): композиты под санкциями, а компонентной базы отечественной нет. Опять же, тут наш университет выполняет ряд проектов по разработке технологий получения композитных материалов.
Сейчас мы работаем над крупными проектами, которые, надеюсь, будут реализованы. Мы активно включились в проект по 216-му ФЗ («Об инновационных научно-технологических центрах и о внесении изменений в отдельные законодательные акты Российской Федерации» – прим. Indicator.Ru). В рамках этого проекта в Тульской области наш филиал, а также Тульский государственный университет и МГУ создают Композитную долину. Это отечественные композиты, прежде всего для аэрокосмической промышленности, на основе углеродных материалов и не только, разнообразные конструкционные материалы.
— Также в интервью вы упоминали, что собираетесь составить программу развития вуза до 2025 года. Как продвигается работа?
— Что касается стратегии — мы не приняли ее в прошлом году. Чем больше мы погружаемся в специфику нашей отрасли и деятельность университета, тем больше появляется дополнений и изменений. Мы понимаем, что этот процесс может быть бесконечным, но в этом году надо остановиться и принять это решение.
— Желательно до 2025 года ее принять.
— Да, я надеюсь, что в этом году мы ее точно сделаем. Мы сейчас активно работаем над стратегией.
— А что вы можете сказать о научной деятельности университета в 2018 году? Находили ли вы сами время заниматься наукой?
— Было опубликовано много статей (больше, чем в предыдущие годы). Для РХТУ год был очень удачный, хотя и непростой. Выиграны проекты рффи, рнф, намечены планы на будущее.
В принципе, год был удачным и в моей научной лаборатории, где мы тоже опубликовали рекордное количество статей. Мы провели первые доклинические испытания контрастного средства для визуализации опухоли головного мозга (это уже моя наука), надеюсь, что скоро клинические испытания начнутся. Проблема импортозамещения в диагностике тоже решается в соответствии с майскими указами президента и запросами Министерства здравоохранения.
— С точки зрения научной работы стало ли менее «обидно быть ученым», как вы выразились в прошлый раз?
— Нам нужно сделать так, чтобы наши преподаватели старались больше заниматься наукой. В моем понимании (и эту политику я продвигаю в университете), любой преподаватель – это ученый. Среди наших преподавателей есть «чистые ученые», ведущие активную научно- исследовательскую работу, коллеги публикуют научные труды, получают гранты, эти умения передают студентам, прививают студентам любовь к науке. Но мы вуз технологический, и большое внимание уделяем разработке новых технологических решений, в данном случае кафедры больше направлены на работу с промышленностью. И по-другому быть не должно: либо преподаватель двигает науку, либо очень близок к технологии. Мы стараемся помогать нашим преподавателям, чтобы они могли уделить больше времени науке.
— И последний вопрос. РХТУ получил право самостоятельно присуждать ученые степени (об этом вам тоже задавали вопрос в предыдущем интервью). Вы говорили, что вам больше импонирует модель МГУ. Как вы воплотили этот план? Присуждены ли уже какие-то ученые степени?
— Нет, пока не присуждены, мы работаем по ВАКовской системе. Мы должны перейти на собственное присуждение ученых степеней с 1 сентября 2019 года. Сейчас мы разрабатываем и практически согласовали установочные документы. И действительно, мы выбрали модель, которая максимально приближена к модели МГУ и ВАКа, но подняли требования по количеству публикаций, и я думаю, что близко к системе МГУ и ВАКа и останемся, и уже в начавшемся году перейдем на собственные диссоветы. У нас будет ряд объединенных советов (по биотехнологии) и закрытый совет (по спецтематикам), которые будут работать по ВАКу.
Источник: Индикатор
Где искать самую старую таблицу Менделеева?
Об этом в рамках открытой лекции «150 лет Периодической системе химических элементов Д. И. Менделеева. История создания» школьникам рассказал Евгений Олегович Калинин, старший преподаватель СПбГУ (кафедра радиохимии). «Данный демонстрационный вариант был изготовлен по указанию самого Дмитрия Ивановича в 1876 году. Недавно средства массовой информации писали о якобы найденной в Сент-Эндрюсском университете самой старой в мире Периодической таблице химических элементов. Так вот, это не так, — рассказывает Евгений Калинин. — Как выяснили эксперты, настенная таблица, обнаруженная в Шотландии, была напечатана в 1880-х годах. И хотя это, безусловно, интересная находка, по-настоящему ценный демонстрационный вариант Периодической системы находится в СПбГУ, в Большой химической аудитории».
Евгений Калинин обратил внимание школьников на разницу в датах между формулированием Периодического закона в 1869 году и созданием его графического образа в виде таблицы в 1876 году. Что происходило в течение семи лет? Почему первый публичный вариант таблицы не был создан раньше?
Когда Дмитрий Иванович сформулировал Периодическую систему, он еще и сам не был уверен в том, в каком окончательном виде следует ее подавать. На осмысление этого вопроса у него ушло несколько лет.
Старший преподаватель СПбГУ Евгений Калинин
Представленный в аудитории СПбГУ вариант не соответствует тому, к которому мы все привыкли. По словам химика, в этой таблице, например, не хватает восьмой (VIII) группы химических элементов — благородных газов. «Они к моменту создания данного варианта таблицы еще не были открыты, и, честно сказать, ни сам Менделеев, ни его современники, конечно, не предполагали, что благородные газы вообще существуют в природе. Поэтому для них места в этом варианте не отведено», — поясняет Евгений Калинин.
Нет в этой таблице и некоторых химических элементов. На их местах стоят прочерки. Эти элементы тогда еще не были открыты, но Дмитрий Иванович Менделеев был убежден, что они должны быть. «На это указывает и тот факт, что в некоторых клеточках нет символа химических элементов, но указан атомный вес. Например, рядом с Са стоит прочерк и цифра 44. Химического элемента нет, но четко указана, какая у него должна быть масса», — объясняет Евгений Калинин.
Менделеев не просто разложил химические элементы по полочкам в зависимости от их атомного веса и химических свойств. Он еще и предсказал, что нужно работать не только с известными на тот момент элементами, но и вести поиск новых.
Старший преподаватель СПбГУ Евгений Калинин
Лекция прошла в аудитории, которая носит название Большой химической. Она находится в здании, построенном в 1894 году по инициативе Дмитрия Ивановича Менделеева. По словам Евгения Калинина, в конце XIX века ежегодно химию в Университете изучали почти 400 человек. При этом больших аудиторий и лабораторий для занятий не было. Поэтому Дмитрий Иванович в 1880-х годах предложил построить специальный лабораторный корпус для преподавания химии в Университете. Правда, сам Менделеев в нем лекции уже не читал, но председательствовал на заседаниях Русского физико-химического общества.
Открытая лекция для школьников прошла в рамках цикла мероприятий, посвященных 150-летию открытия Периодического закона и 185-летию со дня рождения Дмитрия Ивановича Менделеева. На ней присутствовали учащиеся Волховской средней общеобразовательной школы № 1 и лицея № 554 Приморского района Санкт-Петербурга. Следующая лекция состоится 22 февраля.
Все, что стоит знать о Периодической таблице
Независимо от того, висит ли она на стенах классной комнаты, в комнатах общежития или на футболках, периодическая таблица элементов кричит: «Наука!» как никакое другое изображение. И почему бы нет? В таблице насчитывается 118 членов и их число растет, и в ней перечислены все известные химические элементы, (в основном) неизменные строительные блоки всех материалов во Вселенной.
Но это не просто случайный список элементов. Организация периодической таблицы показывает поведение и характеристики элемента: от размера атома, плотности и содержания до того, как он, вероятно, будет взаимодействовать с другими.
Elements 101
Все состоит из атомов, а атомы состоят из своих собственных крошечных частиц: электроны полуслучайно порхают вокруг центрального ядра, состоящего из нейтронов и протонов. (Нейтроны и протоны состоят из других частиц: кварков.) Число протонов, также называемое атомным номером, определяет элемент — измените это, и вы измените сам элемент.
(Источник: DesignUA / Shutterstock)
Как читать таблицу
Многие периодические таблицы включают атомный номер (количество протонов) и атомный вес (который зависит от протонов и нейтронов).Иногда они перечисляют полное название каждого элемента, но часто включают только их одно- или двухбуквенные символы, прозвища, которые делают сложные химические формулы более компактными. Если символ не соответствует названию (как в Au для золота и Na для натрия), вероятно, он основан на оригинальном латинском названии элемента (aurum и natrium).
Элементы в одном столбце часто имеют общие черты, поэтому химики называют эти группы. Грубо говоря, чем правее группа, тем больше у нее электронов, готовых к взаимодействию с другими элементами.Первая группа, известная как щелочные металлы, имеет только один такой электрон, который легко потерять при реакции с элементом, который имеет больше электронов, например, с одним из 17-й группы, галогенами. Благородные газы в последнем столбце названы так, потому что они удерживают все электроны, какие только могут, поэтому им нелегко вступить в реакцию с другими элементами — как это было в старинных благородных домах.
Строки в периодической таблице называются периодами, а сейчас их семь. Они перечисляют элементы в порядке атомных номеров перед тем, как отсечь и продолжить в новом ряду, повторяя установленные образцы химических свойств.Сложная часть построения таблицы — это знать, когда они отсекаются — или, что то же самое, сколько столбцов (групп) включать в каждую строку.
(Источник: Элисон Макки / Discover)
Ряды лантанидов и актинидов — эти два ряда, плавающие сами по себе, названные в честь их первых членов, лантана и актиния, — изолированы таким образом, как уступка ограниченному пространству. Они действительно должны быть зажаты среди других элементов, но полный непрерывный стол был бы слишком громоздким и занимал бы слишком много места.
(Источник: Элисон Макки / Discover)
Общая форма таблицы Менделеева может показаться неровной, но она отражает сумасшедшую орбиту электронов вокруг атомных ядер. Они не вращаются по красивым, аккуратным кругам, как планеты вокруг Солнца; вместо этого электроны разбрасываются в формы, называемые орбиталями, которые зависят от того, сколько других электронов находится поблизости. Например, первые два столбца включают сферические s-орбитали, которые могут содержать до двух электронов; большой блок колонн от бора до неона группирует элементы с вариациями p-орбиталей в форме гантелей.
Периодическая таблица элементов
Воспользуйтесь этой возможностью, чтобы взглянуть на периодическую таблицу и лично убедиться в некоторых ее скрытых открытиях.
(Источник: Элисон Макки / Discover)
Первая периодическая таблица
Ученые давно создали рудиментарные таблицы известных элементов, но 150 лет назад русский химик наделил современную таблицу своей мощью. В 1869 году Дмитрий Менделеев установил то, что мы теперь называем периодическим законом: определенные тенденции, такие как температура плавления и атомный радиус, периодически повторяются среди элементов, когда они перечислены в порядке возрастания атомного веса.Завершите строку и начните новую, когда этот паттерн начнется заново, и вы получите нечто очень похожее на текущую периодическую таблицу, где столбцы представляют общие черты.
Но, что важно, Менделеев не был большим сторонником своих собственных правил. Он оставил пробелы в своей таблице, где, как он чувствовал, могут лежать неоткрытые элементы, даже предсказывая (правильно) некоторые из их атрибутов. И иногда он придумал аранжировку, чтобы сохранить вместе одинаковые элементы, даже если они технически не в порядке. Как оказалось, в начале 20 века химики узнали, что истинный порядок элементов определяется не атомным весом, а количеством протонов в ядре элемента — понимание, которое привело к незначительным изменениям в таблице, спасибо к выдумкам Менделеева.
К настоящему времени ученые заполнили все эти пробелы в таблице. Последние элементы были обнаружены всего 12 лет назад, и в настоящее время мы ищем еще больше, надеясь начать новый ряд.
Дмитрий Менделеев (Источник: Fine Art Images / Heritage Images / Getty Images)
Кто выбирает названия и символы новых элементов?
Первооткрыватели делают — с согласия Международного союза теоретической и прикладной химии (IUPAC). ИЮПАК обычно предлагает окончание названия на -ium для согласованности, и в прошлом практика заключалась в почитании мест (америций и полоний), людей (кюрий и эйнштейний) и даже планет (уран и плутоний).До того, как элемент получил официальное имя, его имя-заполнитель основывается на латинских названиях его атомного номера: oganesson, номер 118, был известен как ununoctium (один-один-восемь-юм).
Есть ли другие столы?
В то время как знакомый прямоугольник является наиболее знаковой и стандартной версией периодической таблицы, существуют и другие организационные схемы, такие как таблица ADOMAH, которая подчеркивает формы электронов, и спиральная таблица Отто Теодора Бенфея, которая более компактна и непрерывна.
(Источник: Wikimedia Commons, Элисон Макки / Discover)
(Источник: Wikimedia Commons, Элисон Макки / Discover)
Все о Периодической таблице
Периодическая таблица
Периодическая таблица, также известная как таблица Менделеева, представляет собой таблицу химических элементов, существующих на Земле.Русскому химику Дмитрию Менделееву приписывают его создание в 1869 году, хотя до этого существовали менее обширные таблицы. Он намеревался отобразить закономерности, проявляющиеся в химических свойствах каждого элемента. С момента его создания были обнаружены новые элементы и добавлены к исходной таблице Менделеева.
СТРУКТУРАСтруктура таблицы Менделеева очень важна. Текущая таблица содержит 117 элементов в очень четком порядке с целью показать сходства и различия в химических свойствах.Из всех элементов 94 встречаются в природе, а остальные 24 были произведены синтетически с помощью ускорителей частиц. Кроме того, большинство копий таблицы Менделеева разделяют металлические и неметаллические элементы темной линией ступенек. Металлы находятся слева, а неметаллы — справа. Кроме того, элементы располагаются в порядке возрастания атомного номера, который представляет собой количество протонов в ядре атома элемента. Строки также организованы таким образом, что элементы с похожими свойствами находятся в одних и тех же столбцах.Внутри квадрата каждого элемента можно найти информацию о символе элемента, атомном номере, атомной массе, электроотрицательности, электронной конфигурации и валентных числах. Внизу периодической таблицы находится двухрядный блок элементов, содержащих лантаноиды и актиниды. Эти группы классифицируются как внутренние переходные металлы.
КЛАССИФИКАЦИЯХимические элементы, классифицированные по группам, периодам и блокам. Группы, также называемые семьями, представляют собой вертикальные столбцы, расположенные в периодической таблице.Группы считаются наиболее важной формой классификации. Многие группы содержат элементы с очень похожими свойствами и имеют специальные названия, такие как галогены и щелочноземельные металлы. Точки состоят из горизонтальных строк таблицы. Так же, как группы содержат определенные тенденции в сходных свойствах, периоды тоже. Например, d-блок содержит ряд переходных металлов. Блоки важны как различные области периодической таблицы из-за внешней оболочки, состоящей из выборов внутри атомов элементов.Блоки ориентированы на эту внешнюю оболочку. Блоки периодической таблицы включают s-блок, p-блок, d-блок и f-блок. Другие группы включают бедные металлы, переходные металлы, металлоиды и платиновую группу.
ХИМИЧЕСКИЕ СВОЙСТВАРасположение элементов в периодической таблице чрезвычайно важно из-за тенденций изменения химических свойств в группах и строках. Свойства элемента можно фактически предсказать, основываясь на его расположении в таблице. Важно помнить, что тренды действуют по-разному при перемещении по таблице вертикально и горизонтально.Тенденции внутри групп объясняются общей электронной конфигурацией в их валентных оболочках. Это также создает сходство в атомном радиусе, электроотрицательности и энергии ионизации. Сверху группы вниз атомные радиусы элементов увеличиваются. Точно так же энергия ионизации и электроотрицательность уменьшаются из-за электронной конфигурации. Периоды также обладают аналогичными тенденциями в электроотрицательности, энергии ионизации, атомных радиусах, а также сродстве к электрону. Двигаясь от левой части таблицы Менделеева к правой, атомные радиусы уменьшаются, что приводит к увеличению энергии ионизации.Кроме того, при движении слева направо возрастают электроотрицательность и сродство к электрону.
ИНТЕРАКТИВНЫЕ РЕСУРСЫПериодическая таблица: интерактивная таблица с подробной информацией по каждому элементу.
Периодическая таблица химических элементов: интерактивный ресурс для изучения отдельных элементов.
Периодическая таблица: интерактивная таблица с биографией Дмитрия Менделеева.
Электроны и периодическая таблица: ресурс о важности электронной конфигурации и периодических тенденций.
Enhanced NMR Periodic Table: еще одна интерактивная таблица с интерактивными элементами от Техасского университета A&M.
Все, что вам нужно знать о Периодической таблице
Таблица Менделеева — одно из тех классических изображений, которые вы найдете во многих научных лабораториях и классах. Это изображение почти каждый видел когда-либо в своей жизни.
Вы также можете найти таблицу Менделеева на футболках, кружках, пляжных полотенцах, наволочках, пододеяльниках и многих других предметах.Он даже вдохновил меня на сборник рассказов.
Кто может забыть таблицу Менделеева, положенную на музыку американцем Томом Лерером, профессором математики из Гарварда, который также был певцом / автором песен и сатириком. Его песня The Elements включает в себя все элементы, которые были известны на момент написания в 1959 году.
С тех пор в периодическую таблицу Менделеева было добавлено несколько новых элементов, в том числе четыре, которые были официально одобрены в прошлом году Международным союзом чистой и прикладной химии (IUPAC).
Но что именно показывает таблица Менделеева?
Короче говоря, это попытка организовать совокупность элементов — всех известных чистых соединений, состоящих из одного типа атомов.
Есть два способа посмотреть, как устроена таблица Менделеева, основанная либо на наблюдаемых свойствах содержащихся в ней элементов, либо на субатомном строении атомов, образующих каждый элемент.
Основная современная таблица Менделеева.Shutterstock / Duntaro
Элементы
Когда ученые начали собирать элементы в 1700-х и 1800-х годах, медленно выявляя новые в течение десятилетий исследований, они начали замечать закономерности и сходство в их физических свойствах.Некоторые были газами, некоторые — блестящими металлами, некоторые бурно реагировали с водой и так далее.
В то время, когда элементы были впервые открыты, структура атомов не была известна. Ученые начали искать способы систематизировать их, чтобы схожие свойства можно было сгруппировать вместе, точно так же, как кто-то, собирающий ракушки, может попытаться организовать их по форме или цвету.
Задача осложнялась тем, что не все элементы были известны. Это оставляло пробелы, из-за которых расшифровка шаблонов немного напоминала попытку собрать мозаику из недостающих частей.
Разные ученые придумали разные типы таблиц. Первую версию нынешней таблицы обычно приписывают русскому профессору химии Дмитрию Менделееву в 1869 году, а обновленная версия — в 1871 году.
Периодическая таблица Менделеева впервые опубликована за пределами России в Zeitschrift für Chemie (1869, страницы 405-6).
(Викимедиа / Дмитрий Менделеев)
Важно отметить, что Менделеев оставил пробелы в таблице, куда, по его мнению, следует поместить недостающие элементы.Со временем эти пробелы были заполнены, и появилась окончательная версия, которую мы знаем сегодня.
Атомы
Чтобы действительно понять окончательную структуру периодической таблицы, нам нужно немного понять об атомах и о том, как они устроены. У атомов есть центральное ядро (ядро), состоящее из более мелких частиц, называемых протонами и нейтронами.
Это число протонов, которое дает элементу его атомный номер — число, которое обычно находится в верхнем левом углу каждого прямоугольника в периодической таблице.
Свойства водорода, указанные в периодической таблице.
(Shutterstock / duntaro)
Таблица Менделеева расположена в порядке возрастания атомных номеров (слева направо, сверху вниз). Он варьируется от элемента 1 (водород H) в верхнем левом углу до недавно утвержденного элемента 118 (oganesson Og) в правом нижнем углу.
Количество нейтронов в ядре может быть разным. Это дает начало различным изотопам для каждого элемента.
Например, вы, возможно, слышали о датировании по углероду-14 для определения возраста объектов.Этот изотоп представляет собой радиоактивную версию обычного углерода C (или углерода-12), который имеет два дополнительных нейтрона.
Но почему под основной таблицей находится отдельный блок элементов, и почему основная таблица имеет странную форму с выступом наверху? Это сводится к тому, как устроен другой компонент атома — электроны.
Электроны
Мы склонны думать, что атомы устроены чем-то вроде луковицы, с семью слоями электронов, называемыми «оболочками», обозначенными K, L, M, N, O, P и Q, окружающими ядро ядра.
Представьте себе атом с центральным ядром, содержащим все протоны и нейтроны, окруженным серией оболочек, содержащих электроны.
(Разговор, CC BY-ND)
Каждая строка в периодической таблице как бы соответствует заполнению одной из этих оболочек электронами. У каждой оболочки есть подоболочки, и порядок, в котором они заполняются, зависит от требуемой энергии, хотя это сложный процесс. Мы вернемся к ним позже.
Проще говоря, первый элемент в каждой строке запускает новую оболочку, содержащую один электрон, в то время как последний элемент в каждой строке имеет две (или одну для первой строки) подоболочек во внешней оболочке, полностью занятых.Эти различия в электронах также объясняют некоторые сходства свойств между элементами.
С одной или двумя подоболочками во внешнем слое, заполненными электронами, последние элементы каждого ряда совершенно инертны, поскольку во внешней оболочке нет дыр или зазоров для взаимодействия с другими атомами.
Вот почему элементы в последнем столбце, такие как гелий He, неон (Ne), аргон (Ar) и так далее, называются благородными газами (или инертными газами). Все они газы, и они «благородны», потому что редко связываются с другими элементами.
Напротив, элементы первого столбца, за исключением водорода (как и в грамматике английского языка, всегда есть исключения!), Называются щелочными металлами. Элементы первого столбца похожи на металл по своему характеру, но имея только один электрон во внешней оболочке, они очень реактивны, поскольку этот одинокий электрон очень легко задействовать в химической связи. При добавлении в воду они быстро реагируют с образованием щелочного (основного) раствора.
Каждая оболочка может вместить все большее количество электронов.Первая оболочка (K) подходит только для двух, поэтому в первой строке периодической таблицы всего два элемента: водород (H) с одним электроном и гелий (He) с двумя.
Вторая оболочка (L) вмещает восемь электронов. Таким образом, вторая строка периодической таблицы содержит восемь элементов с зазором между водородом и гелием для размещения дополнительных шести.
Третья оболочка (M) вмещает 18 электронов, но третий ряд по-прежнему содержит только восемь элементов. Это связано с тем, что дополнительные десять электронов не добавляются к этому слою до тех пор, пока первые два электрона не будут добавлены к четвертой оболочке (N) (почему мы узнаем позже).
Таким образом, зазор в четвертом ряду увеличен для размещения дополнительных десяти элементов, что приводит к «отрыву» от верхней части стола. Дополнительные десять соединений в средней части называются переходными металлами.
Четвертая оболочка содержит 32 электрона, но, опять же, дополнительные электроны не добавляются к этой оболочке до тех пор, пока некоторые из них также не будут добавлены к пятой (O) и шестой (P) оболочкам, что означает, что как четвертый, так и пятый ряды содержат 18 элементов.
Для следующих двух строк (шестой и седьмой) вместо дальнейшего расширения таблицы в сторону для включения этих дополнительных 14 элементов, которые сделают ее слишком широкой, чтобы ее было легко читать, они были вставлены как блок из двух строк, называемый лантаноидами. (элементы с 57 по 71) и актиноиды (элементы с 89 по 103) под основной таблицей.
Периодическая таблица выглядела бы иначе, если бы лантаноиды и актиноиды были включены в нее.
(Разговор, CC BY)
Вы можете увидеть, где они могли бы поместиться, если бы периодическая таблица была расширена, если вы посмотрите на два нижних квадрата в третьем столбце таблицы выше.
По столбцам
Есть еще один усложняющий фактор, определяющий окончательную форму стола. Как упоминалось ранее, по мере того, как электроны добавляются к каждому слою, они переходят в разные подоболочки (или орбитали), которые описывают места вокруг ядра, где они с наибольшей вероятностью могут быть обнаружены.Они известны под буквами s, p, d и f.
Буквы, используемые для орбиталей, фактически получены из описаний излучения или поглощения света электронами, движущимися между орбиталями: s harp, p rincipal, d iffuse и f undamental.
Каждая оболочка имеет свою собственную конфигурацию подоболочек с именами от 1s до 7p, что дает общее количество электронов в каждой оболочке по мере продвижения по периодической таблице.
(Разговор, CC BY-ND)
Как упоминалось ранее, порядок, в котором подоболочки заполняются электронами, не так прост. Вы можете увидеть порядок, в котором они заполняются, на изображении ниже, просто следуйте порядку, как вы читали бы слева направо.
(Разговор, CC BY-SA)
Существует интерактивная таблица Менделеева, которая также хорошо иллюстрирует последовательность заполнения, если вы щелкаете по атомам.
Элементы в столбце обычно имеют схожие свойства, но в некоторых местах элементы, расположенные рядом, также могут быть похожими.Например, в переходных металлах кластеры драгоценных металлов вокруг меди (Cu), серебра (Ag), золота (Au), палладия (Pd) и платины (Pt) очень похожи.
Большинство существующих элементов с высокими атомными номерами, включая четыре сверхтяжелых элемента, добавленные в прошлом году, очень нестабильны и никогда не были обнаружены в природе или изолированы от нее.
Вместо этого они создаются и анализируются в ничтожных количествах в сильно искусственных условиях. Теоретически могут быть и другие элементы, помимо известных сейчас 118 (есть дополнительные суборбитали g, h и i), но мы пока не знаем, будет ли какой-либо из них достаточно стабильным, чтобы быть изолированным.
Классический дизайн
Периодическая таблица Менделеева видела много красочных и информативных версий, созданных за эти годы.
Периодическая таблица украшает такси в Великобритании.
(Flickr / Fr Gaurav Shroff, CC BY-NC-ND)
Одна из моих любимых — художественная версия с оригинальными произведениями искусства для каждого элемента, заказанная Королевским химическим институтом Австралии по случаю Международного года химии в 2011 году.
Другой фаворит — интерактивная версия с изображениями элементов.Создатели этого сайта также опубликовали журнальный столик под названием The Elements и приложение Apple с видеороликами о каждом элементе.
Интерактивные версиибыли также созданы Королевским химическим обществом (их также можно загрузить как приложение) и ChemEd DL среди других.
Классический дизайн таблицы Менделеева может быть использован для игры в «Морской бой».
Играем в линкоры с периодической таблицей на первом Всемирном фестивале науки в Брисбене в 2016 году.
(Разговор, CC BY-NC-ND)
Существует также множество забавных версий, которые помогают организовать множество объектов, включая еду, пиво, смайлики, приложения для iPad и птиц.
Что касается The Elements Тома Лерера, песня еще не обновлена, чтобы включить все элементы, известные сегодня, но на протяжении многих лет на нее делали каверы.
Актер Дэниел Рэдклифф, прославившийся о Гарри Поттере, исполнил одну из версий во время выступления в качестве гостя на шоу Грэма Нортона BBC.
Существуют и другие музыкальные версии элементов, но они тоже еще не обновлены, чтобы включить все записи периодической таблицы.
Таким образом, периодическая таблица — это химическая систематика всех элементов. Его триумф в том, что он по-прежнему актуален для ученых, а также становится частью популярной культуры.
Марк Бласкович, старший научный сотрудник, Квинслендский университет
Эта статья переиздана из The Conversation по лицензии Creative Commons.
Как далеко заходит Периодическая таблица?
До декабря 2015 года в периодической таблице были дыры, элементы были синтезированы, но еще не признаны официально.Но когда мы вступаем в Международный год Периодической таблицы, классическая периодическая таблица была заполнена до седьмой строки: в конце 2015 года Международный союз теоретической и прикладной химии официально подтвердил элементы 113, 115, 117 и 118. Новая элементы также получили свои окончательные названия: нихониум, московий, теннессин, оганессон. Усилия по поиску следующих элементов, 119 и 120, продолжаются.
Периодическая таблица элементов — «стойкий символ» химии, химик Эрик Р.Шерри восторгалась. «Он украшает стены лекционных залов и лабораторий всех типов, от университетов до промышленных предприятий», — писал он в книге American Scientist . «Это одна из самых мощных икон науки. Он отражает суть химии в одном элегантном узоре ». Дмитрий Менделеев впервые опубликовал схему организации всех известных в то время элементов в 1869 году, и эта система, хотя и не была совершенной, стала фундаментальной в изучении химии.
Вначале даже Менделеев не осознавал масштабов своего открытия.
Менделеев не был первым, кто придумал систему для классификации элементов, но, как отмечает Скерри, «его версия оказала наибольшее влияние на научное сообщество». В периодической таблице элементы упорядочены по строкам в соответствии с их атомным номером, числом протонов в ядре атома и по столбцам в соответствии с конфигурациями самых удаленных электронов атома. Эта конфигурация обычно определяет «индивидуальность» элемента, а также его размер и форму.Мягкие металлы, такие как литий и калий, которые сильно реагируют с другими, населяют одну колонку, в то время как фтор и йод, неметаллические реактивные элементы, живут в другой.
Менделеев предсказал не только существование неизвестных тогда элементов, но и их свойства. Вначале даже Менделеев не осознавал масштабов своего открытия, пишет историк науки Майкл Гордин. «Если бы Менделеев осознавал значение периодической системы, он, вероятно, не отнес бы ее представление к Русскому химическому обществу в марте 1869 года Н.А. Меншуткин, когда он уезжал проверять сыродельные кооперативы ». Но это быстро изменилось: «к 1871 году Менделеев совершенно ясно выразил свою веру в то, что он выделил новый закон химии».
Из 1-го английского издания книги Дмитрия Менделеева «Принципы химии» (1891 г.), опубликованной на Wikimedia Commons. Этот закон доводится до предела, поскольку химики синтезируют новые элементы. Уже сейчас, когда атомные номера становятся все выше, химические свойства некоторых из новых элементов не похожи на свойства других элементов той же группы.Это, как пишет Скерри в статье для Scientific American за 2013 год, «может подорвать само логическое обоснование существования таблицы: повторяющиеся закономерности, давшие название таблице Менделеева». Сколько именно элементов еще предстоит открыть? Есть ли конец периодической таблицы Менделеева? Когда мы его достигнем? Что он учит нас о природе элементов?
Создание новых элементов
До тех пор, пока физики не исследовали обломки ядерных реакторов и взрывов, были известны только 92 элемента природного происхождения, вплоть до урана.В радиоактивном материале физики обнаружили новые элементы: нептуний, плутоний, америций, эйнштейний и другие. Однако, помимо элемента 100, фермия, даже водородные бомбы не были достаточно мощными, чтобы производить новые элементы, поэтому ученые изменили свою тактику.
Вместо грубой силы ключом была ловкость. Ученые использовали циклотроны и ускорители, чтобы довести ионы легких элементов до высокой скорости, а затем выстрелили ими по ядрам элементов с более высокими атомными номерами. Если все шло правильно, ядра атомов в пучке и мишени сливались.Цель: добавить протон и увеличить атомный номер, тем самым создав новый элемент. Соответственно, первый элемент, созданный таким образом, получил название менделевий.
Исследовательские центры в США и России, в основном Национальная лаборатория Лоуренса Беркли и Объединенный институт ядерных исследований в Дубне, развивались в 1950-х, 60-х и 70-х годах. Каждые несколько лет открывался и назывался новый элемент, который в конечном итоге достигал элемента 106 (сиборгий). Центр исследований тяжелых ионов GSI им. Гельмгольца (GSI) в Германии одержал верх, изменив свой подход к «холодному синтезу»: фокусировка низкоэнергетического луча на цель с высоким атомным номером привела к открытию элементов из бория. (107) до копернициума (112).
Создавая новые сверхтяжелые элементы, ученые сражаются против основ природы.
Создание нового элемента — мимолетная радость, и на самом деле это, по-видимому, основная причина для ученых, которые их создают. Как пишет ведущий физик-ядерщик Юрий Оганесян, в честь которого назван элемент 118, в Scientific American пишет: «Бомбардируя тяжелые ядра ионными пучками более легких ядер, ученые создают сверхтяжелые ядра, которые настолько нестабильны, что расщепляются на части, зачастую лишь крошечные. доли секунды после их создания.”
Создавая новые сверхтяжелые элементы, ученые сражаются против основ природы: в элементах с низким атомным весом протоны и нейтроны слипаются, потому что сильное ядерное взаимодействие объединяет их. Но когда все больше и больше протонов упаковывается в ядро, сильная ядерная сила начинает уступать другой силе, кулоновской силе. Эта сила заставляет частицы одного заряда раздвигать друг друга. Большинство сверхтяжелых ядер подвергаются ядерному делению в течение миллисекунд, расщепляясь на более легкие элементы, или они сначала выплевывают несколько альфа-частиц, состоящих из двух протонов и двух нейтронов, а затем распадаются на части.
На берегу острова стабильности
С элементами 113–118 первооткрыватели приближались к дразнящей цели: острову стабильности. Теории предсказывают, что когда определенное «магическое» число протонов и нейтронов упаковано в ядро, ядро становится более стабильным и долгоживущим. Кальций, никель, олово и свинец имеют исключительно стабильные ядра, что, по мнению теоретиков, связано с тем, что эти элементы имеют магическое число протонов и / или нейтронов. Эти «магические числа» соответствуют заполненным ядерным оболочкам, которые могут сделать ядро более стабильным.
Элементы, вокруг которых встречаются магические числа протонов и нейтронов, «остров стабильности», привлекают исследователей сверхтяжелых элементов. Но точное местоположение острова в периодической таблице неизвестно. Некоторые из вновь синтезированных элементов кажутся более стабильными: одна форма элемента 117 со 177 нейтронами задерживается на 112 миллисекунд. Следующим «магическим числом» нейтронов будет 184, но пока максимум — 177 нейтронов. Ученые могут приближаться к берегу, но они еще не достигли суши.
Периодический закон (по Круксу), опубликованный в 1933 году на Wikimedia Commons. Это потому, что создание даже небольшого количества нового сверхтяжелого элемента — это сверхтяжелая задача. Создание элемента 117 представляло особую проблему. Единственное место, где производится достаточное количество мишени, берклия, — это Окриджская национальная лаборатория в Теннесси, в тысячах миль от Дубны, где группа Оганесяна провела столкновение. Производство беркелия началось за два года до начала эксперимента в Дубне.Потребовалось 250 дней облучения, чтобы произвести достаточное количество берклия, и 90 дней обработки, чтобы очистить его. Затем часы начали тикать. Берклий радиоактивен с периодом полураспада 327 дней. Все 22 миллиграмма должны были быть доставлены в ОИЯИ в течение временного окна, в котором ускоритель и пучок были доступны. Это сработало: 150 дней бомбардировки драгоценной мишени из берклия кальцием создали шесть атомов элемента 117.
Работа по созданию элемента 119, следующего сверхтяжелого элемента, началась в декабре 2017 года в лаборатории RIKEN в Вако, Япония.С 2019 года команда Оганесяна в Дубне готовится к охоте на 119 человек. Еще в 2007 году исследователи в Дубне и GSI в Германии начали попытки синтезировать элемент 120. До сих пор не было обнаружено никаких признаков того или иного элемента.
В неизвестность
Попытки заполнить восьмую строку периодической таблицы могут привести к новому пониманию физики атомов. Элементы имеют периодическую структуру в своих химических свойствах, потому что эти свойства в значительной степени определяются пространством, в котором электроны атома обитают вокруг его ядра, особенно в самой внешней области.Эти области, математически описываемые как «орбитали», имеют дискретный диапазон размеров и форм, а структуры внешних орбиталей изменяются периодическим или повторяющимся образом. Таким образом, атомы с разными атомными номерами могут иметь похожие формы, что приводит к повторяющемуся или «периодическому» рисунку блоков элементов, которые имеют одинаковые внешние орбитальные формы. С элементом 121 электроны займут совершенно новую орбиталь, с которой никогда раньше не сталкивались, — g-орбитали.
Никто толком не знает, где закончится стол.
Насколько крупнее может увеличиться таблица Менделеева, все еще остается открытым вопросом. «Мы знаем, что количество элементов в таблице Менделеева конечно. Необходимо ответить на вопрос: как далеко мы можем зайти? » написали физики Питер Армбрустер и Фриц Петер Хессбергер, соавторы элементов 108-112, в Scientific American . На момент написания, в 1998 году, они уже признали, что было достигнуто: «Мы прошли долгий путь с 1940-х годов, когда Нильс Бор предсказал, что фермий, элемент 100, будет последним элементом периодической таблицы.”
Ричард Фейнман предсказал, что элемент 137 будет последним. Но на самом деле никто не знает, где закончится стол. Расчеты конца таблицы основаны на теории относительности. Когда ядра становятся больше, больше протонов в ядре означает большую силу, притягивающую электроны, поэтому электроны, движущиеся вокруг них, должны двигаться все быстрее и быстрее, достигая скоростей, которые составляют значительную часть скорости света. На этих скоростях электроны становятся «релятивистскими», а поведение атомов отличается от ожидаемого, исходя из их положения в таблице.В конце концов, расчеты предсказывают, что электроны должны будут двигаться быстрее света, что невозможно. Исходя из этого, некоторые ученые предсказывают, что концом может быть элемент 170, поскольку это может быть точка, в которой достаточно протонов, чтобы попросить электроны сделать невозможное.
Периодическая таблица, опубликованная в мае 2016 г. на Wikimedia Commons. Мы видим некоторые релятивистские эффекты в элементах повседневной жизни. В атомах золота электроны вращаются вокруг ядра со скоростью, превышающей половину скорости света.Это изменяет орбитали электронов так, что золото поглощает синий свет, а фотоны всех других цветов отражаются. Мы наблюдаем белый свет минус синий свет, характерный золотисто-желтый блеск обручальных колец, который отличает золото от окружающих его серебристых элементов в периодической таблице.
Будут ли химические свойства вновь открытых элементов подчиняться периодичности, или релятивистские эффекты приведут к трещинам в периодическом законе? Поскольку новые сверхтяжелые вещества производятся в очень малых количествах, химики не могут исследовать их с помощью традиционных подходов, таких как засовывание элемента в колбу и наблюдение за его реакцией с другими химическими веществами.Вместо этого они разрабатывают эксперименты, чтобы получить простые ответы «да-нет» об их свойствах, спрашивая, например, будет ли элемент 112 при очень низкой температуре связываться с золотом, как металл? Будет ли он оседать на льду, как благородный газ?
Уже в 1990-х годах ранние эксперименты показали, что резерфорд (104) и дубний (105) не ведут себя в соответствии с их положением в периодической таблице. Согласно периодическому закону, эти два элемента должны вести себя как элементы, находящиеся прямо над ними, гафний и тантал.Вместо этого резерфорд реагирует как плутоний, который находится довольно далеко в периодической таблице, в то время как дубний ведет себя как протактиний, удаленный элемент в таблице. Но не все супертяжеловесы ведут себя неожиданно. Сиборгий (106) и бориум (107) действуют так, что в соответствии с тем, что предсказывала таблица Менделеева, научные статьи по ним были озаглавлены «Странно обыкновенный сиборгий» и «Скучный бориум», — отмечает Скерри.
Остается ли периодическая таблица Менделеева периодической для очень тяжелых атомов, как признает Шерри, «не имеет большого практического значения, по крайней мере, в обозримом будущем.Потеря предсказательной способности в сверхтяжелой сфере не повлияет на полезность остальной части таблицы ». Однако «вопрос о влиянии специальной теории относительности затрагивает самое сердце химии как дисциплины». Если периодический закон потеряет предсказательную силу из-за специальной теории относительности, химия будет больше полагаться на физику. Но если периодический закон останется (в основном) действующим, химия сохранит некоторую независимость.
Периодическая таблица элементов — Science Learning Hub
Периодическая таблица элементов объединяет все известные элементы в группы с аналогичными свойствами.Это делает его важным инструментом для химиков, нанотехнологов и других ученых. Если вы поймете периодическую таблицу Менделеева и научитесь ее использовать, вы сможете предсказать, как будут вести себя химические вещества.
Здесь мы рассмотрим только основы, но этого должно быть достаточно, чтобы вы начали изучать закономерности и взаимосвязи, которые можно найти в таблице.
Атомы
Атомы — это строительные блоки материи. Атом состоит из трех основных частей — протонов, нейтронов и электронов.Есть более мелкие частицы, но они нас здесь не интересуют. Протоны и нейтроны образуют ядро в центре атома (водород немного отличается, у него есть только протон). Электроны перемещаются в большом пространстве за пределами ядра. Электроны организованы по энергетическим уровням — поведение элемента зависит от того, насколько легко получить или потерять электроны на самых внешних энергетических уровнях.
Атомный номер
Атомный номер элемента — это количество протонов в атоме — количество протонов определяет, что такое элемент.Например, если у атома шесть протонов, это может быть только углерод. Атомный номер также может сказать нам, сколько электронов имеет атом. Исходя из этого, мы можем понять, как расположены электроны, и это расскажет нам, как элемент будет реагировать с другими.
Элементы
Элемент — это вещество, состоящее из атомов с одинаковым атомным номером. Элементы не могут быть разделены на более простые вещества обычными химическими методами. Элемент железо состоит только из атомов железа, а атомы железа везде одинаковы — атомы железа на Земле такие же, как атомы железа на Марсе.
Таблица Менделеева
Вам поможет копия таблицы Менделеева — та, что здесь, поможет вам начать работу, или вы можете распечатать полную таблицу с веб-сайта ниже.
У каждого элемента есть квадрат в периодической таблице. В некоторых версиях таблицы эти квадраты могут содержать много надписей, но для начала достаточно трех частей информации — каждый квадрат должен содержать название элемента, его официальный химический символ и его атомный номер. Например, квадрат для железа будет выглядеть примерно так:
. Вы заметите, что элементы в периодической таблице расположены в ряды и столбцы.
- Строки называются периодами.
- Столбцы называются группами.
Элементы в группе (столбце) имеют одинаковое количество внешних электронов, поэтому они имеют схожие химические свойства.
Существует очевидная закономерность, на которую следует обратить внимание:
- Атомный номер увеличивается по мере того, как вы двигаетесь вправо по строке.
- Атомный номер увеличивается по мере движения вниз по столбцу.
Есть и другие закономерности. Например, энергия, необходимая для отвода электрона от атома:
- возрастает при движении слева направо
- понижается при перемещении сверху вниз
Чем больше вы узнаете об атомной структуре, тем больше закономерностей и взаимосвязей вы найдете в периодической таблице.
Имена групп
Группы элементов с похожими свойствами имеют имена и обычно окрашиваются в периодическую таблицу по-разному.
Группа 1 | Щелочные металлы. |
Группа 2 | Щелочноземельные металлы. |
Группы 3–12 | Переходные металлы — Периодические таблицы имеют дополнительный блок переходных металлов внизу, для элементов, называемых редкоземельными элементами (или лантаноидами) и актинидами.Атомные номера этих элементов фактически находятся в нижнем левом углу основной таблицы. |
Группы 13–16 | Металлы, полуметаллы и неметаллы — у них есть общие свойства, но их недостаточно для группы, чтобы заполнить столбец. |
Группа 17 | Галогены. |
Группа 18 | Благородные газы. |
Водород имеет атомный номер 1, поэтому он находится в верхнем левом углу таблицы с щелочными металлами группы 1.Он имеет такое же количество электронов на внешнем энергетическом уровне, что и другие элементы в группе 1, но, поскольку это газ, он обычно относится к неметаллической группе.
Идеи действий
- Развитие периодической таблицы — Используйте эту статью, чтобы узнать о первом научном открытии элемента в 1649 году и о том, как он превратился в периодическую таблицу в том виде, в каком мы ее знаем сегодня.
- Атомные часы — Используйте ресурс для учителей по атомным часам, чтобы познакомить учащихся с названиями и символами химических элементов.
- Элементный рэп — в этом упражнении учащиеся знакомятся с названиями и символами химических элементов, создавая рэп или стихотворение.
- Поиск символа — в этом упражнении учащиеся знакомятся с символами химических элементов, создавая их, используя буквы из фразы или предложения.
Связанное содержимое
Команда Центра научного обучения подготовила коллекцию ресурсов, связанных с периодической таблицей элементов. Войдите, чтобы сделать эту коллекцию частью вашей частной коллекции, просто нажмите на значок копии.Затем вы можете добавить дополнительный контент, примечания и внести другие изменения. Зарегистрировать учетную запись в Science Learning Hubs легко и бесплатно — зарегистрируйтесь, используя свой адрес электронной почты или учетную запись Google. Найдите кнопку «Войти» вверху каждой страницы.
Полезные ссылки
Ниже приведены некоторые сайты, посвященные таблице Менделеева. У них есть интерактивные занятия для студентов.
В 2019 году периодической таблице элементов исполняется 150 лет. Радио Новой Зеландии отмечает Международный год Периодической таблицы элементов сериалом «Элементаль».Каждую пятницу в «Ночах с Брайаном Крампом» есть элемент недели.
Посетите веб-сайт Международного года Периодической таблицы Менделеева.
Давайте узнаем о таблице Менделеева
Периодическая таблица Менделеева узнаваема сразу. Эта хорошо известная таблица находится в учебниках химии и на стенах классных комнат. В нем собраны все известные элементы, и он существует в различных формах уже более 150 лет. Но версия той диаграммы, которую построил русский ученый Дмитрий Менделеев в 1869 году, отличается от той, которую мы видим сегодня.
См. Все записи из серии «Давайте узнаем».
В то время его диаграмма содержала всего 63 элемента. Это все, что было известно. Менделеев оставил пробелы в своей таблице, где должны были подходить предсказанные, но еще не известные элементы. И как только ученые нашли все встречающиеся в природе, они начали бомбардировать два элемента вместе, чтобы создать новые элементы. Сегодня в таблице 118 известных элементов.
В этом видео корреспондент Science News по физике Эмили Коновер объясняет, что нужно, чтобы установить достоверность настоящего, нового элемента — и назвать его.Последним участникам потребовались годы экспериментов, а затем решение судейской коллегии.
Хотите узнать больше? Для начала у нас есть несколько историй:
Неизменно полезная таблица Менделеева Химии отмечает большой день рождения: ей 150 лет, и эта «таблица» может принимать самые разные формы, от блок-схем до спиральных деревьев — и не зря (21.11.2019) Читаемость: 8,2
У новейших элементов наконец-то есть имена: Nihonium? Теннессин? Это не части тела или лекарства.Они входят в число названий, данных четырем новейшим сверхтяжелым элементам. (08.06.2016) Читаемость: 8.5
Астрономы наконец-то нашли космический источник золота и серебра: гравитационные волны указывают на ответы на некоторые давние загадки Вселенной (16.10.2017) Читаемость 8.1
Узнать больше
Ученые говорят: Периодическая таблица
Ученые говорят: атомный номер
Explainer: Зоопарк частиц
Отправляйтесь на периодическую охоту за мусором, пока вы застряли дома.Сколько элементов можно найти, не выходя из дома?
Из Science News : 150 лет спустя периодическая таблица Менделеева содержит больше историй, чем элементов, и Как периодическая таблица превратилась из эскиза в непреходящий шедевр.
Неизменная таблица Менделеева Химии отмечает большой день рождения
Висящие на стене квадраты выглядят как неровная стена из блоков алфавита. Буквы не составляют слова. Столбцы неровные. Эта диаграмма — символ химии — известна как Периодическая таблица элементов.Дмитрий Менделеев (MEN-duh-LAY-ev), российский ученый, работающий в Санкт-Петербурге, предложил раннюю версию. Это было 150 лет назад. Но даже сегодня эта диаграмма помогает ученым разобраться в атомах и молекулах, составляющих нашу Вселенную.
Элементы — это строительные блоки всей материи. Их атомы соединяются вместе, образуя буквально все — нас, воздух, которым мы дышим, организмы, которые разделяют наш мир, и все остальные молекулы газа или частицы массы, встречающиеся во всей нашей Вселенной.
Строки и столбцы периодической таблицы соответствуют так называемому периодическому закону . Он утверждает, что общие черты между химическими элементами повторяются в регулярных паттернах по мере увеличения элементов. Эти паттерны связывают элементы со схожим химическим поведением и помогают химикам рассказать, как атомы реагируют с образованием молекул. То, как выстраиваются строки и столбцы в этой таблице, указывает на общие черты между группами связанных элементов. Понимание этих отношений помогает химикам создавать новые соединения.Это также помогает им понять, как устроена жизнь. Это даже помогает им предсказать, как будут вести себя новые материалы.
В 1869 году русский химик Дмитрий Менделеев предложил периодический закон и свою первую таблицу Менделеева. Он опубликовал эту периодическую таблицу два года спустя в учебнике Основы химии ( Основы химии ). Ряд строк показывает, что химия носит периодический характер, а это означает, что определенные свойства повторяются. Основываясь на повторяющихся шаблонах, он оставил пробелы для четырех элементов, которые, как он ожидал, будут существовать.В течение 10 лет ученые откроют три из них.
Дмитрий Менделеев / Институт истории науки
Но хорошо известная таблица Менделеева — далеко не единственная таблица Менделеева. Ученые построили множество, некоторые из которых имеют самые разные формы. Некоторые разработали химики. Ученые и учителя в других областях разработали другие.
«Альтернативные формы полезны из-за различных аспектов науки, которые они иллюстрируют», — отмечает Кармен Джунта. Он химик в колледже Ле Мойн в Сиракузах, штат Нью-Йорк.Y. Эти менее традиционные периодические таблицы дают возможность не только выделить некоторые из особенностей химии, — говорит он, но и сфокусировать их на них.
Учителя и родители, подпишитесь на шпаргалку
Еженедельные обновления, которые помогут вам использовать Science News для студентов в учебной среде
В 2019 году мир отмечает периодическую таблицу Менделеева во всех ее формах и то, как она помогает организовать и осмыслить строительные блоки нашей Вселенной.
ЭлементарноСразу после Большого взрыва Вселенная состояла только из водорода и гелия — двух самых легких элементов. Гравитация сближала эти атомы во все больших количествах. В конечном итоге это создаст плотные, раскаленные огненные печи, которые мы знаем как звезды. В центре этих звезд сильное давление сливало атомные ядра — центры атомов — создавая более крупные ядра.
Это медленно выкованные более крупные и тяжелые элементы. Они включали углерод, элемент, необходимый для всей жизни, какой мы ее знаем.Эти звездные кузницы также образовали кислород, которым мы должны дышать.
Создание элементов крупнее железа требовало еще большей космической огневой мощи. Тяжелые атомные ядра образовались в результате взрыва массивных умирающих звезд. Эти сверхновые силой столкнули более мелкие элементы вместе.
Менделеев в своей периодической таблице 1869 года расположил элементы в порядке возрастания массы. Он был одним из первых ученых, которые осознали, что в химии есть повторяющиеся закономерности. По мере того, как элементы становятся больше, некоторые из их свойств со временем повторяются.Некоторые элементы предпочитают реагировать, становясь положительно заряженными. Некоторые предпочитают заряжаться отрицательно. Такие закономерности позволили ученым предугадать, будут ли сочетаться разные типы элементов и как они это будут.
Менделеев написал в своем исследовательском журнале, что идея этого стола пришла ему во сне. Он начал с скандала. Но когда химические свойства повторились, он начал новую серию. Он выстроил элементы с похожим поведением в столбцы. Он оставил пробелы. Эти отверстия, рассуждал он, обозначают элементы, которые, вероятно, существовали, но еще не были обнаружены.
Когда он опубликовал эту таблицу, Менделеев предсказал свойства и массы четырех новых элементов. В конце концов все четыре были обнаружены — три всего за 10 лет.
Самая ранняя спираль была спроектирована французским геологом Александром-Эмилем Бегуайе де Шанкуртуа в 1862 году. У нее не было «рядов». Вместо этого все элементы намотаны вокруг цилиндра в одну длинную линию.
Александр-Эмиль Бегуайе де Шанкуртуа / Wikimedia Commons
Александр-Эмиль Бегуйе де Шанкуртуа был французским геологом.За семь лет до знаменитой таблицы Менделеева он создал спиральную «таблицу». Он расположил элементы в порядке их атомного веса. Он показал повторяющиеся периоды. Однако перерывов между рядами не было. Вместо этого он намотал свою длинную тонкую диаграмму на цилиндр. Таким образом, каждая строка перетекала в следующую. И похожие элементы выстроились друг над другом аккуратными столбиками.
Другие ученые составили аналогичные диаграммы. Вскоре усилия по систематизации всех известных элементов нарастали.По мере развития всех этих диаграмм одна из них стала доминирующей. Его сегодня можно встретить в классах и в учебниках по всему миру.
Каждый из 118 известных элементов имеет свой собственный химический символ — одну или две буквы, которые гордо представляют название элемента из его поля в периодической таблице. Некоторые из этих сокращений очевидны, например, H для водорода или C для углерода. Другие восходят к древним временам. Например, символ натрия — Na. Почему? На латыни натрий называется natrium .
Каждое поле в таблице имеет целое число, обычно в верхнем левом углу. Названный атомным номером, он показывает, сколько протонов или положительно заряженных частиц упаковано в ядро элемента. Это ядро также включает нейтроны (частицы с массой, но без заряда). Ядро окружает облако, состоящее из отрицательно заряженных электронов гораздо меньшего размера.
Нижнее число в квадрате диаграммы для каждого элемента включает цифры после десятичной точки. Это значение представляет собой атомную массу элемента.Он представляет собой среднюю массу атома этого элемента.
Периодическая таблица Менделеева проста, мощна и продолжает давать новые эксперименты, — говорит Эрик Шерри. Он преподает химию в Калифорнийском университете в Лос-Анджелесе. Он также пишет книги о таблице Менделеева. Он описывает организационные принципы, лежащие в основе периодической таблицы, как «абсолютно важное открытие».
Двойные башни стали доминироватьСамая распространенная сегодня таблица Менделеева иногда известна как версия «башен-близнецов».Водород (H) венчает высокую башню слева. Гелий (He) наверху правой башни.
Периодический круглый стол расставляет элементы из массива дерева. Он разработан, чтобы показать, как электроны расположены в виде узоров внутри каждого элемента. В этой конструкции в форме дерева периоды роста становятся частью более широких дисков. Подобные элементы накладываются друг на друга. Вы можете удалить каждый слой, чтобы увидеть элементы в каждой «строке».
Гэри Кац / Институт истории науки
По мере того, как атомы становятся больше, они становятся более сложными.В этих диаграммах период в периодической таблице относится к ряду элементов, демонстрирующих некоторый повторяющийся цикл. В таблице ширина строки, также называемая точкой, определяется таким образом, чтобы сохранялся шаблон поведения элементов в столбце. Сначала узор повторяется в двух элементах, так что ширина ряда составляет два элемента. Затем узор повторяется в восьми элементах. По мере того, как элементы становятся больше, как отмечает Скерри, «периоды становятся все длиннее и длиннее» — в конечном итоге с 18 элементами, а затем с 32.
Чем длиннее, тем больше периоды могут сделать базу из тяжелых элементов этой таблицы неуклюже широкой. Чтобы обойти это, диаграмма двойной башни обычно вытаскивает часть двух нижних рядов. Эти элементы размещаются внизу страницы, почти как сноски. Эти нижние ряды содержат группы элементов, известных как лантаноиды (LAN-tha-nydes) и актиниды (AK-tih-nydes).
Актиниды включают новейшие и самые крупные элементы. Многие из них радиоактивны и не встречаются в природе.Вместо этого физики делают их в лабораториях, бомбардируя более мелкие элементы друг в друга. Эти радиоактивные сверхтяжелые элементы также очень нестабильны. Это означает, что они распадаются на более мелкие элементы за доли секунды.
Чем они полезныТаблица Менделеева может служить своего рода книгой рецептов. На диаграмме показано, как элементы соотносятся друг с другом. То, где элемент находится на столе, говорит химику, как он может или не может взаимодействовать с другими ингредиентами.Часто эти полезные характеристики включают его массу, температуру кипения и другие важные данные.
Расположение стола помогает химикам решать проблемы. Например, химики могут захотеть создать новое соединение с характеристиками, аналогичными существующему — только лучше. Таким образом, они могут искать замену с аналогичными функциями, начиная с другого элемента из того же столбца таблицы.
Настоящий дар этих таблиц, говорит Бриджит Ван Тиггелен, — это «хранение всей информации в одном месте, обучение и обмен ею.Историк, она работает европейским директором Института истории науки в Филадельфии, штат Пенсильвания,
.Диаграмма с двумя башнями имеет много преимуществ, — говорит Марк Лич. Он работает химиком в Англии в Манчестерском столичном университете. Он утверждает, что ни одна другая таблица не может так хорошо отображать повторяющиеся шаблоны, в то же время включая другие функции.
Например, все металлы находятся слева. Справа торчат неметаллы. На этой диаграмме также показано, как изменяется размер атома и насколько легко он может отдать электрон.Такие черты важны для понимания того, как атомы будут действовать, реагировать и вступать в брак с другими, образуя молекулы.
Альтернатива Роя Александра столу Twin Tower разрезает ряды на полоски. Когда он снова собрал их вместе, получилась трехмерная версия таблицы Менделеева. Он также оказался почти идентичным тому, что был создан физиком Георгием Гамовым четверть века назад.
Рой Александр
Но диаграмма башен-близнецов не идеальна.
Химики часто спорят, например, где разместить водород и гелий.А плоская двухмерная таблица на самом деле не показывает, как строки соединяются друг с другом. Когда вы подходите к концу одного ряда, Шерри говорит: «У вас возникает ощущение, что вы как бы падаете».
Рой Александр работал строителем выставок. Ему не понравилось, как внезапно закончились ряды стола в башне близнецов. Поэтому в 1965 году он разрезал традиционную таблицу Менделеева на полоски. Затем он собрал их вместе, создав трехмерную версию.
Спустя годы он узнал, что физик Георгий Гамов построил почти идентичную таблицу в 1940-х годах.Александр вспоминает: «Было удивительно, насколько он выглядел идентичным моему патентному рисунку».
Учет все более продолжительных периодовКогда Бегуйе де Шанкуртуа впервые создал свою периодическую таблицу, многие из крупнейших элементов еще не были обнаружены. По мере увеличения элементов общие черты повторяются все реже. В конце концов, более длинные ряды с элементами лантаноидов и актинидов сделали традиционную таблицу неуклюже широкой.
Трехмерный стол может включать эти более длинные строки, просто делая спираль шире.Канадский химик Фернандо Дюфур разработал ElemenTree, чтобы проиллюстрировать это (см. Фото). Он сделал каждый период в виде шестиугольного слоя, который содержал все элементы, которые обычно появляются в одном ряду на диаграмме с двумя башнями. Подобные элементы по-прежнему выстраиваются вертикально.
Канадский химик Фернандо Дюфур разработал ElemenTree, показанный здесь, для обработки все более крупных «рядов» в виде кольца в этой трехмерной периодической «таблице».
Ingenium / Канадские музеи науки и техники / Ingenium
Но стол в форме дерева — не единственный трехмерный ответ.В 1950-х годах учительница химии Дженни Клаусон использовала цилиндр для своего стола. Но вместо того, чтобы выпирать лишние элементы, она подтянула некоторые из них к центру.
Еще одна проблема со столом с двумя башнями — куда поместить водород и гелий. Например, водород иногда действует скорее как металл. Он сбрасывает свой электрон и притягивает отрицательно заряженные ионы. В других случаях он действует как неметалл, захватывает лишний электрон и становится отрицательно заряженным. Затем он действует больше как фтор или хлор и поглощает положительные ионы.
Чтобы учесть это, химик Теодор Бенфей создал в 1960-х годах плоский спиральный столик. Он поместил водород и гелий в центр большого синего круга. Каждая из трех внешних спиц внутри круга представляет собой группу похожих элементов. Чтобы включить более крупные элементы и возрастающие периодические циклы, он добавил террасы, выступающие из круга. К ним относятся переходные металлы, лантаноиды и актиниды.
Плоский стол, такой как башни-близнецы, удобно повесить на стену или распечатать в книге.Однако Лич добавляет: «На самом деле нет причин, по которым таблица Менделеева не является трехмерной».
Развлечения и игры?Одно из последних дополнений к растущей библиотеке периодических таблиц поступило от Европейского химического общества (ECS). Компания ECS, расположенная в Брюсселе, Бельгия, стремится привлечь внимание к относительной нехватке многих важных элементов. В нем отмечается, что в обычный сотовый телефон входит 30 элементов. И многие из этих элементов не являются широко доступными.
Одна из новейших таблиц была разработана Европейским химическим обществом. Он показывает каждый «блок» на диаграмме, размер которого соответствует его относительной численности или редкости на Земле. Показанная здесь на английском языке таблица также имеет версии на 32 других языках, включая галисийский, иврит, шотландский гэльский, русский и китайский (мандаринский).
Европейское химическое общество (CC BY-ND)
«Нам необходимо внимательно изучить нашу склонность к выбрасыванию и ненадлежащей переработке таких предметов», — утверждает ECS.«Если не будут предложены решения, мы рискуем увидеть, что многие природные элементы, из которых состоит окружающий нас мир, закончатся — будь то из-за ограниченных запасов, их расположения в зонах конфликтов или нашей неспособности полностью их переработать».
ECS признает, что этот новый стол «заставляет задуматься». И это не случайно. Он хочет, чтобы люди поняли, как важно не тратить зря «исчезающие элементы». В нем говорится, что каждый должен «задаться вопросом, действительно ли необходимы обновления наших телефонов и других электронных устройств.«И когда наша электроника умирает, — говорится в документе, -« нам нужно убедиться, что мы перерабатываем », чтобы относительно дефицитные элементы« не попадали на свалки и не загрязняли окружающую среду ».
Чтобы изучить, как люди используют элементы, ECS разработала бесплатную онлайн-видеоигру Elementary Escapades.
«Есть много места для новых периодических таблиц», — говорит Лич из Манчестера. Фактически, он стал хобби собирать новые и размещать их в Интернете. Он также всегда ищет старых.«Я, наверное, получаю новый каждую неделю», — говорит он.
Scerri также попросил студентов разработать новые. «У каждого из них, — говорит он, — есть свои собственные достоинства».

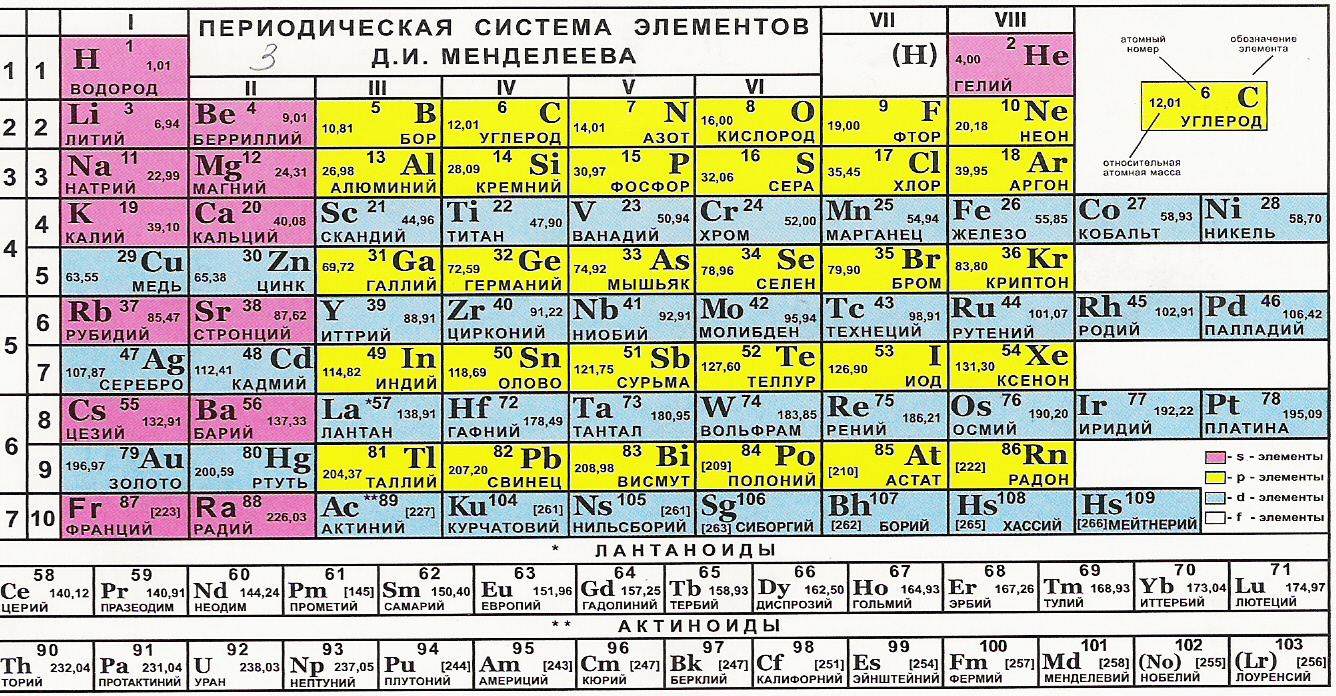 И на сегодняшний день 118 элементов располагаются по той самой структуре, которую придумал Менделеев».
И на сегодняшний день 118 элементов располагаются по той самой структуре, которую придумал Менделеев».