Периодическая таблица Менделеева / Блог :: Бингоскул
Таблица Менделеева является фундаментом нашего современного знания о химии.
Содержание:
- Сколько элементов в таблице Менделеева?
- Классический вид периодической таблицы Менделеева
- Таблица Менделеева для ЕГЭ по химии
- Периодический закон Менделеева
Сколько элементов в таблице Менделеева?
Ответ: 118 или 126 элементов в зависимости от вида таблицы.
Почему такая разница?
В природе люди обнаружили 94 элемента. Другие 24 элемента были созданы в лабораториях. Всего получается 118 штук. Еще 8 элементов являются лишь гипотетическими вариантами.
Классический вид периодической таблицы Менделеева


Таблица Менделеева для ЕГЭ по химии
Ниже приведена таблица, которую можно использовать на ЕГЭ по химии, входит в пакет разрешенных документов.
Периодический закон Менделеева
Существуют две формулировки периодического закона химических элементов: классическая и современная.
Классическая, в изложении его первооткрывателя Д.И. Менделеева:
«Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементов».
Современная:
«Свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера)».
Ряд активности металлов
Таблица растворимости солей, кислот, оснований в воде
Решай с ответами задания ЕГЭ по химии:
Таблица Менделеева
Периодическая таблица Менделеева
Таблица Менделеева, (или периодическая система химических элементов) — это таблица, которая квалифицирует химические элементы по различным свойствам, зависящим от заряда атомного ядра. Эта система выражает, в виде таблицы, периодический закон химических элементов, который в 1869 году открыл Русский ученый химик Д.И. Менделеев. Самый первый вариант таблицы, был разработан Менделеевым в 1869-1871 годах, он определял зависимость свойств химических элементов, от атомной массы (в то время это называлось атомным весом). Было предложено несколько сотен различных вариантов изображения свойств химических элементов, от аналитических кривых графиков, и до различных геометрических фигур. Но ученые, в конце концов, сошлись во мнении, что самым удобным вариантом будет изображение в виде двухмерной таблицы, в которой каждый столбик будет указывать на физико-химические свойства того или иного элемента, а периоды элементов приближенных друг к другу, будут определять строки таблицы.
Открытие, сделанное Русским химиком Менделеевым, сыграло (безусловно) наиболее важную роль в развитии науки, а именно в развитии атомно-молекулярного учения. Это открытие позволило получить наиболее понятные, и простые в изучении, представления о простых и сложных химических соединениях. Только благодаря таблице мы имеем те понятия об элементах, которыми пользуемся в современном мире. В ХХ веке проявилась прогнозирующая роль периодической системы при оценке химических свойств, трансурановых элементов, показанная еще создателем таблицы.
Разработанная в ХIХ веке, периодическая таблица Менделеева в интересах науки химии, дала готовую систематизацию типов атомов, для развития ФИЗИКИ в ХХ веке (физика атома и ядра атома). В начале ХХ века, ученые физики, путем исследований установили, что порядковый номер, (он же атомный), есть и мера электрического заряда атомного ядра этого элемента. А номер периода (т.е. горизонтального ряда), определяет число электронных оболочек атома. Так же выяснилось, что номер вертикального ряда таблицы определяет квантовую структуру внешней оболочки элемента, (этим самым, элементы одного ряда, обязаны сходством химических свойств).
Открытие Русского ученого, ознаменовало собой, новую эру в истории мировой науки, это открытие позволило не только совершить огромный скачек в химии, но так же было бесценно для ряда других направлений науки. Таблица Менделеева дала стройную систему сведений об элементах, на основе её, появилась возможность делать научные выводы, и даже предвидеть некоторые открытия.
 Одна из особенностей периодической таблицы Менделеева, состоит в том, что группа (колонка в таблице), имеет более существенные выражения периодической тенденции, чем для периодов или блоков. В наше время, теория квантовой механики и атомной структуры объясняет групповую сущность элементов тем, что они имеют одинаковые электронные конфигурации валентных оболочек, и как следствие, элементы которые находятся в пределах одой колонки, располагают очень схожими, (одинаковыми), особенностями электронной конфигурации, со схожими химическими особенностями. Так же наблюдается явная тенденция стабильного изменения свойств по мере возрастания атомной массы. Надо заметить, что в некоторых областях периодической таблицы, (к примеру, в блоках D и F), сходства горизонтальные, более заметны, чем вертикальные.
Одна из особенностей периодической таблицы Менделеева, состоит в том, что группа (колонка в таблице), имеет более существенные выражения периодической тенденции, чем для периодов или блоков. В наше время, теория квантовой механики и атомной структуры объясняет групповую сущность элементов тем, что они имеют одинаковые электронные конфигурации валентных оболочек, и как следствие, элементы которые находятся в пределах одой колонки, располагают очень схожими, (одинаковыми), особенностями электронной конфигурации, со схожими химическими особенностями. Так же наблюдается явная тенденция стабильного изменения свойств по мере возрастания атомной массы. Надо заметить, что в некоторых областях периодической таблицы, (к примеру, в блоках D и F), сходства горизонтальные, более заметны, чем вертикальные.
Таблица Менделеева содержит группы, которым присваиваются порядковые номера от 1 до 18 (с лева, на право), согласно международной системе именования групп. В былое время, для идентификации групп, использовались римские цифры. В Америке существовала практика ставить после римской цифры, литер «А» при расположении группы в блоках S и P, или литер «В» — для групп находящихся в блоке D. Идентификаторы, применявшиеся в то время, это то же самое, что и последняя цифра современных указателей в наше время (на пример наименование IVB, соответствует элементам 4 группы в наше время, а IVA – это 14 группа элементов). В Европейских странах того времени, использовалась похожая система, но тут, литера «А» относилась к группам до 10, а литера «В» — после 10 включительно. Но группы 8,9,10 имели идентификатор VIII, как одна тройная группа. Эти названия групп закончили свое существование после того как в 1988 году вступила в силу, новая система нотации ИЮПАК, которой пользуются и сейчас.
Многие группы получили несистематические названия травиального характера, (к примеру – «щелочноземельные металлы», или «галогены», и другие подобные названия). Таких названий не получили группы с 3 по 14, из за того что они в меньшей степени схожи между собой и имеют меньшее соответствие вертикальным закономерностям, их обычно, называют либо по номеру, либо по названию первого элемента группы (титановая, кобальтовая и тому подобно).
Химические элементы относящиеся к одной группе таблицы Менделеева проявляют определенные тенденции по электроотрицательности, атомному радиусу и энергии ионизации. В одной группе, по направлению сверху вниз, радиус атома возрастает, по мере заполнения энергетических уровней, удаляются, от ядра, валентные электроны элемента, при этом снижается энергия ионизации и ослабевают связи в атоме, что упрощает изъятие электронов. Снижается, так же, электроотрицательность , это следствие того, что возрастает расстояние между ядром и валентными электронами. Но из этих закономерностей так же есть исключения, на пример электроотрицательность возрастает, вместо того чтобы убывать, в группе 11, в направлении сверху вниз. В таблице Менделеева есть строка, которая называется «Период».
Среди групп, есть и такие у которых более значимыми являются горизонтальные направления (в отличии от других, у которых большее значение имеют вертикальные направления), к таким группам относится блок F, в котором лантаноиды и актиноиды формируют две важные горизонтальные последовательности.
Элементы показывают определенные закономерности в отношении атомного радиуса, электроотрицательности, энергии ионизации, и в энергии сродства к электрону. Из-за того, что у каждого следующего элемента количество заряженных частиц возрастает, а электроны притягиваются к ядру, атомный радиус уменьшается в направлении слева направо, вместе с этим увеличивается энергия ионизации, при возрастании связи в атоме — возрастает сложность изъятия электрона. Металлам, расположенным в левой части таблицы, характерен меньший показатель энергии сродства к электрону, и соответственно, в правой части показатель энергии сродства к электрону, у не металлов, этот показатель больше, (не считая благородных газов).
Разные области периодической таблицы Менделеева, в зависимости от того на какой оболочке атома, находится последний электрон, и в виду значимости электронной оболочки, принято описывать как блоки.
В S-блок, входит две первые группы элементов, (щелочные и щелочноземельные металлы, водород и гелий).
В P-блок, входят шест последних групп, с 13 по 18 (согласно ИЮПАК, или по системе принятой в Америке — с IIIA до VIIIA), этот блок так же включает в себя все металлоиды.
Блок — D, группы с 3 по 12 (ИЮПАК, или с IIIB до IIB по-американски), в этот блок включены все переходные металлы.
Блок – F, обычно выносится за пределы периодической таблицы, и включает в себя лантаноиды и актиноиды.
А теперь о «Таблице Менделеева»
Каждый советский школьник, знавший химию на отлично (я, например), был уверен в следующем факте: Периодический закон и Периодическая система химических элементов были изобретены великим русским ученым Менделеевым, и точка. Первенство, уникальность и гений Менделеева не подлежали никакому сомнению.
Но на первом курсе университета, в учебнике немецкого языка мной с удивлением был обнаружен текст под названием Lothar Meyer, из которого я узнал, что у периодической системы как минимум два автора, которые сделали открытия вроде бы как независимо друг от друга. И это зародило серьезные сомнения в уникальности гения, тем более что своё открытие немец Лотар Мейер опубликовал… в 1864 году, на 5 лет раньше Менделеева (1869).
Сегодня вы можете узнать настоящую историю открытия Периодического Закона.
Немаловажным является тот факт, что оба ученых — и Лотар Мейер, и Дмитрий Менделеев, в 1860-м году посетили съезд химиков в Карлсруэ, Германия. На этом съезде идея зависимости свойств химических элементов от их атомных весов просто витала в воздухе.
Но еще задолго до этого съезда попытка систематизации элементов была сделана Дёберайнером (в 1829 году). Идеи Дёберайнера в 1843 году развил другой немецкий химик Леопольд Гмелин, который показал, что взаимосвязь между свойствами элементов и их атомными массами значительно сложнее, чем триады Дёберайнера.
Француз де Шанкуртуа в 1862 предложил систематизацию химических элементов, основанную на закономерном изменении атомных масс — «земную спираль». Де Шанкуртуа был одним из первых учёных, отметивших периодичность свойств элементов; его винтовой график действительно фиксирует закономерные отношения между атомными массами элементов.
Таблица де Шанкуртуа (1862):

Химик Джон Ньюлендс в августе 1864 года составил таблицу, в которой расположил все известные элементы в порядке увеличения их атомных весов. Он, безусловно, первым дал ряд элементов, расположенных в порядке возрастания атомных масс, присвоил химическим элементам соответствующий порядковый номер и заметил систематическое соотношение между этим порядком и физико-химическими свойствами элементов. Но его таблица имела ряд недостатков (напр. в некоторых ячейках было по два элемента), поэтому была воспринята научным обществом скептически.
Таблица Ньюлендса:

В 1864 же году Уильям Одлинг опубликовал таблицу, в которой элементы были размещены согласно их атомным весам и сходству химических свойств, однако не сопроводил её какими-либо комментариями.
И в том же 1864 году опубликована книга Лотара Мейера «Die modernen Theorien der Chemie» (Современная Теория Химии), и его первая таблица из 28 элементов, размещённых в шесть столбцов согласно их валентностям. Мейер намеренно ограничил число элементов в таблице, чтобы подчеркнуть закономерное изменение атомной массы в рядах сходных элементов. Мейер указал, что если элементы располагаются в порядке их атомных весов, они попадают в группы, в которых подобные химические и физические свойства повторяются через определенные промежутки.
Ранняя версия таблицы Мейера (1862):
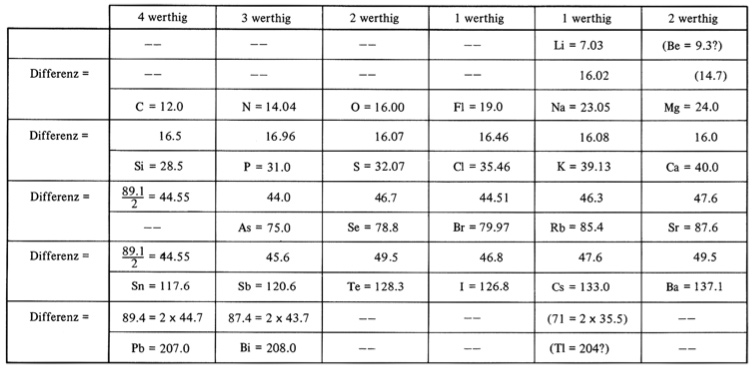
Доработанная версия таблицы (1870):

Через пять лет после Мейера, в 1969 году Менделеев опубликовал доклад, в котором сообщил об открытии им зависимости между атомными весами элементов и их химическими свойствами. В том же году он опубликовал «Основы химии», в которых был приведен первый вариант его таблицы, содержащей 19 горизонтальных рядов и 6 вертикальных. Таблица Менделеева весьма значительно отличались от той, которую Вы видели на уроках химии. На то время было известно только 63 элемента, из которых один — дидим — оказался смесью празеодима и неодима.
Первый вариант таблицы Менделеева (1869):

В 1870 году вышла работа Мейера, содержащая обновленную таблицу под названием «Природа элементов как функция их атомного веса», состоявшая из девяти вертикальных столбцов. Сходные элементы располагались в горизонтальных рядах таблицы; некоторые ячейки Мейер оставил незаполненными. Таблица сопровождалась графиком зависимости атомного объёма элемента от атомного веса, имеющий характерный пилообразный вид, прекрасно иллюстрирующий термин «периодичность».
В ноябре 1870 года Менделеев опубликовал статью «Естественная система элементов и применение её к указанию свойств неоткрытых элементов», в которой он впервые употребил термин «периодический закон» и указал на существование нескольких не открытых ещё элементов и предсказал их свойства (так же, как и у Мейера, таблица Менделеева имела незаполненные ячейки).
В 1871-м году Менделеев сформулировал закон как: «Свойства простых тел, а также формы и свойства соединений элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса».
В 1882 году Мейер и Менделеев одновременно получили медали от Royal Society (Королевского общества) за их исследования в области Периодического закона. Необходимо знать, что таблицы Мейера и Менделеева и в 1870-м, и в 1871-м, и в 1891-м годах все еще значительно отличались от привычной нам и по форме, и по содержанию: даже в 1891-м году, к примеру, там не было благородных газов.
Таблица элементов версии 1871 года:
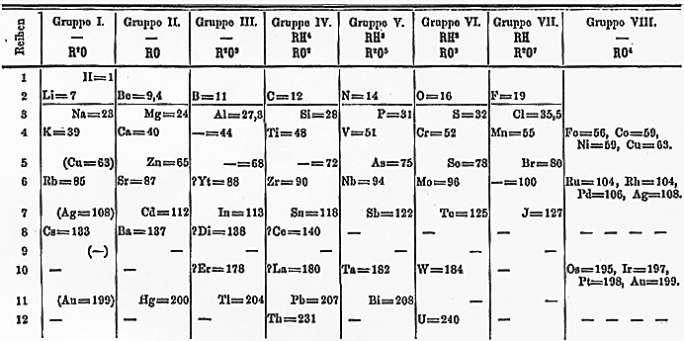
Доработанная таблица Менделеева, 1891 год, благородные газы все еще отсутствуют, зато есть дидим:

Еще одна версия таблицы 1891 года (напоминает таблицу де Шанкуртуа, не находите?):

Но самое главное заключается в том, что заблуждались и Мейер, и Менделеев. Современный закон звучит так: «Свойства простых веществ, а также формы и свойства соединений элементов находятся в периодической зависимости от ЗАРЯДА ЯДЕР атомов элементов». То есть не от атомного веса (массы), а от заряда ядер. Это в корне меняет всю суть закона. Ведь существуют изотопы — атомы одного элемента с одним зарядом ядер, практически одинаковыми химическими свойствами, но разной атомной массой (водород, дейтерий и тритий; уран 235 и уран 238 и т.п.).
Для того, чтобы прийти к этой формулировке Закона и современному виду Таблицы элементов, потребовались многие годы работы и исследования Рамзая, Браунера, Сведберга, Содди, Мозли и других ученых.
В 1911 году голландец Ван Дер Брук предположил совпадение атомного номера с величиной положительного заряда ядра атома, что стало основой современной классификации химических элементов. В 1920-м году англичанин Чедвик экспериментально подтвердил гипотезу Ван ден Брука; тем самым был раскрыт физический смысл порядкового номера элемента в Периодической системе, а закон приобрел современную формулировку (зависимость от заряда ядер).
И, наконец, в 1923 году Нильс Бор заложил основы современного представления о теории Периодического закона: причина периодичности свойств элементов заключается в периодическом повторении строения внешнего электронного уровня атома.
Нужно ли говорить, что на сегодня в Таблице присутствуют (существуют в природе и синтезированы) 118 химических элементов, в отличие от 63-х, известных во второй половине 19 века; а короткая версия Таблицы, которую вы видели в школе, официально отменена на международном уровне в 1989 году (хоть и продолжает приводиться в большом числе российских справочников и пособий и после этого времени). Кроме основного общепринятого вида таблицы, существует множество форм (иногда довольно вычурных), предложенных разными учеными.
Современная таблица:
Резюме: при всем уважении к Менделееву и его работам, он внес важный вклад, но был лишь одним из многих, приложивших руку к тому, что мы сегодня называем Периодическим законом и Периодической системой химических элементов. И да, в тех исследованиях Мейер его в общем-то опередил, хотя в 19 веке разница в пять лет считалась «практически одновременно» 🙂 Сравнив вид таблиц Менделеева и современной (и формулировки законов), становится понятно, почему во всем мире таблицу и закон называют просто Периодической таблицей элементов и Периодическим законом — из уважения к огромному труду большого количества ученых.
Если Вы дочитали до этого места — Вы молодец 🙂
Таблица Менделеева. Такая разная. : moris_levran — LiveJournal
1 марта 1869 года Менделеев закончил свою работу «Опыт системы элементов, основанной на их атомном весе и химическом сходстве». Этот день считается днём открытия периодического закона элементов Д.М. Менделеева. «Открытие Д.И. Менделеева относится к фундаментальным законам мироздания, таким как закон всемирного тяготения Ньютона или теория относительности Эйнштейна, а Д.М. Менделеев стоит в одном ряду с именами этих великих физиков». Академик А.И. Русанов.«Периодическая система как была, так и осталась в самых новейших решениях проблемы о веществе главной путеводной звездой». Проф. А. Н. Реформатский.
«Когда подходишь к оценке личностей, подобных Д. И. Менделееву, к анализу их научного творчества, невольно является желание отыскать в этом творчестве элементы, всего более отмеченные печатью гения. Из всех признаков, отличающих гениальность и ее проявление, два, кажется, являются наиболее показательными: это, во-первых, способность охватывать и объединять широкие области знания и, во-вторых, способность к резким скачкам мысли, к неожиданному сближению фактов и понятий, которые для обыкновенного смертного кажутся далеко стоящими друг от друга и ничем не связанными, по крайнем мере до того момента, когда такая связь будет обнаружена и доказана». Л. А. Чугаев, профессор химии.
Да и сам Менделеев понимал огромное значение открытого им закона для науки. И верил в его дальнейшее развитие. «По видимому, периодическому закону будущее не грозит разрушением, а только надстройки и развитие обещает». Д.И. Менделеев.
Первоначальный вид таблицы, написанный рукой Д.И. Менделеева.
Если бы все научные знания мира пропали бы, из-за какого либо катаклизма, то для возрождения цивилизации одним из главных законов стал бы периодический закон Д.И. Менделеева. Успехи атомной физики, включая ядерную энергетику и синтез искусственных элементов, стали возможными лишь благодаря Периодическому закону. В свою очередь, они расширили и углубили сущность закона Менделеева.
Периодический закон сыграл огромную роль в развитии химии и других естественных наук. Была открыта взаимная связь между всеми элементами, их физическими и химическими свойствами. Это поставило перед естествознанием научно-философскую проблемы огромной важности: эта взаимная связь должно получить объяснение.
Открытию периодического закона предшествовало 15 лет напряженной работы. Ко времени открытия периодического закона было известно 63 химических элемента, существовало около 50 различных классификаций. Большинство ученых сравнивали между собой только сходные по свойствам элементы, поэтому не смогли открыть закон. Менделеев же сравнивал между собой все, в том числе и несходные элементы. Менделеев выписал на карточки все известные сведения об открытых и изученных в то время химических элементах и их соединениях, расположил их в порядке возрастания их относительных атомных масс и всесторонне проанализировал всю эту совокупность, пытаясь найти в ней определенные закономерности. В результате напряженного творческого труда он обнаружил в этой цепочке отрезки, в которых свойства химических элементов и образованных ими веществ изменялись сходным образом – периодически – периоды. С развитием учения о строении электронной оболочки атомов стало ясно, почему свойства атомов показывают периодичность с возрастанием атомной массы. Атомы с одинаковой внешней сферой составляют одну группу. Атомы с одинаковым числом внешних сфер — составляют один ряд. Атомы с ядрами, имеющими одинаковые заряды, но разные массы, обладают одинаковыми химическими свойствами, но разными атомными весами и представляют собой изотопы одного и того же химического элемента. По существу свойства атомов отражают свойства внешних электронных оболочек, которые тесно связанны с законами квантовой физики.
Сама таблица Менделеева много раз трансформировалась, отображая разную информацию о свойствах атомов. Встречаются и курьёзные таблицы.
Так называемая короткопериодная или короткая форма ТМ 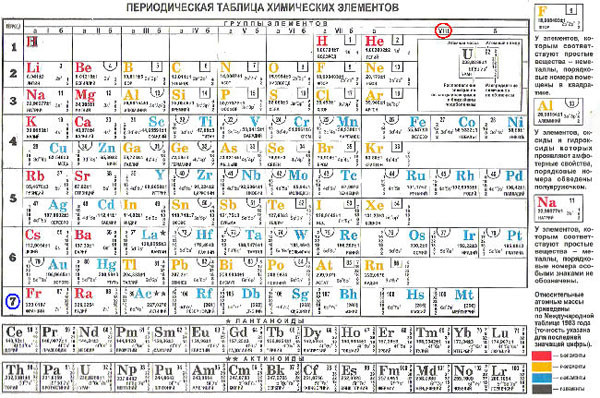

Длиннопериодная или длинная форма ТМ
Сверхдлинная.
Флаги государств, обозначающие страну, где впервые открыли данный элемент.
Названия элементов, которые были отменены или оказались ошибочными, как например, история с дидимом Di — оказался в дальнейшем смесью двух вновь открытых элементов празеодима и неодима.
Здесь синим цветом обозначены элементы, образованные во время Большого Взрыва, голубым — синтезированные во время первичного нуклеосинтеза, жёлтые и зелёные цвета обозначают элементы, синтезированные соответственно в недрах «малых» и «больших» звёзд. Розовым цветом — вещества (ядра), синтезируемые во время вспышек сверхновых звёзд. Кстати, золото (Au) ещё синтезируется во время столкновений нейтронных звёзд. Фиолетовые — созданные в лабораториях искусственно. Но это ещё не вся история… 
Здесь разными цветами обозначены органические, неорганические и незаменимые элементы, необходимые для построения тел живых существ, в том числе и нас. 




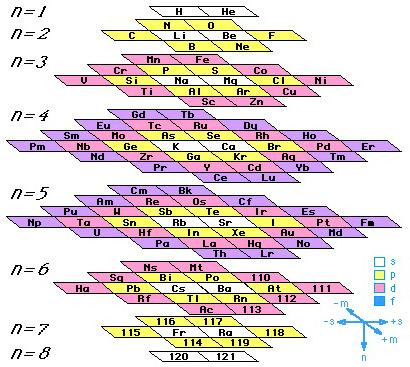
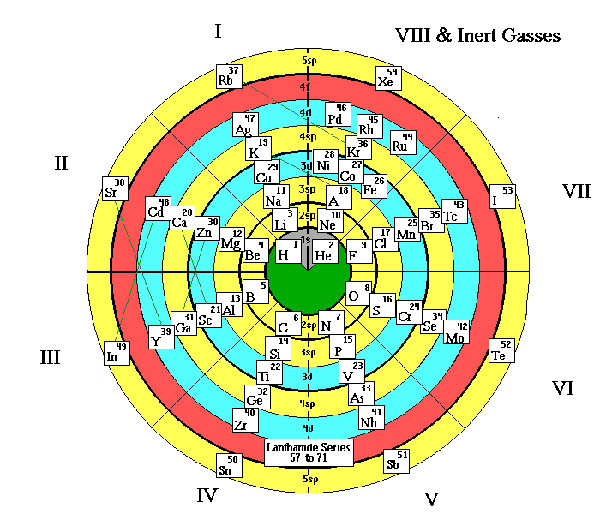

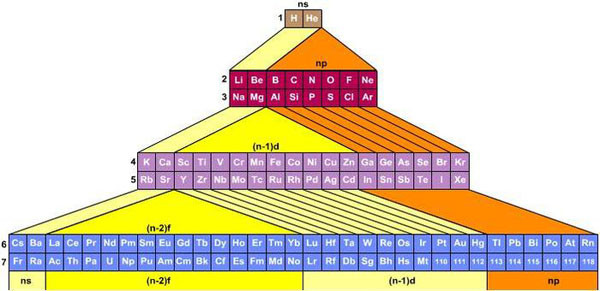
Таблица-башня
Предложена в 2006-ом Виталием Циммерманом на основе идей Чарльза Джанета. Он изучал орбитальное заполнение атомов — то, как располагаются электроны относительно ядра. И на основе этого разделил все элементы в четыре группы, рассортировав их по конфигурациям положения электронов. Таблица предельно проста и функциональна.



Таблица — спираль.
В 1964-ом Теодор Бенфей предложил поставить в центр таблицы водород (H), а прочие элементы разместить вокруг него по спирали, которая раскручивается по часовой стрелке. Уже на втором витке спираль вытягивается в петли, который соответствуют переходным металлам и лантаноидам с актиноидами, предусмотрено место для неизвестных пока суперактинидов. Это придает таблице вид экстравагантного дизайнерского решения.
Таблица — радужная спираль.
Изобретена в 1975 химиком Джеймсом Хайдом. Он увлекался кремнийорганическими соединениями, поэтому в основание таблицы попал именно кремень, так как у него большое число связей с другими элементами. Различные категории элементов так же объединены по секторам и отмечены нужным цветом. Таблица красивее аналогов, но из-за криволинейной формы пользоваться ею непросто.



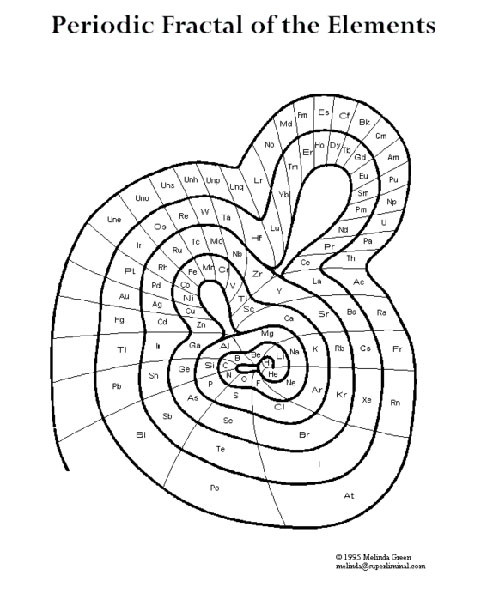


Эти таблицы отображают последовательность заполнения электронных оболочек. Во всяком случае некоторые из них. Все эти таблицы выглядят весьма экзотично.
Таблица изотопов. Здесь отображено время «жизни» различных изотопов, их стабильность в зависимости от массы ядра. Впрочем, это уже не таблица Менделеева, это совсем другая (ядерная физика) история…
С таблицей Менделеева по жизни / Хабр
2019 год провозглашен Генеральной ассамблеей ООН (A/RES/72/228) и одобрен Генеральной конференцией ЮНЕСКО (39 C/60) Международным годом Периодической таблицы химических элементов в честь 150-летия открытия Периодического закона химических элементов Д.И. Менделеевым. В 1869 году Д.И. Менделеев впервые опубликовал свою первую схему Периодической таблицы в статье «Соотношение свойств с атомным весом элементов» в журнале Русского химического общества.
Как ни прискорбно осознавать, но для абсолютного большинства людей, знакомство с периодической системой элементов Д.И.Менделеева (и одноименной таблицей) начинается, и как правило, заканчивается в средней школе (
Еще с далеких школьных лет как-то так повелось, что для меня по важности таблица Менделеева находилась на одном уровне с таблицей умножения. Связно это, я так подозреваю, с довольно успешным участием в химических олимпиадах. Припоминается, как часто во время совместных посиделок, друзья проверяли меня «на вшивость», спрашивая атомную массу первого пришедшего в голову элемента. А так как в голову среднестатистическому (т.е. далекому от химической науки) школьнику, в лучшем случае, приходило максимум 10-15 названий распространенных элементов, то выучить их атомные массы, при условии практически постоянного решения олимпиадных рассчетных задач, было под силу наверное абсолютно любому. Я же не считал способность запомнить атомные массы основных элементов (макро-) чем-то из ряда вон, еще и потому, что на т.н. hi-level олимпиадах (вроде республиканской) встречал людей которые помимо того, что знали атомные массы всех лантаноидов/актиноидов, так еще и могли эти массы назвать с точностью до третьего знака после запятой.
Лирическое отступление про аналоговые таблицы периодической системы Менделеева
На визитках, ввиду их малого размера, крайне тяжело разместить максимальную информацию. Опытным путем установлено, что лучший вариант для печати (масштабируемый) — это оригинальная IUPAC таблица. Лаконичность и читаемость. IUPAC = Международный Союз по теоретической и прикладной химии, своеобразный «законодатель мод» в мировой химической науке.
Пример для подражанияПолучаются примерно вот такие визитки, при необходимости кое-какие данные можно выбросить (например название, если химического образования достаточно, чтобы ориентироваться в символах, хотя признаться, я тоже иногда путаю названия актиноидов, особенно недавно открытых). Для тех, кто захочет повторить — я сделал прозрачную минималистичную PNG-шку.
Помимо визиток иногда нужна «ручная» аналоговая таблица, которую можно к примеру распечатать форматом А2 и уложить на стол/стену и т.п. Ниже представлены именно такие, максимально информативные варианты (сугубо ИМХО, принимаю дополнения).
Как часто говорила моя любимая учительница химии, Лилия Халиловна Полуян «химию выучить нельзя, химию надо чувствовать… понимать». Вот и предложенные ниже картинки, на мой взгляд, способствуют именно понимаю, что химия — это не абстрактные задачи, стакан с синей жидкостью и фокусы с жидким азотом в каком-нибудь очередном музее науки, а вполне себе вещь из реальной жизни, с которой каждый из нас сталкивается по несколько раз на день. Предложенные ниже варианты, помимо привязки к реальной жизни, еще и английский выучить помогут.
Отличный вариант для продвинутых школ и даже детских садовТаблица Менделеева в картинках (для визуалов)Таблица Менделеева в словах (для аудиалов)
Что касается «взрослых» вариантов таблиц, то они приведены ниже. Во время отсутствия достаточно мощных носимых устройств (PDA) или же необходимого софта, так сказать, paper-ready таблица была основным источником информации (даже на фотоаппарате в виде масштабируемой картинки доводилось носить с собой). Под спойлером — именно такой, «проверенный в полях», вариант.Любимая бумажная таблица МенделееваЛицевая сторона
Оборотная сторона с кристаллографией
Отдельного упоминания заслуживают изотопы. Как правило, в условиях «традиционной» таблицы периодической системы, места для размещения информации об изотопах катастрофически не хватает. Ну и вообще, ценится информация про изотопы (~ в 0.99$ — смотреть ниже). Поэтому изотопы чаще идут отдельным листом. В качестве отличного примера может выступать таблица изотопов от IUPAC (IPTEI 2018 год). Под спойлером приведена кликабельная картинка более ранней чем IPTEI версии, но разница будет заметна только узким специалистам 🙂IPTEI для печати
Per aspera ad astra. Тернистый путь от аналога к цифре
На Хабре периодически всплывают статьи, посвященные «персональной эволюции» пользовательских устройств на примере конктерного автора. Чаще всего обозревается железо, иногда особенности ПО. Я тоже хочу рассказать об эволюции своего зоопарка карманных компьютеров, но через профессиональную призму — призму химика и связанного с этим основного инструмента — таблицы периодической системы элементов Д.И. Менделеева. Часто для проверки устройств на совместимость с конкретным человеком, человек этот пытается запустить на устройстве то windows 3.11, то Doom II. Ваш покорный слуга — пытается запускать таблицу Менделеева.
Не скажу, что здесь есть какая-то оригинальность. Логично, что при освоении новой для себя области, человек первым делом пытается перенести в нее привычные вещи. А что может быть привычнее для любого нормального химика, чем родненькая табличка :). Мне подтверждением служил тот факт, что в то время когда я занимался поиском очередного мобильного ассистента, мой дорогой друг Сережа (c Днем Рождения тебя, кстати, как прочитаешь!) aka navanax cо своим удаленным российским коллегой Johnny_B писал на ассемблере… конечно же таблицу Менделеева (period) для миниатюрной KolibriOS (на Хабре есть даже аутентичный блог от KolibriOS Project Team).
Итак, продолжим наш разговор, и вернемся к PDA. Как и у многих из поколения 80-90хх первым моим PDA/КПК cтал Palm — черно-белая модель m125 на двух АА-батарейках. Cчитай, дорогой читатель, что «синдром утенка», но вот как открою фотографии этой «ладошки» — такой теплотой заливает, как все равно у любимого деда остался на выходные ночевать…Что за синдром такой ?
Синдром утёнка — принцип в поведении и психологии, когда человек, увидев что-то в первый раз, считает его самым лучшим, удобным и приятным. Чем меньше что-то похоже на первую любовь, тем хуже воспринимается. Синонимичен ему термин импринтинг (запечатление), который был зафиксирован и открыт ученым Конрадом Лоренцом.
Возможно мнение мое отдает субъективностью, но с тех пор я не встречал платформ, на которых был бы настолько эргономичный и удобный софт. В случае Palm это было приложение ChemTable v2.32, ставшее для меня на долгие годы образцом для подражания, применимым к периодическим таблицам элементов.
Особенно из плюсов хотелось бы отметить, помимо обширной, если не исчерпывающей справочной информации, еще и возможность поправлять данные/вносить свои позиции. Здесь даже имеется подробная инструкция, такое приложение не устареет никогда.
Отдельно мне, как воспитаннику кафедры радиохимии, нравилось то, что в ChemTable были указаны изотопы и их соотношение в земной коре. Как-то само собой я стал использовать эту характеристику как индикатор качества периодической таблицы Менделеева. Сравнительный анализ бесплатных/PRO версий многих сабжевых приложений показывает, что таким индикатором пользуюсь не только я. Кстати…
Неспокойно на душе и поэтому…чистосердечно признаюсь, у меня есть эмулятор Palm. Это приложение PHEM Palm Hardware Emulator от компании Perpendox Software. По-сути, это порт линуксового POSE (dlinyj кстати на его примере учил хабра-людей программировать под Palm). Как и старший брат, андроид-эмулятор поддерживает сеть, карту памяти, граффити. Просто устанавливаем приложение на андроид-устройство, в storage/emulated/0/phem/roms закидываем образ ROM (образ прошивки) нужного нам Palm-а (вот здесь можно найти образ от легендарного Palm m100 (свой m125 я нашел здесь). Скины (они же Skins, они же «внешний вид оригинального КПК» можно взять из POSE. Ложим в storage/emulated/0/phem/romsУстановка любых программ происходит через меню программы (читать «эмулирует HotSync»). Выбираем папку на смартфоне где лежат нужные *.prc и отдаемся во власть воспоминаний…
Следующим моим минималистичным PDA (а основное требование у меня как правило было далеко не наличие wifi и сочного цветного экрана, а энергосбережение — максимальное время работы + легко заменяемые аккумуляторы) стал легендарный Casio PV-S450 (американский вариант PV-400plus без jog-dial колесика).Для тех кто забыл, напоминаю, как выглядит…
Софта для карманных компьютеров Casio изначально было немного, но удивительно, как и в случае Palm m100 4 мб родной памяти хватало для большинства задач. Были заметки, неплохой калькулятор, таблица Менделеева, читалка книг и программа для работы с базами данных в формате CSV. Было хранение всех данных во флэш-памяти (т.е. данные НЕ пропадали вслед за разрядом аккумулятора — сегодня тяжело поверить, что такое вообще возможно), приятная голубая подсветка и работа от батареек ААА (какие-то дикие по сегодняшним меркам цифры работы от одного комплекта батарей на протяжении месяцев (!)). Ну и помимо всего прочего, Pocket Viewer-ы — серия бесклавиатурных PDA, которая работала на основе архитектуры x86. Знаю, есть спецы, которые мне могут припомнить шедевральную Nokia 9110, которая работала на встроенном AMD 486 процессоре частотой 33 Мгц. Но то, то была клавиатурная модель.Исторический пруф
Ладно, немного я отклонился от темы своего повествования. Итак, в Casio PV была в наличии собственная периодическая таблица, с незамысловатым названием Periodic. Умела показать ряд/период, атомную массу, энергию ионизации, электронную конфигурацию. Простенько и ничего лишнего. Но учитывая обильность ПО для этой платформы — требовать чего-то иного было бы глупо. Необходимую дополнительную информацию я носил в виде CSV-файла (те самые изотопы, упомянутые в начале повествования). На картинке ниже — показан реальный внешний вид Periodic.
Благодарность: хотелось бы отдельную благодарность выразить жене за старательность и умение, позволившее сфотографировать белочку (прим. мое — картинку локализатора PVOS), которая появляется на экране на считанные доли секунды. Сам, сколько не пытался, так и не смог поймать, видимо в женщине с рождения заложено это чутье/сродство к маленьким животным.
Хотелось бы отметить, что так как в выборе устройств-компаньонов, я чаще всего исходил из соображений экономичности, не удивительно, что PocketPC/WinMobile системы как-то не тронули мое сердце (хотя был, был iPAQ h3210 с двумя типами карт, правда продал я его достаточно быстро — так что, если кто-то расскажет про лучшую для Windows Mobile таблицу Менделеева — с радостью дополню статью) и я плавненько с Palm перескочил на, с позволения сказать, EPOC смартфоны от Nokia — легендарные 9300/9500. Единственный недостаток этих телефонов — отсутствие подсветки клавиатуры. Клавиатура имхо — на 98% близка к идеалу, на 100% идеал — клавиатура старшего брата этих смартфончиков — PSION Series 5MX. Аппаратные отличия между 9300 и 9500 для меня оказались не критичны, носил 9300, потому что меньше и эргономичнее.
Так вот, в случае Symbian Series 80 существовала одна единственная версия таблицы Менделеева. Это Periodic Table 1.03 от финского программиста Sami Vuori. Плотно поработав с приложением я обнаружил в нем несколько недочетов и ошибок, рассудил, что программист-создатель уже наверное давно плюнул на это дело, взял и написал ему с просьбой поделиться исходниками. В итоге мы с фином начали тесно общаться, и под конец уже забыли про эту утилиту. Sami оказался отличным парнем. Дружим до сих пор. Но приложение его работало до тех пор, пока работал мой 9300i.
За безвременно «уставшим» 9300i пошли клавиатурные Nokia E53 и E90 с S60.3 на борту. Здесь, к сожалению, выбор был невелик. Пусть комментаторы, если что поправят, но для Series 60 не было адекватной таблицы Менделеева (только достаточно слабые поделки в виде java-мидлетов). Поэтому, поэтому пришлось вернуться к аналоговым таблицам и носить с собой картинки. Благо мощности смартфонов Nokia без проблем позволяли легко масштабировать рисунок и находить нужную информацию.
После утраты своей рабочей Series 60 Nokia E53 я перешел сразу на финальный вариант — «последний из магикан»/«лучший смартфон Nokia» — Nokia 808 PureView (+Symbian Belle FP2), которым, кстати, с удовольствием пользуюсь и сейчас. Подозреваю, перейду я с него на что-то другое только либо в случае серьезного повреждения, либо в случае отказа сотовых операторов от диапазона частот доступных для данного телефона. Как камера и звонилка — идеальный вариант. Никаких там обновлений, длительное время работы, и в принципе, весь джентельменский набор программ (а в нем, помимо таблицы Менделеева, есть даже весьма функциональный OBD-сканер для авто).
Для Symbian Belle несмотря на ее «платиновый» (по уровню доведенности до ума) статус, существует не так много таблиц Менделеева. На мой субъективный химический взгляд наиболее красивой и удобной для Symbian S^3/S^5 является программа Periodic Table v 1.3 от компании Naveen CS. Запас данных стандартный, из бонусов — графическое отображение электронной конфигурации, список всех элементов, возможность сравнить два элемента, ссылка на страницу Википедии, посвященную элементу. Работает шустро, правда списка изотопов — нет.
Как я установил для себя еще с университетской скамьи, телефон должен звонить, а карманный комьютер — помогать (ибо КПК, англ. Personal Digital Assistant, PDA — «личный цифровой помощник»). Поэтому любой современный Android-смартфон, без SIM-карты выступает в роли отличного PDA (даже с точки зрения времени работы от батареи). Пусть подход и достаточно ортодоксальный, но в моем случае он еще и максимально комфортный (из-за разделения объектов в пространстве можно не бояться, что пропустишь важный звонок из-за разрядившейся благодаря wifi батареи).
Так вот, было бы удивительно, если бы при невероятной популярности Android-устройств для них не было качественных таблиц Менделеева. Такие таблицы конечно же есть, правда одновременно с ними сосуществует огромное количество приложений, где собственно таблица выступает лишь в качестве приятного дополнения. Достаточно написать в плэймаркете волшебные ключевые слова («таблица менделеева») и вот уже вам предлагают скачать 100500 различных приложений. Очень много приложений уровня «для детей», такое впечатление, что разработчики подразумевают, что «взрослый информацию и так найдет… в книгах». Поэтому поиск адекватной, «взрослой» периодической системы это целый НИОКР. Ну и помимо уже упомянутой инфантилизации, такое впечатление, что люди часто забывают зачем таблица нужна. Там может быть внутри что угодно, от видео, на котором показано, как горит какой-то элемент в среде фтора, до решений школьных задач за 6-7-9 классы и т.п. Все что можно, за исключением того, что нужно. Поэтому я, раз уж появился повод, обращаюсь к программистам, которые берутся за естественно-научные проекты, не имея должного профессионального фундамента. Ребята, не экономьте на научных консультантах! (стучите в facebook если что ;))
На «народном» 4PDA почему-то в каталоге программ Android нет ссылок на нормальный софт, зато опять есть эти вездесущие «детские приложения». Elements, Periodic Table , Таблица Менделеева — имхо никакой критики не выдерживают и серьезно отстают от описанных ниже приложений. Единственное, что по духу и наполнению они все близки к Periodic от моего Casio PV-S400+ 🙂
В общем, учитывая все выше изложенное, рискну озвучить своих фаворитов среди сонма таблиц Менделеева для Android и, если вдруг я что-то (какое-то невероятное приложение) упустил, то с удовольствием выслушаю в комментариях дополнения и подправлю статью. От лирики переходим к тройке лидеров.
Приложение первое Periodic Table от Royal Society of Chemistry. Проходит «изотопный тест», на каждый изотоп имеется своя «карточка», где указаны даже типы распада.
Приложение второе Merck PTE от Merck KGaA. Проходит «изотопный тест», содержание изотопов указано в стиле Palm ChemTable ([изотоп]-[массовая доля]). Хотя в целом таблица более информативна (чего стоит сортировка и поиск нужного элемента по десятку параметров). Ну и покрасивее, Merck все-таки…
Упомянутые выше программы абсолютно бесплатны, единственное, что может кого-то (скорее всего школяров, а не профессиональных химиков) смутить — отсутствие русского языка. Если ж все-таки язык критичен — то вашему вниманию третье приложение — Таблица Менделеева 2019 PRO — Химия стоимостью «всего за 0.99$». Есть и бесплатная light версия — Таблица Менделеева 2019 — Химия.
Интересно, что основное отличие Pro от light именно в наличии информации об изотопах (т.е. бесплатная версия «изотопный тест» не проходит, но из-за небольшой стоимости программы я решил закрыть на это глаза). Вообще заметил интересную особенность русскоязычных программ — все пытаются изотопы продать за деньги 🙂
В общем, таблица сделана достаточно красиво, чего стоит анимированная электронная конфигурация. Плюс есть неоспоримые преимущества в виде, например, эмиссионного спектра излучения (такого я в других PDA-шных таблицах не встречал).
Честно говоря, некоторое время колебался, а не заплатить ли автору мизерные 0.99$. Но потом успокоился и решил, что анимация и русский язык в таблице менделеева конечно хорошо, но лучше уж я как-нибудь по-старинке, без эмисионного спектра излучения обойдусь. Как пела в годы моего студенчества певица Таня Терешина «Не пытайся купить то, что я и так отдам тебе даром…«.
Ну и… Честно говоря, закидайте меня помидорами, но я больше доверяю компании Merck (не говоря уж про Royal Society of Chemistry), которые известны не только своими научными достижениями, но и прекрасными базами данных (Merck Database у меня до сих пор где-то на cd-rom валяется). В этом плане некая «широко известная в узких кругах» компания August Software выглядит, конечно, послабее. Но отзывы на PlayMarket сугубо положительные (вопрос, от кого).
На сим закругляюсь, я постарался в статье честно расказать про свой опыт общения с бумажными и цифровыми периодическими таблицами Д.И. Менделеева. Вещи описанные в статье, в прямом смысле выстраданы и проверены в жестких полевых «во время халтур» условиях, а значит — я могу смело их рекомендовать 🙂 Выбирать вам, и надеюсь, мои замечания окажуться полезными. И еще раз…
Дополнение: ну и конечно же таблица Менделеева активно эксплуатируется на ПК. Лучшей, на мой взгляд, вариацией для нетбуков/ноутбуков/планшетов/ПК на Windows я считаю приложение PL Table от Константина Полякова. Правда автор, видимо, забросил свое детище, так как на оф.сайте можно найти все что угодно, кроме самой таблицы. Но как всегда — поможет Google.
Внешний вид PL Table 4.5Интересный и достаточно подробный (боюсь без проверки употреблять слово «исчерпывающий») web-вариант таблицы предложил пользовател Bov87 Динамическая таблица Менделеева — Ptable
И завершает мой импровизированный рейтинг «настольных» таблиц, вариант для unix-систем, который называется Kalzium (KDE). Отличное приложение, с массой справочной информации и красивой графической реализацией. Как говорится, ищите в репозиторияхKalzium живьем
p.s. тут внезапно @andrei.raiski, которого я очень ценю и уважаю за его химические советы (и не только, именно этот человек привел меня к мысли «а мне нужен персональный компьютер») в очередной раз удивил. Очень милая миниатюрная таблица Менделеева с кусочками
Важно! Все обновления и промежуточные заметки из которых потом плавно формируются хабра-статьи теперь можно увидеть в моем телеграм-канале lab66. Подписывайтесь, чтобы не ожидать очередную статью, а сразу быть в курсе всех изысканий 🙂
ТОП-25 рекомендаций по быстрому и легкому изучению таблицы Менделеева!
Привет моим умным читателям! Недавно Таня из Ростова поделилась со мной информацией о том, что хочет пойти учиться на медика.
Девочка скоро заканчивает школу и усиленно готовится к поступлению.
Одним из самых сложных для нее моментов является периодическая система химический элементов Д. И. Менделеева. И она попросила меня помочь ей в этом.
Действительно, на первый взгляд таблица Менделеева кажется огромной и очень сложной для запоминания. Но если вникнуть во все тонкости и понять ее, а также выучить основные элементы, трудностей в дальнейшем не будет.
Тем, кто как и Таня, хочет быстро и легко понимать данную таблицу, можно прочитать мою статью.
Если материал будет интересен и полезен для вас и ваших друзей, пожалуйста, делайте репосты, а также пишите комментарии и ставьте лайки.
Вступление или С чего начать?
Почему надо учить именно таблицу Менделеева? Ведь есть множество другой информации, которая мне намного нужнее.
- Первая причина: Навыка запоминания еще нет. А потому процесс запоминания будет происходить медленно (вы же ходить не сразу научились, ведь так?), а нужную информацию обычно нужно запомнить быстро. В результате, вы скорее всего будете себя подгонять, из-за чего результат вас разочарует, и вы продолжите пользоваться старыми добрыми методами, окрестив все это фигней и лишней тратой времени.
- Вторая причина: ведь на чем-то тренироваться нужно, а таблица является прекрасным тренажером, освоив который вы приобретете навыки запоминания точной (числовой), абстрактной, буквенной и табличной информации (как раз той, что вызывает множество проблем при запоминании). Вы разовьете свое воображение, гибкость мышления и вообще хорошенько вкачаете мускул памяти. А выполняя упражнения, ко всему прочему научитесь не только запоминать, но и доставать из памяти на свет божий нужную вам информацию.
- Третья причина: развитие уверенности в своих силах, веры в свою память и умственные способности. Ведь если вы знаете наизусть таблицу Менделеева, то сможете выучить любую другую таблицу, сколь бы сложной она не была. Ну, и конечно же, вы всегда сможете похвастаться перед друзьями, что можете без труда назвать любой элемент таблицы по его номеру, названию, атомной массе, или же написать ее всю за каких-то десять минут.
Многие скажут: «Это невозможно!». Спешу их разочаровать. Это возможно и совершенно не сложно, а даже весело и приятно, хотите верьте, хотите нет, а лучше проверьте.
Но сразу хочу предупредить, что никакого волшебного метода, магических слов или мантр, напевая которые, вы мгновенно все запомните, нет. Запоминание — это навык. И как любой другой навык он требует времени и усилий на его приобретение. Так что не пугайтесь, если сначала запоминаться все будет медленно и со скрипом. Помните: что тренируется, то развивается.
Ассоциации
Так каким же способом мы будем ее запоминать? Не зубрить же ее в самом деле?
Конечно нет. Мы будем использовать мнемонику (искусство запоминания), изобретенную еще древними греками. Строится она на ассоциативном мышлении. Ассоциация — это связь. Наш мозг мыслит ассоциативно: незнакомые понятия он связывает со знакомыми, образуя целые сети разнообразных связей.
Я обещал, что не буду вдаваться в теотеризирование, но алгоритм построения ассоциаций не могу не привести:
- Представьте каждый образ отдельно как можно ярче.
- Соедините их вместе в движении.
- Связь должна быть парадоксальной, смешной и т.д. (см. ниже)
Желательно, чтобы ваша связь включала в себя следующие элементы:
Теперь давайте немного попрактикуемся и проассоциируем два простых слова: СВИНЬЯ и СИГАРА.
Итак, сначала представили себе свинью, жирную такую, морда в грязи. Почувствовали запах от нее исходящий, потрогали ее кожу. Теперь так же с сигарой: представьте, повертите ее в руках, понюхайте.
А теперь нам нужно эти два образа соединить. Простой образ свиньи и рядом лежащей сигареты очень быстро выветрится из нашей памяти, и следа не останется. Давайте попробуем совместить их парадоксально, например, свинья, развалившись в вашем любимом кресле, с наслаждением курит сигару и посматривает на вас с явным превосходством, вроде как не вы гомо сапиенс, а она — венец эволюции. Она чего-то вам хрюкает, но вы не можете ничего понять. И вообще, какого черта эта свинья делает в моем кресле! Почувствуйте негодование, ощутите запах сигары и свиньи.
Представили? Глупо, нереально, ведь свиньи не курят сигары, но ведь забавно.
Или так, садистский вариант: вы курите сигару (представьте все ощущения) и почему-то решили затушить ее о свою любимую свинью. Вы с яростью тушите ее о мягкое место свиньи, та визжит и убегает.
Неправильных ассоциаций не бывает. Каждый человек уникален, и мыслит совершенно не так, как все остальные шесть миллиардов (в этом легко убедиться, выполнив упражнение, которое я, возможно, опубликую позже).
Упражнение
К каждой паре слов придумайте минимум по три «картинки», как мы это сделали выше.
Постарайтесь, чтобы ваши картинки были уникальными, смешными и запоминающимися. Сделали? А теперь скажите, какое слово было в паре у слов: диван, обои и зеркало? Если ассоциации были яркими, то вы без труда назовете второе слово в паре.
Видите, какой славный бонус. Запоминать и не пытались, а запомнили! И мы подходим к очень важному теоретическому тезису: память — это побочный эффект мышления. Следовательно, если вы мыслите эффективно, но и запоминаться будет все само собой. Вот развитием этого самого мышления мы и будем заниматься.
Обзор Таблицы
Ну что ж, теперь у нас в руках есть все (почти все), что нужно для того, чтобы запомнить эту громадину. Но нам еще понадобится план.
Давайте взглянем на таблицу: элементы в ней не просто так валяются, а упорядочены по периодам, группа, рядам и порядковым номерам. С какого же бока к ней подступиться?
Можно начинать учить в лоб, по порядку, начиная с первого номера и заканчивая последним, но для нас это будет пока слишком сложно из-за обилия числой информации. Мы же будем изучать ее по рядам. А чтобы запомнить, какой ряд за каким следует, мы сначала запомним последовательность первых элементов каждого ряда, а именно:
Данную последовательность мы будем называть «вертикалью». Затем, каждый элемент вертикали мы будем дополнять остальными элементами в ряду, строя горизонталь. Для того, чтобы запомнить вертикаль, нам нужно сначала создать фон, на который мы запишем название элементов.
Создание фона
Существуют следующие три главных мнемонических принципа:
- Ассоциации.
- Образ.
- Локализация (фон).
С первыми двумя мы уже познакомились, а вот на третьем остановимся подробнее.
Давайте представим запоминание как процесс письма. Для того чтобы что-то зафиксировать нам нужна ручка и бумага. Ручкой в данном случае является метод создания ассоциативных картин, а бумагой — фон. Вряд ли у нас получится законспектировать лекцию, водя ручкой не по бумаге, а по воздуху. Точно также у нас вряд ли получиться надолго запомнить картинки, плавающие в вакууме.
Самые два популярных метода создания фона это метод Цицерона и метод Опорных Образов. С методом Цицерона мы познакомимся немного позже в других статьях, а сейчас давайте создадим свой первый опорный список из десяти элементов, на которые затем и «запишем» вертикаль.
Возьмите лист бумаги и нарисуйте на ней цифру 1. Теперь внимательно посмотрите на нее, повертите лист, поприближайте, поудаляйте. Что она вам напоминает? Может быть это столб, или гвоздь, или флаг? Выберите образ, который вам полюбился больше всего. Проделайте то же самое с остальными цифрами.
Ну, вот и все. Ваш опорный список готов. Вот, что получилось у меня:
Теперь пробегитесь по образам считая от нуля до девяти и обратно. А теперь вразброс: 9, 4, 7, 1, 3, 8, 2, 0. Ну как? Получается?
Внимание! Прежде чем записывать информацию на опорный список, нужно его выучить так, чтобы он стал неотъемлемой частью вас самих. Как таблица умножения, например.Запоминаем вертикаль
Итак, у нас десять элементов и десять опорных образов. Кроме того, вспомнив опорный образ, мы тут же автоматически вспомним номер ряда. Удобно, не правда ли?
Нам остался последний шаг: каким-то образом представить совершенно абстрактые для нас существительные. Например, название элемента Литий у меня не вызывает никаких конкретных образов. Его сложно представить, потому что я никогда в жизни его не видел, ведь так? Как же быть?
Мы будем пользоваться методом звуковых ассоциаций или попросту говоря, к каждому названию элемента мы будем подбирать созвучное слово, которое очень просто представить.
Например:
Водород — вода.
Теперь нам есть, что представить. Представляем воду, бескрайнее море и блики солнца на его поверхности. А вслух произнесите, удерживая образ воды, слово водород. Поехали дальше.
Литий — литье (для автомобилистов) или лист, например.
С остальными элементами попробуйте проделать те же действия самостоятельно.
Отлично! Вот теперь мы с вами можем переходить к запоминанию вертикали. Для этого мы будем ассоциативно связывать образ опорного списка и образ, символизирующий элемент, следуя всем указаниям, данных выше.
1 — водород.
Гвоздь — вода.
Представляем, что поливаем гвоздь, и тот начинает расти у нас на глазах, пуская словно ветви из себя другие гвозди. Привлеките все чувства, представляя эту картину. Вслух произносим название элемента: водород.
2 — литий.
Лебедь — литье.
Представляем, как лебедь жалуется вам, что, мол, литье совсем износилось, и показывает вам свои лапы, и вы с удивлением отмечаете, что вместо лап у него колеса с ужасно изношенным литьем. Вы сочувственно качаете головой, а вслух произносите: «Литий».
Далее, самостоятельно. Ну, как? Получилось? Конечно получилось! Что ж, примите мои поздравления!
Теперь давайте проверим. Вспомните по порядку всю вертикаль, считая от 1 до 10 (0 заменяет нам число 10). Если озвучить, выглядит это примерно так: так, один, ага, гвоздь, я его поливал водой, водород. Вслух произносим только название элемента.
А теперь вразброс:Назовите первый элемент 4-го ряда, а теперь 9-го, 2-го, 7-го, 3-го.
Резюме
Мы с вами:
- познакомились с ассоциативным мышлением и научились использовать его в целях запоминания.
- создали свой первый опорный список и записали на него первую группу таблицы.
- научились преобразовывать абстрактную информацию в конретные образы с помощью созвучных слов.
Дальше — интереснее!
Как выучить таблицу Менделеева? С этой проблемой рано или поздно вынужден столкнуться каждый школьник. К счастью, задача кажется сложной лишь на первый взгляд. Простые техники запоминания, описанные в статье, помогут быстро и легко справиться с ней.
Полезные советы
Ни для кого не секрет, что повторение – мать учения. Как выучить таблицу Менделеева, если ученик не возвращается к ней снова и снова? Обязательно следует распечатать материал и везде носить его с собой. Повторять элементы необходимо каждый раз, когда возникает свободное время (в очереди, в транспорте, на перемене).
Еще более эффективный вариант – создание копии таблицы вручную. Этот способ идеален для школьников, у которых наиболее развита кинестетическая (мышечная) память. Во время переписывания таблицы можно не только выучить некоторые элементы, но и лучше понять ее устройство, что также способствует эффективному запоминанию.
Не стоит ставить недостижимые цели, выучить всю таблицу за день невозможно. Вполне достаточно запоминать несколько элементов в сутки, а затем повторять те, что были изучены ранее.
Игры
Как выучить таблицу Менделеева? Для лучшего запоминания можно подключить ассоциативное мышление. Для каждого элемента необходимо сочинить небольшую историю, причем вовсе не обязательно делать ее серьезной. Не исключено, что смешной рассказ быстрее отложится в памяти. К примеру, Аргентина получила свое название в честь аргентума (серебра), так как первопоселенцы обнаружили много серебра на этой земле.
Не стоит тратить время, сочиняя истории для запоминания простых элементов. С большой вероятностью в памяти уже и так присутствует информация о том, что водород – это H. Лучше сосредоточиться на том, что кажется наиболее сложным.
Картинки
Как выучить таблицу Менделеева, если не помогают способы, описанные выше? На помощь придут картинки, на которых изображены предметы, часто встречающися в повседневной жизни. Каждый элемент, который необходимо зафиксировать в памяти, должен ассоциироваться с тем или иным рисунком.
Вовсе не обязательно тратить время на рисование картинок. Как быстро выучить таблицу Менделеева? Необходимо распечатать карточки со всеми элементами или создать их вручную, а затем каждый лист прикрепить к конкретному предмету в доме. Скажем, можно «назвать» стол водородом, представить себе, как он превращается в водородную бомбу и взрывается. Также можно вообразить, что у холодильника есть нос, который позволяет ему дышать (кислород). Главное, чтобы образы были яркими и не оказались чересчур сложными.
Разделение таблицы
Как быстро выучить таблицу Менделеева? Опытные педагоги советуют собственноручно разделить ее на части. Многие таблицы уже разбиты на категории, которые включают в себя разные виды элементов. Как правило, такие категории обозначаются различными цветами. Однако школьник может создать удобный для запоминания шаблон собственными силами, так материал лучше отложится в памяти.
К примеру, можно скомпоновать элементы по тяжести, расположить их, двигаясь от простейших к сложным. Можно также учить таблицу по столбцам или строкам. Главное, чтобы пользоваться новым шаблоном было комфортно.
Современный метод
Таблица Менделеева, фото которой можно увидеть в этой статье, легко отложится в памяти, если обратиться к специальным флеш-играм. Созданы программы, которые способствуют запоминанию элементов в игровой форме. Флеш-игры подразумевают поиски элементов по буквенному обозначению, названию, массе. Интересно, что игрок может работать не только со всей таблицей, но и с одной из ее частей. Таймер, усложняющий задачу, используется по желанию.
Баллада о магнии
Как запомнить таблицу Менделеева? Почему бы не написать небольшую песню, посвященную ей?! Натрий, кальций, рубидий – рифмы к названиям элементов подбираются очень легко. Кстати, можно не только сочинить балладу, облегчающую запоминание, но и найти подходящий вариант в глобальной сети. Очевидно, что от песни всегда можно отказаться в пользу стихотворения, если его написание кажется более легкой задачей.
Маленькие хитрости
Таблица Менделеева включает в себя более сотни элементов, поэтому приступать к ее запоминанию стоит заблаговременно. Почему бы не повесить материал над рабочим столом задолго до того, как его знание действительно понадобится? Ежедневно наблюдая названия химических элементов, школьник автоматически будет запоминать их. Это пригодится, когда придется приступить к изучению таблицы всерьез.
[Источник: http://fb.ru/]Вовсе не обязательно запоминать новые элементы, созданные человеком. Большинство учителей не требует этого. Речь идет о наделенных повышенной радиоактивностью элементах, представляющих серьезную опасность (после 112). Также полезно время от времени заставлять себя выполнять контрольные работы, проверяя полученные знания. Задания можно найти в учебниках или в интернете.
Лайфхак: как выучить таблицу химических элементов
Существует один весьма распространённый и устойчивый миф о том, что Дмитрий Менделеев открыл свою таблицу химических элементов во сне.
Друзья мои! Нужно быть совершенно недалёкого представления об учёных, чтобы утверждать о том, что научные открытия можно делать во сне или случайно. Известно высказывание самого Дмитрия Ивановича: «Я над ней (таблицей элементов — прим. Учёного Кота), может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово».
А пытались-то многие!
Попытки классифицировать и систематизировать химические элементы возникали задолго до Менделеева. Первую значимую попытку в 1829 году сделал немецкий химик Иоганн Вольфганг Дёберейнер, затем его труды развил другой немец — Леопольд Гмелин. Во Франции определённых успехов достиг химик-геолог Александр де Шанкуртуа. Однако все эти работы не выдерживали научной критики, как например, не смогла устоять система элементов, предложенная англичанином Джоном Ньюлендсом.
Лишь в 1869 году на заседании Русского химического комитета было заслушано сообщение Дмитрия Менделеева об открытии им фундаментального закона природы — Периодического закона. В том же году вышел его учебник «Основы химии», в котором впервые этот закон был представлен в виде таблицы.
Конечно же и труды Меделеева подверглись жесточайшей научной критике! Его идеи не сразу признавались научным сообществом. Лишь только после того, как были открыты новые химические элементы, предсказанные ранее Менделеевым, например, галлий, скандий, германий, Периодический закон был окончательно признан, как одна из теоретических основ химии.
Первый способ: «раскраска»
Так как легко и просто выучить периодическую таблицу химических элементов Менделеева?
Первым способом можно начать знакомство с периодической таблицей ещё в детстве. Подберите карандаши соответствующего цвета, наклейте наклеечки с названиями элементов и дайте ребёнку раскрашивать таблицу.
Второй способ: «Морской бой»
Второй способ более интересней. Многие наверняка знакомы с игрой «Морской бой». Распечатайте таблицу и обозначьте цифрами и буквами вертикали и горизонтали. «Морской бой» начинается!
Со временем можно усложнять игру — например, перестать нумеровать столбцы и строки. И играть, называя только названия:
Если идти по дальнейшему пути усложнения игры, то вместо названия химических элементов, можно называть его атомную или молекулярную массу.
Попробуйте! Вы будете лучше ориентироваться в таблице!
[Источник: https://kpfu.ru/]А какие есть еще варианты?
Каждый второй родитель старается с детства ориентировать ребенка на перспективное будущее. Так что, уже в начальной школе выбирают специализированные курсы с углубленным изучением предметов. Например, биохимическое направление позволит в будущем сдать ВНО без проблем и с позитивным баллом.
Соответственно, больше шансов поступить в вуз с высоким рейтингом, чтобы ребенок продолжал изучение предметов этого цикла и стал великим химиком, врачом или фармацевтом. Но, учебные нагрузки требуют большой работы от ученика. Поэтому вопрос, как выучить таблицу менделеева, должен стать для вас насущным. В профильных классах требуют досконального знания всех элементов в правильном порядке. Выучить непросто, но возможно.
Учим с умом
- Не пытайтесь «зазубривать» элементы. Механическая память хранит информацию две недели от силы. Затем, если информация уже не нужна (ребенок рассказал учителю таблицу наизусть), мозг как бы «стирает» ненужное. А таблица понадобится еще не один год. Так что, этот метод не подходит.
- Детям с развитой зрительной и механической памятью вместо заучивания наизусть, рекомендуют другой способ. Уделите время, перерисуйте таблицу с пустыми окошками. По мере прочтения оригинала, запоминайте и воссоздайте ее в своей таблице. Рисуйте такие таблицы до первой ошибки и старайтесь. Если нарисовали элемент не там, где надо, новую таблицу рисуйте без подглядываний вплоть до этого элемента. Так, будет весомый стимул запомнить больше информации за раз.
- Если важно запомнить обозначения элементов в таблице – попробуйте метод ассоциаций. Повторяйте тройки «элемент- название -обозначение» и придумайте ассоциации. Аргентум – это серебро. Запомните, что в честь элемента названа Аргентина. Когда туда высадились впервые, нашли много серебра. Так изучение таблицы будет осознанным и интересным.
- Если проверят именно ту поочередность элементов, как она дана в таблице, метод ассоциаций чуть измените. Запомнить обозначения элементов в правильной последовательности легко, если писать истории с повторением элементов в той же последовательности, как в таблице. Пример: «Вода залила гелиевую ручку». Это первая строчка, где встречаем «Н — водород» и «Не — гелий». Придумайте полноценные логические истории. Таблица выучится на года и с гарантией. Ученик, при этом, не устанет и отнесется к изучению с пониманием.
Как сделать это максимально быстро?
Для школьников быстро выучить таблицу Менделеева — ужасный сон. Даже 36 элементов, которые традиционно задают педагоги, оборачиваются в несколько часов изнурительной зубрёжки. Многие не верят, что изучить таблицу Менделеева реально. Однако использование мнемотехники способно существенно упростить жизнь школьникам.
Ориентироваться в теории и избрать подходящую технику
Правила, делающие легче изучение материала, именуются мнемоническими. Основная их хитрость — творение ассоциативных взаимосвязей, как только информация абстрактная упаковывается в колоритную картину, звук либо даже аромат. Есть некоторое количество мнемонических техник.
К примеру, можно написать повествование из частей запоминаемой инфы, отыскать однозвучные слова (цезий Цезарь; рубидий — рубильник), подключить пространственную фантазию либо просто элементы таблицы Менделеева зарифмовать.
Об азоте баллада
Рифмовать элементы таблицы Менделеева лучше всего со значением, по конкретным признакам например, по валентности. Так, металлы щелочные рифмуются совсем просто и звучат, как песня Калий, литий, рубидий, натрий, рубидий, франций, цезий.
Кальций, магний, цинк и барий — валентность их паре равна — неумирающая классика фольклора школьного. На эту же тему Калий, натрий, сребро одновалентное добро и Калий, натрий и аргентум всегда одновалентны. Творчество в различие от зубрёжки, которой максимально хватает на несколько дней, провоцирует длительную память.
Кислотный триллер
Для лучшего запоминания элементов таблицы Менделеева придумывается история, в которой они преобразуются в героев, подробности пейзажа либо сюжетные составляющие. Вот, к примеру, всем знакомый текст «Азиат (Азот) стал ливнем (Литий) обливать воду (Водород) в сосновый Бор (Бор). Однако не он (Неон) был нам необходим, а Магнолий (Магний)».
Эту история можно дополнить ситуацией о ferrari (феррум — железо), в которой скрытый агент ехал Хлор 017 (семнадцать — последовательный номер хлора), чтоб словить преступника Арсения (арсеникум — мышьяк), у которого было тридцать три зуба (33 — последовательный номер мышьяка), однако внезапно что-то кислое ему в рот попало (кислород — кислое), это было 8 отравленных пуль (восемь — последовательный номер кислорода)…
Такие истории можно рассказывать до бесконечности. Также, триллер, созданный по темам периодической таблицы Менделеева, можно вручить преподавателю литературы, как экспериментальный текст. Ему, наверное, понравится.
Выстроить дворец памяти
Это одно из имён достаточно действенной техники запоминания, когда в работу включается мышление пространственное. Её секрет в том, что мы все можем легко описать собственное жилище либо путь от дома до торгового центра, института, школы.
[Источник: http://1todo.ru/] Поделиться статьей с друзьями!Чтоб быстро выучить элементы таблицы Менделеева необходимо расположить их по дороге (либо в комнате), при этом каждый элемент представить очень визуально, ясно, ощутимо. Например, водород — худой блондин с вытянутым личиком. Человек кладёт плитку — кремний. Группа бизнесменов в дорогой автомашине — инертные газы. И, естественно, гелий — торговец воздушных шариков.
комиксы, гиф анимация, видео, лучший интеллектуальный юмор.
Таблица Менделеева… Это 118 неповторимых ячеек, 18 групп, 8 периодов!
Таблица Менделеева… Это 7021 протон на всех!
Таблица Менделеева… Ты с нами уже почти 145 лет!
Таблица Менделеева… Это лантаноиды и актиноиды, галогены и инертные газы, щелочные и щелочно-земельные, просто металлы, неметаллы!
Таблица Менделеева… Это яркость на обороте почти каждого учебника по химии!
Таблица Менеделеева… Здесь есть всё, что есть в тебе!
Подробнее
1РА) 1 пор«» ‘ ■Ё и « г “1 г (на) вГ^ •мол Периодическая система химических элементов Д.И. Менделеева Кщш ■ И ** ■ ■ т*’ • Нд-.у:г № — Мд ‘1№ 18СЛи) • • им* • < 15 (ША) Х4(1УА) 15 (УА) 16 (У1А) 17СЛ1А) м 501«) 4<1УВ) 5 (^8) 6(У)В> 7(\Л«8) 8 (УН!) 9(\ЛИ) 10 (У1»0 И<№> 17<НВ) К — Са — Бс » П 4 мм*» «мм V ~ Сг М*И _• к*м НЛО» «ММ м»и «*м* ми. • К(М НПО И»« 4) *М1* к Ми-.- •**«* «м Яи — Бг •= У •- гг 7 ЫЬ~ Мо~ Тс = Яи я ЯЬ = Ра — Ад» Сс1 ~ 1п ~ Бп ~ БЬ 5 К«1 ММ И»ц *ЧК *»•** ПИ *•• ИМ« И» «И ИМЛГ ы.».,, »и*»» ИМ» ИМ* »м» «ш&йвб ^ ¿г > *« «/ ■ я? 1 ■» С5 « Ва Г. 1а*~ Hf = Та = W = Яе = 0$ = 1г € Яг 7 мч Ас’!-. Rf = ОЬ Р»Г) (*1) 1М*} я« * ПыЗё IV V ВИ 1»М1 1*»| |М4| ▲ И 1»»| * Ии««« С = им» * f Дм* N 3 »МИ ¡й пи* • *«* И МММ Г Л*И А1 Р ~ мяй и.И0 » чгЛЩТ гГ~ ММ4 4 •*чм II «•*•» Р « НЛ* «¡1« »• <•*- Б ~ км* и I» Ш И Цми! И “.11- >• <мм 6с — Ав 5* Бе 5 »!>* НШ ММ «я »• *И-^ МАИ ч<*>* у# Кг “ «« И мга и С~м- Бп “ »»м» 3. »• <0ИАИ БЬ- нм» еа и им* п£?3 1» *м & ¿И» Ц »• Коми Хс~ ш »« (ММ РЬ » •>э ‘» И-« 81 -йене &3 Ро ** Л0.Н •»« ЙММ ▲ ¿1 и д…. А1 * ММ* 4Д 4 и **»• р- ‘ им» Еб1 ‘ ии» А 1И — ■ иия 1»*1 А йир (МЦ г ▲ »и ииИ |т| А ии5 иио 1«Ч 1″Ч ||| * Л * ё •* »»И* Ег — + Ч-и Тт ? * |И,М УЬ » П ЛмммМ и» * Яп^ Шг N0 ~ и; ■ «\л * ГЦниномды • Актиноиды
Таблица Менделеева,Периодическая система химических элементов
Еще на тему
Таблица Менделеева(44)
Периодическая таблица в формате PDF со 118 элементами


Выберите из большой коллекции PDF-файлов для печати. Включены цветные периодические таблицы, черно-белые таблицы, пустые таблицы и широкий выбор специальных таблиц. У нас также есть выбор периодических таблиц на других языках помимо английского. В этих таблицах используются последние данные IUPAC.
Файлы PDF с периодической таблицей
Для печати таблиц в формате PDF требуется, чтобы Adobe открывала, читала и распечатывала.Эти столы идеально подходят для изготовления больших плакатов или настройки размеров стола.
Периодическая таблица цветов — В этой таблице представлены последние данные IUPAC по всем 118 элементам в приглушенной, легко читаемой цветовой схеме. [PDF-файл]
Периодическая таблица цвета свечения — Эта таблица содержит стандартные значения атомного веса ИЮПАК для всех 118 элементов. Группы элементов обведены светлым цветом для удобства чтения и печати. [JPG] [PDF]
Оптимизированная периодическая таблица для принтера — Эта красочная таблица оптимизирована для печати.Он использует четкий шрифт и удобные для печати цвета. Включены факты для всех 118 элементов. [PDF] [PNG]
Черно-белая периодическая таблица — Независимо от того, отвлекает ли цвет или вы его просто не хотите, вот вам черно-белая таблица из 118 элементов. [PDF-файл]
Периодическая таблица без имен — это таблица, которую нужно использовать, если вы изучаете названия элементов или просто хотите более чистую таблицу, периодическую таблицу с символами и числами. [Цветной PDF] [Черно-белый PDF]
Периодическая таблица для детей — Плитки из 118 элементов имеют цветную рамку, которая указывает на группу элементов, или же они черно-белые.Каждая атомная масса округлена до двух десятичных знаков для облегчения вычислений. [Цветной PDF] [Черно-белый PDF]
Пустая периодическая таблица — Заполните пустые поля. Предоставляются ячейки и формат для всех 118 элементов. [PDF-файл]
Периодическая таблица размеров атомов — См. Относительные размеры атомов элементов. [PDF-файл]
Периодические таблицы в формате JPG и PNG
Таблицы в формате JPG и PNG являются файлами изображений. В частности, файлы PNG — это файлы очень маленького размера, которые печатаются очень четко.
Периодическая таблица ярких цветов HD — Это таблица, показанная выше. Он содержит имена элементов, символы, атомные номера, атомные массы и группы элементов. Это изображение PNG с разрешением 1920 × 1080 пикселей, доступное на белом или черном фоне. [таблица на белом] [таблица на черном]
Таблица звезд и туманностей Хаббла — это файл изображения в формате JPG, который печатается для создания большого красочного плаката таблицы Менделеева. [JPG image]
Условия использования
Вы можете загрузить и распечатать эти PDF-файлы с периодической таблицей для использования в качестве раздаточных материалов и обоев для личного или учебного использования.Однако эти изображения защищены авторским правом и не могут быть размещены в других местах в Интернете, адаптированы или использованы для продажи каким-либо образом. Мы сохраняем за собой все права на файлы PDF.
.Периодическая таблица: Чтение периодической таблицы
Еще раз, вот ссылка для просмотра таблицы Менделеева в полный размер: Чтобы увидеть таблицу Менделеева, щелкните здесь. Когда появится окно, наведите указатель мыши на элементы, чтобы увидеть их конкретная информация. Вы также можете получить доступ к таблице Менделеева, войдя в справочный раздел SparkNotes, который находится в верхней части каждого SparkNotes стр.
Общая структура периодической таблицы
Как указано в последнем раздел, периодический таблица упорядочивает элементы в соответствии с общими схемами сходства.Ниже очень небольшое изображение периодической таблицы. Это практически нечитаемо с точки зрения конкретных информации, но позволяет легко увидеть общие тенденции в структуре периодической таблицы.
 Рисунок%: очень маленькая таблица Менделеева
Рисунок%: очень маленькая таблица МенделееваВертикальные столбцы таблицы Менделеева (отмечены желтыми полосами в рисунок) называются группами. Горизонтальные ряды называются периоды. Всего 18 групп и 7 периодов. Обсуждая периодическая таблица с этого момента мы будем использовать термины группа и период.Вниз по группе означает движение сверху вниз; через период означает двигаясь слева направо.
Чтение периодической таблицы: углерод
Чтобы описать информацию, содержащуюся в каждой отдельной ячейке, мы будем использовать конкретный пример: углерод.
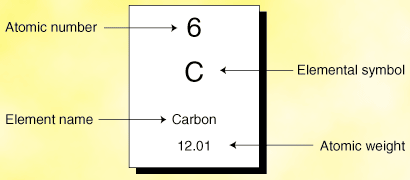 Рисунок%: Описание углерода в периодической таблице
Рисунок%: Описание углерода в периодической таблицеИмя элемента
Назначение имени элемента очевидно. Однако многие периодические таблицы не содержат имен элементов. В таких ситуациях вы должны запомнить символы, соответствующие названию каждого элемента.
Символ элемента
Каждый элемент имеет определенный одно- или двухбуквенный символ, который используется как синоним его имени. Эти следует запомнить. В большинстве случаев символы довольно четко соответствуют названию элемента, который они представляют, как C соответствует углероду. Однако иногда имя и символ элемента имеют мало связь. Например, ртуть обозначается символом Hg.
.Chem4Kids.com: Элементы и Периодическая таблица: Периодическая таблица
Периодическая таблица организована как большая сетка. Каждый элемент помещается в определенное место из-за его атомарной структуры. Как и в любой другой сетке, в периодической таблице есть строки (слева направо) и столбцы (вверх и вниз). Каждая строка и столбец имеют определенные характеристики. Например, магний (Mg) и кальций (Mg) находятся во втором столбце и имеют определенные сходства, в то время как калий (K) и кальций (Ca) из четвертой строки имеют разные характеристики.Магний и натрий (Na) также имеют общие качества, потому что находятся в один период (схожие электронные конфигурации). Несмотря на то, что они пропускают некоторые квадраты между ними, все строки читаются слева направо. Когда вы смотрите на периодическую таблицу, каждая строка называется периодом (Понять? Как таблица PERIODic.). Все элементы периода имеют одинаковое количество атомных орбиталей. Например, каждый элемент в верхнем ряду (первый период) имеет одну орбиталь для своих электронов. Все элементы во втором ряду (второй период) имеют две орбитали для своих электронов.По мере продвижения вниз по таблице каждая строка добавляет орбиталь. В настоящее время существует максимум семь электронных орбиталей. Теперь вы знаете, что месячные идут слева направо. Периодическая таблица также получила особое название для своих вертикальных столбцов. Каждый столбец называется группой . Элементы в каждой группе имеют одинаковое количество электронов на внешней орбитали . Эти внешние электроны также называются валентными электронами . Это электроны, участвующие в химических связях с другими элементами.
Каждый элемент в первом столбце (первая группа) имеет один электрон во внешней оболочке. Каждый элемент во втором столбце (вторая группа) имеет два электрона во внешней оболочке. Продолжая считать столбцы, вы будете знать, сколько электронов находится во внешней оболочке. Когда вы смотрите на элементы перехода, есть исключения из порядка, но вы понимаете общую идею. Переходные элементы добавляют электроны на предпоследнюю орбиталь.
Например, азот (N) имеет атомный номер семь.Атомный номер говорит о том, что в нейтральном атоме азота семь электронов. Сколько электронов находится на его внешней орбитали? Азот находится в пятнадцатом столбце, обозначенном «Группа VA». «V» — это римская цифра для пяти, обозначающая количество электронов на внешней орбитали. Вся эта информация говорит вам, что на первой орбитали есть два электрона, а на второй — пять (2-5).
Фосфор (P) также находится в группе VA, что означает, что он также имеет пять электронов на своей внешней орбитали.Однако, поскольку атомный номер фосфора равен пятнадцати, электронная конфигурация составляет 2-8-5.
Водород (H) и гелий (He) — особые элементы. Водород в нейтральной форме не имеет нейтрона. Есть только один электрон и один протон. Вы, вероятно, не найдете атомарного водорода, плавающего сами по себе. Атомарный водород хочет объединиться с другими элементами, чтобы заполнить свою внешнюю оболочку. Ваша химическая работа, скорее всего, будет использовать молекулярный водород (H 2 ) или ионы водорода (H + , протоны). Гелий (He) отличается от всех других элементов. Он очень стабилен, имея всего два электрона на внешней орбитали (валентной оболочке). Несмотря на то, что у него всего два электрона, он все еще сгруппирован с благородными газами, у которых есть восемь электронов на их внешних орбиталях. Благородные газы и гелий «счастливы», потому что их валентная оболочка заполнена.
ChemCam Rock Laser для MSL (видео Лос-Аламоса, Нидерланды)
.
История периодической таблицы Урок
Введение
«Периодическая таблица элементов — один из самых мощных символов в науке: единый документ, который изящно отражает суть химии. Действительно, ничего подобного не существует в биологии, физике или любой другой области науки. , в этом отношении.» Таблица Менделеева — это «инструмент, который служит для организации всей химии». Эрик Р. Скерри
Хотя Дмитрия Менделеева часто считают «отцом» периодической таблицы Менделеева, работа многих ученых способствовала ее нынешней форме.В этом уроке Софии сделана попытка обобщить основные вехи в развитии этого инструмента.
Весь текст этого упражнения взят из книги Эрика Р. Скерри «Периодическая таблица: ее история и ее значение», Oxford University Press, © 2007. {Ссылка на книгу}
Scerri, E. (2007). Таблица Менделеева: ее история и ее значение. Оксфорд: Издательство Оксфордского университета. ISBN 0-19-530573-6.
Иоганн Вольфганг Дёберейнер (1817)
В 1817 году Иоганн Доберейнер первым заметил существование различных групп из трех элементов, впоследствии названных триадами, которые демонстрировали химическое сходство и отображали важную числовую взаимосвязь, а именно, что вес среднего элемента был приблизительным средним значением значения двух элементов, фланкирующих его в триаде.Его первая триада включала кальций, стронций и барий. Он требовал, чтобы его триады, чтобы быть значимыми, выявляли химические отношения между элементами, а также числовые отношения. Это наблюдение сначала мало повлияло на химический мир, но позже стало очень влиятельным.
В 1829 году он добавил к своему открытию три новых триады.
- хлор, бром, йод
- натрий, литий, калий
- сера, селен, теллур
http: // слайд-плеер.com / slide / 6976715/24 / images / 28 / D% C3% B6bereiner% E2% 80% 99s + Triads + Name + Atomic + Mass + Calcium + 40 + Barium + 137.jpg
{стр. 42-43}
Леопольд Гмелин (1843)
Хотя Дёберейнера справедливо считают создателем понятия триады, Гмелин также проделал большую полезную работу в этой области, и именно он ввел термин «триада». Как и Доберейнер, Гмелин рассматривал как химические, так и числовые отношения при поиске триад, и он смог расширить работу своего предшественника, используя улучшенные атомные веса, которые были недоступны Доберейнеру.Например, в то время как Дёберейнер сгруппировал магний вместе с щелочноземельными элементами на основе их химического сходства, он не смог найти триадную взаимосвязь, включающую его и другие щелочноземельные элементы. Гмелин, с другой стороны, смог выявить взаимосвязь, используя свои собственные недавно полученные значения атомных весов.
Но одним из наиболее замечательных аспектов творчества Гмелина была система расположения элементов. Благодаря существованию четырех несвязанных триад, открытых Доберейнером, Гмелин смог сделать огромный скачок вперед в создании системы, основанной на триадах, состоящих из 55 элементов.Кроме того, его система в целом была упорядочена в соответствии с возрастающим атомным весом (хотя это не было явно организовано таким образом). Этой работой Гмелину удалось уловить правильную группировку большинства известных тогда элементов основной группы. Гмелин расположил свои триады горизонтально в виде V-образной схемы.
Когда Гмелин опубликовал свое новое расположение химических элементов, он, возможно, был первым автором учебника химии, который использовал свою систему в качестве основы для представления информации в своем учебнике химии.
{стр. 44-46}
Александр Эмиль Бегуйе де Шанкуртуа (1862)
В 1862 году де Шанкуртуа опубликовал свой теллурический винт , или свою систему расположения известных химических элементов. Он предложил трехмерное представление элементов, расположенных в соответствии с тем, что он назвал возрастающими «числами» по спирали. Эта таблица представляет собой сокращенную таблицу, в которой не отделяются элементы основной группы от переходных металлов.
https: // загрузить.wikimedia.org/wikipedia/commons/5/57/Telluric_screw_of_De_Chancourtois.gif
http://cea.quimicae.unam.mx/estru/tabla/05_Parametros.htm
Он был первым, кто осознал, что свойства элементов являются периодической функцией их атомного веса. Хотя он натолкнулся на это ключевое понятие, лежащее в основе периодической системы, система де Шанкуртуа не произвела большого впечатления на химиков, и ему обычно не уделяют должного внимания по нескольким причинам. Во-первых, его оригинальная публикация не включала диаграмму, в основном из-за сложности, с которой издатель столкнулся при попытке воспроизвести ее.Во-вторых, его система включала некоторые ионы, соединения и сплавы. Кроме того, его публикация не появилась в химическом журнале (она была опубликована в журнале Académie des Sciences, Comptes Rendus ), и в последующие годы он не развивал свои идеи. В качестве примечания он был разочарован тем, что в журнал Comptes Rendus не удалось включить его диаграмму, поэтому он переиздал свою систему в 1863 году. Но, поскольку она была опубликована в частном порядке, она получила даже меньше внимания со стороны других ученых, чем его оригинал.
{стр. 68-71}
Джон Александр Рейна Ньюлендс (1863)
В 1863 году Ньюлендс опубликовал первую из множества систем классификации элементов. Он разработал свою систему без преимуществ новых значений атомного веса, которые были опубликованы после очень важной конференции по химии в 1860 году. Его первая опубликованная статья о классификации элементов была опубликована анонимно, хотя он вскоре раскрыл свою личность в ответ. на критику.
В 1864 году Ньюлендс опубликовал свою вторую статью о классификации элементов. На этот раз он использовал более точные атомные веса, выпущенные в 1860 году. Менее чем через месяц после появления этой системы он опубликовал третью систему, но в эту таблицу он включил меньше элементов (24 плюс место для нового элемента) и не сделал ничего. упоминание об атомных весах. Тем не менее, эта статья имеет большое значение, поскольку Ньюлендс присвоил порядковый номер каждому из элементов, отказавшись от арифметических прогрессий в атомных весах, которые беспокоили более ранних исследователей.Ньюлендс просто выстроил элементы в порядке увеличения атомного веса, не заботясь о значениях этих весов. Самым важным, что Ньюлендс сделал в своей третьей публикации по классификации элементов, было представление периодической системы; то есть он обнаружил закономерность повторения свойств элементов через определенные регулярные промежутки времени. В этом, конечно же, и заключается суть периодического закона, и Ньюлендс заслуживает похвалы за то, что так рано признал этот факт вместе с Де Шанкуртуа.Другим нововведением системы Ньюлендса в 1864 году было то, как он поменял местами элементы йода и теллура, чтобы отдать предпочтение химическим свойствам над очевидным порядком атомного веса.
В 1865 году Ньюлендс разработал еще одну систему, которая значительно улучшила систему предыдущего года, поскольку теперь он включил 65 элементов в порядке возрастания атомного веса, снова используя порядковые числа, а не фактические значения атомного веса.Он зашел так далеко, что провел аналогию между периодом элементов и музыкальной октавой, в которой тоны отображают повторение с интервалом в восемь нот. Это стало известно как его «закон октав».
«Если элементы расположены в порядке их эквивалентов с небольшими перестановками, как в прилагаемой таблице, можно заметить, что элементы, принадлежащие к той же группе, обычно появляются на одной и той же горизонтальной линии. Также будет видно, что числа аналогичных элементов различаются либо на 7, либо на несколько кратных семи; другими словами, члены одной и той же группы стоят по отношению друг к другу в таком же отношении, как концы одной или нескольких октав в музыке…. Восьмой элемент, начинающийся с заданного, является своего рода повторением первого. Я предлагаю назвать это конкретное соотношение октавным законом ».Это утверждение знаменует собой довольно важный шаг в эволюции периодической системы, поскольку оно представляет собой первое четкое объявление нового закона природы, касающегося повторения ими свойств элементов через определенные интервалы в их последовательности. Ньюлендс гораздо более ясно высказался о существовании периодического закона, чем Де Шанкуртуа, который просто упомянул его как возможность.Закон октав полностью применим к первым двум периодам, за исключением благородных газов, которые еще не были открыты. Помимо этого, периодичность Ньюлендса неизбежно столкнется с трудностями, поскольку включение переходных металлов делает более поздние периоды намного более длительными, чем 8.
Ньюлендс впервые объявил о своем законе октав в докладе, представленном Лондонскому химическому обществу в 1866 году, но, к его большому несчастью, его идеи были восприняты плохо. То, что представил Ньюлендс, было улучшенной версией его системы 1865 года (см. Ниже).Самый известный ответ Ньюлендсу — это часто цитируемый Джордж Кэри Фостер, который предположил, что Ньюлендс вполне мог бы получить лучшую схему классификации, если бы он просто упорядочил элементы в алфавитном порядке по первой букве каждого из их имен. Ньюлендс продолжал публиковать работы о периодической системе до 1878 года.
https://upload.wikimedia.org/wikipedia/commons/e/e5/Newlands_periodiska_system_1866.png
{стр. 72-80}
Юлиус Лотар Мейер (1864)
Мейера больше всего помнят за его независимое открытие периодической системы, хотя больше всего заслуги у Менделеева.
В 1864 году Мейер опубликовал таблицу из 28 элементов, расположенных в порядке возрастания атомного веса. Мейер изо всех сил пытался упорядочить элементы только по атомному весу и признал необходимость упорядочения элементов также на основе химических свойств. В некоторых случаях он, казалось, решил позволить химическим свойствам перевешивать строгий порядок атомных весов, что Менделеев не мог сделать. Примером этого является группировка теллура с такими элементами, как кислород и сера, в то время как йод группируется с галогенами, несмотря на их порядок в соответствии с атомным весом.Организация элементов Мейера в столбцах (по вертикали) похожа на некоторые группы, которые можно увидеть в современной периодической таблице.
Еще одна примечательная особенность таблицы Мейера — наличие множества пробелов для обозначения неизвестных элементов. И снова выясняется, что устранение пробелов возникло не от Менделеева, которому пришлось ждать еще пять лет, прежде чем даже рискнуть опубликовать периодическую систему и, в конечном итоге, сделать подробные прогнозы, благодаря которым он впоследствии стал так хорошо известен.
Сходства периодических таблиц Мейера и Менделеева:
- Оба элемента расположены за счет увеличения атомного веса.
- Оба распознали закономерность в свойствах элементов, упорядоченных по атомным весам.
- Оба оставили пробелы для неоткрытых элементов.
{Стр. 92-98}
Дмитрий Иванович Менделеев (1869)
Хотя периодические системы были независимо созданы шестью соавторами, система Дмитрия Менделеева до сих пор оказала наибольшее влияние.Система Менделеева была не только более полной, чем другие, но он также работал намного усерднее и дольше для ее принятия. Он также пошел намного дальше, чем соавторы, используя его для предсказания существования ряда неизвестных элементов.
В 1869 году Менделеев создал первую версию полной таблицы Менделеева, которая включала большинство известных элементов. Первоначально он сгруппировал элементы в соответствии с тем, как они соединяются с водородом с образованием соединений, но это не обнаружило никаких признаков других отношений между элементами.Когда Менделеев переключил свою организацию на перечисление элементов путем увеличения атомного веса, его периодическая система, казалось, встала на свои места. В таблице Менделеева он оставил несколько свободных мест, специально предвосхищая многие еще неизвестные элементы. Самые известные предсказания Менделеева касались элементов скандия, галлия и германия, в которых он предсказал высокоточные атомные веса и другие физические свойства.
Именно эти смелые прогнозы отличают Менделеева от его конкурентов.Его гений заключался в его способности интуитивно просеивать массу правильных и неправильных знаний об элементах, которые были накоплены, чтобы создать систему, которая была одновременно элегантной и достаточно прочной, чтобы противостоять химическим и физическим открытиям, которые последуют за этим.
{стр. 103-106, 123-124}
Генри Гвин Джеффрис Мозли (1913)
В 1913 и 1914 годах Генри Мозли показал, что элементы следует упорядочивать в соответствии с их атомным номером, а не атомным весом.
Предшественники Мозли упорядочили периодическую таблицу по атомному весу, а затем присвоили каждому элементу произвольную величину, называемую атомным номером, в зависимости от порядка элементов в периодической таблице, но без какого-либо физического смысла.
Мозли работал студентом-исследователем у Резерфорда в Манчестере. Он сначала экспериментировал с 14 элементами, девять из которых, от титана до цинка, образовали непрерывный ряд в периодической таблице. Мозли открыл фундаментальную величину, которая увеличивалась через регулярные промежутки времени по мере того, как он перемещался по своей последовательности элементов в том порядке, в котором они появлялись в периодической таблице.Он быстро распознал эту величину как положительный заряд ядра. После этого открытия атомный номер стал известен как число протонов в ядре. Работа Мозли ясно показала, что последовательные элементы в периодической таблице имеют атомный номер на одну единицу больше. Исходя из этого факта, Мозли и другие смогли определить, какие пробелы еще предстоит заполнить в периодической системе, и обнаружили, что всего семь таких случаев все еще ждут своего открытия. В отличие от предыдущих списков пробелов, этот список теперь был полностью окончательным и включал точные атомные номера все еще неуловимых элементов, которые составляли 43, 61, 72, 75, 85, 87 и 91.
https://www.iupac.org/publications/ci/2012/3404/ud.html
Хотя использование атомных номеров не привело к каким-либо глубоким изменениям формы периодической таблицы Менделеева, пояснение, которое Мозли внес в периодическую таблицу, решило давние проблемы, связанные с обращением пар никеля и кобальта, а также теллура и йода, которые преследовал Менделеева на протяжении всей его карьеры. Его открытие также помогло разместить редкоземельные элементы, что было одной из самых сложных проблем периодического закона, поскольку их было заведомо трудно разделить химически.
Мозли никогда не был свидетелем успеха своего открытия, потому что он был убит в первые годы Первой мировой войны, выстрелом в голову в 1915 году турецкий солдат во время битвы при Галлиполи. Ему было 27 лет. Принято считать, что если бы Мозли прожил еще один год, он почти наверняка был бы удостоен Нобелевской премии в 1916 году за открытие физических основ атомного числа. Поскольку Нобелевские премии вручаются только живым лауреатам, эта возможность умерла с Мозли в Галлиполи.Нобелевская премия по физике 1916 г. вообще не присуждена.
{стр. 31; 170-173}
Гленн Теодор Сиборг (1945)
В 1945 году Сиборг обнаружил, что в периодической таблице необходимо серьезное изменение. Несколько элементов, которые считались принадлежащими к семейству переходных металлов, были выделены из основной части таблицы Менделеева, чтобы сформировать ряды лантанидов и актинидов (нижние две строки).
Гленн Сиборг предположил, что элементы, начинающиеся с актиния, номер 89, следует рассматривать как серию редкоземельных элементов, а не предыдущую мысль о том, что редкоземельные элементы начинаются после элемента 92, урана.Новая периодическая таблица Сиборга предполагает, что элементы европий (63) и гадолиний (64) должны иметь характеристики, аналогичные неоткрытым элементам 95 и 96 соответственно. В результате Сиборгу удалось синтезировать и идентифицировать два новых элемента, которые были названы америций (95) и кюрий (96).
http://d1068036.site.myhosting.com/periodic.f/synthesis.html
Сиборг был главным или соавтором десяти элементов: плутония, америция, кюрия, берклия, калифорния, эйнштейния, фермия, менделевия, нобелия и 106-го элемента, названного в его честь сиборгием.Он один из двух людей, чей элемент был назван в честь них еще при жизни.
«Это величайшая честь, когда-либо оказанная мне — я думаю, даже лучше, чем получение Нобелевской премии», — сказал Сиборг, один из первооткрывателей плутония и девяти других трансурановых элементов. «У будущих студентов-химиков, изучающих периодическую таблицу, может появиться причина спросить, почему элемент был назван в честь меня, и таким образом узнать больше о моей работе». — Гленн Сиборг
{стр. 21-22, 307}
.
