Зачем нужен иммунитет, и как он работает? — Группа компаний «Просвещение»
«Зачем нужен иммунитет?» — это не только один из самых популярных детских вопросов, но и отличный вариант для проектной деятельности. Особенно сейчас, когда дети и взрослые «гуглят» все, что связано с заболеваниями, вирусам и защитой от них. В этом материале мы собрали информацию, которая поможет как ученику, так и учителю.
Что такое иммунитет?
Иммунитетом называют способность организма находить чужеродные тела и вещества (антигены) и избавляться от них. Слово «иммунитет» происходит от латинского immunitas, что значит «избавление от чего-либо».
Виды иммунитета
Различают клеточный иммунитет, при котором уничтожение чужеродных тел осуществляют клетки, например фагоциты, и гуморальный иммунитет, при котором посторонние тела удаляются с помощью антител, доставляемых кровью. Клеточный иммунитет был открыт И.И. Мечниковым, а гуморальный — П.
Иммунитет может быть видовым (человек не болеет чумкой собак). К некоторым чужеродным телам иммунитет бывает наследственным (врождённым), к другим он появляется после того, как антиген будет выявлен и опознан, а затем обезврежен (приобретённый иммунитет).
Как работает иммунитет нашего организма?
Врождённая иммунная система обладает широким арсеналом для встречи и борьбы с вредными вирусами. Постараемся объяснить это «на пальцах»:
- Фагоциты – например, макрофаги, которые «съедают» бактерии.
- Система комплемента – сложный комплекс из белковых молекул, которые умеют разрушать бактерии.
- Цитокины – сигнальные белковые молекулы, которые передают информацию о воспалении или инфекции в организме.

- Антигенпрезентирующие клетки (APC) – эти клетки умеют «выставлять наружу» пептиды, которые являются частью вируса или бактерии. Иными словами, это дружинники, которые показывают полиции нарушителя! APC – это связующее звено между двумя иммунными подсистемами, о второй из которых ниже.
Адаптивная иммунная система
В самом начале те самые антигенпрезентирующие клетки (АРС) отправляются с кусочком патогена в лимфоузлы, где им навстречу идут Т-лимфоциты. При встрече выясняется, что принесенный АРС образец не является здоровой и родной частью организма, а потому Т-лимфоциты переходят в состояние боевой готовности, превращаясь:
- В Т-киллера, который способен уничтожить нездоровые клетки организма.
- В Т-хелпера, который активирует B-лимфоциты. Вообще эти лимфоциты умеют производить более 100 миллионов видов антител, потому наш организм и может справиться с огромным количеством патогенов.

Активация В-лимфоцитов: часть клеток превращается в в плазматические клетки, способные к продукции антител, другие становятся клетками памяти. Скачать инфографику можно в конце статьи.
Что происходит, если организм сталкивается со знакомым патогеном?
За это тоже отвечают чудесные B-лимфоциты. Оказываются, они умеют вырабатывать не только антитела, но и превращаться в клетки памяти. Эти клетки несут на своего поверхности рецепторы, распознающие конкретный антиген, и живут они довольно долго, так что переживать не стоит.
Итак, представим, что в организм попал патоген, который уже атаковал организм. При прошлой встрече с вирусом необходимые антитела появились в достаточном количестве через две недели. Теперь же АРС показывает уже знакомый ей патоген клетке памяти, та волнуется, активируется и начинает производить антитела в ускоренном режиме – в 100 раз быстрее! В итоге уже через пару дней ваш организм готов к борьбе с захватчиком.
При прошлой встрече с вирусом необходимые антитела появились в достаточном количестве через две недели. Теперь же АРС показывает уже знакомый ей патоген клетке памяти, та волнуется, активируется и начинает производить антитела в ускоренном режиме – в 100 раз быстрее! В итоге уже через пару дней ваш организм готов к борьбе с захватчиком.
Зачем нужны прививки?
Причиной очень многих заболеваний являются болезнетворные микробы. Болезни, ими вызванные, могут захватить целые страны и области — подобные случаи, которых в истории человечества множество, называются эпидемиями.
Кто же доказал, что в корне заболеваний лежат вредные микробы, а не проклятие, насланное врагами или колдунами (мы не шутим, подобное объяснение было самым популярным в Средние века)? Причастность микробов к заразным заболеваниям доказал француз Луи Пастер.
Именно этот ученый доказал, что специально зараженный ослабленными микробами человек в будущем уже серьезно не заболеет. Его антитела и лейкоциты справятся с бактериями с помощью выработанного 
Пастер предложил не только эту бесконечно важную для медицины идею, но и разработал вакцины от различных болезней. Самым ярким примером будет вакцина против бешенства. Вирус бешенства, которым болеют многие животные, опасен и для человека, потому уколы от бешенства после укуса даже приятной на вид уличной собаки обязательны. Вирус бешенства поражает нервную систему и приводит к судорогам глотки и параличу дыхательных мышц или к прекращению сердечной деятельности.
Что происходит, когда человеку делают прививку?
Если человек здоров, ему вводят вакцину (ослабленному организму делать прививку нельзя, так как даже малое количество болезнетворных бактерий может спровоцировать болезнь). Вакцина содержит ослабленные микробы или их яды, которые, попадая в организм, вызывают иммунную реакцию. В итоге человек получает иммунитет от болезни, которую ему привили.
Таблица «Виды иммунитета». Источник: Учебник по биологии, 9 класс. Линия УМК И. Н. Пономаревой. Биология (Линейная) (5-9)
Линия УМК И. Н. Пономаревой. Биология (Линейная) (5-9)
Прививки и виды иммунитета
- Иммунитет, имеющийся или самовозникающий у человека, называют естественным.
- Иммунитет, полученный путём использования медицинских средств, называют искусственным.
Создание искусственного иммунитета нашло широкое распространение во всём мире и только. Отказ от прививок в нашей стране, к сожалению, законен, но подобное поведение — нерационально, абсолютно ненаучно и опасно!
Темы для докладов и проектной деятельности по биологии. Раздел «Иммунитет»
- Зачем человеку нужен иммунитет?
- Открытие Луи Пастера: в мастерской исследователя
- Работы английского врача Э.Дженнера: кто вдохновил Пастера?
- Самые опасные эпидемии в истории: что могло помочь их избежать?
- Прививки в раннем детстве: к чему может привести их отсутствие?
- Как укреплять свою иммунную систему?
- Заболевания иммунной системы: причины и последствия.

- Приключения Т-лимфоцитов (творческое задание: написать рассказ от имени защитников организма)
Понятие иммунитета. Справка — РИА Новости, 27.09.2010
Специфический и неспецифический иммунитет
Неспецифический (врожденный) иммунитет – это однотипные реакции организма на любые чужеродные антигены.
Главным клеточным компонентом системы неспецифического иммунитета служат фагоциты, основная функция которых — захватывать и переваривать проникающие извне агенты.
Для возникновения подобной реакции чужеродный агент должен иметь поверхность, т.е. быть частицей (например, заноза).
Если же вещество молекулярно-дисперсное (например, белок, полисахарид, вирус), не токсичное и не обладает физиологической активностью, оно не может быть нейтрализовано и выведено организмом по вышеописанной схеме.
В этом случае срабатывает специфический иммунитет. Он приобретается в результате контакта организма с антигеном и характеризуется формированием иммунологической памяти. Его клеточными носителями служат лимфоциты, а растворимыми — иммуноглобулины (
Его клеточными носителями служат лимфоциты, а растворимыми — иммуноглобулины (
Первичный и вторичный иммунный ответ
Специфические антитела продуцируются специальными клетками — лимфоцитами. Причем для каждого вида антител существует свой тип лимфоцитов (клон).
Первое взаимодействие антигена (бактерии или вируса) с лимфоцитом вызывает реакцию, названную первичным иммунным ответом, в ходе которого лимфоциты начинают развиваться в виде клонов. Затем некоторые из них становятся клетками памяти, другие превращаются в зрелые клетки, продуцирующие антитела. Главные особенности первичного иммунного ответа — существование латентного периода до появления антител, затем выработка их лишь в небольшом количестве.
Вторичный иммунный ответ развивается при последующем контакте с тем же самым антигеном. Основная особенность – быстрое развитие лимфоцитов с дифференцировкой их в зрелые клетки и быстрая выработка большого количества антител, которые высвобождаются в кровь и тканевую жидкость, где могут встретиться с антигеном и эффективно побороть болезнь.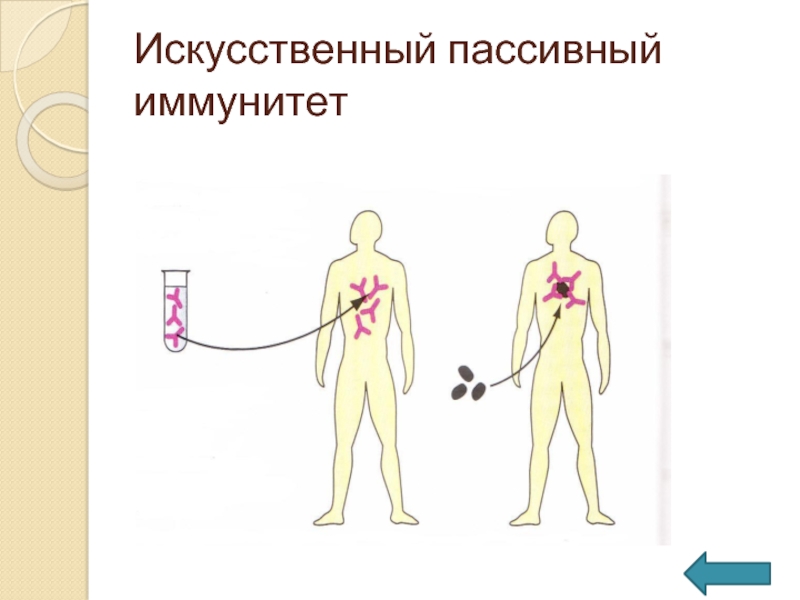
Естественный и искусственный иммунитет
К факторам естественного иммунитета относят иммунные (система комплемента, лизоцим и др. белки) и неиммунные механизмы (кожа, слизистая, секрет потовых, сальных, слюнных желез, желез желудка, нормальная микрофлора).
Искусственный иммунитет вырабатывается при введении в организм вакцины или иммуноглобулина.
Активный и пассивный иммунитет
Активная иммунизация стимулирует собственный иммунитет человека, вызывая выработку собственных антител. После инфекции в организме остаются «клетки памяти», и в случае последующих столкновений с возбудителем они начинают снова (уже быстрее) продуцировать антитела.
При пассивной иммунизации в организм вводятся уже готовые антитела (гаммаглобулин). Введенные антитела при столкновении с возбудителем «расходуются» (связываются с возбудителем в комплекс «антиген-антитело»).
Пассивная иммунизация показана, когда необходимо в короткие сроки создать иммунитет на непродолжительное время (например, после контакта с больным).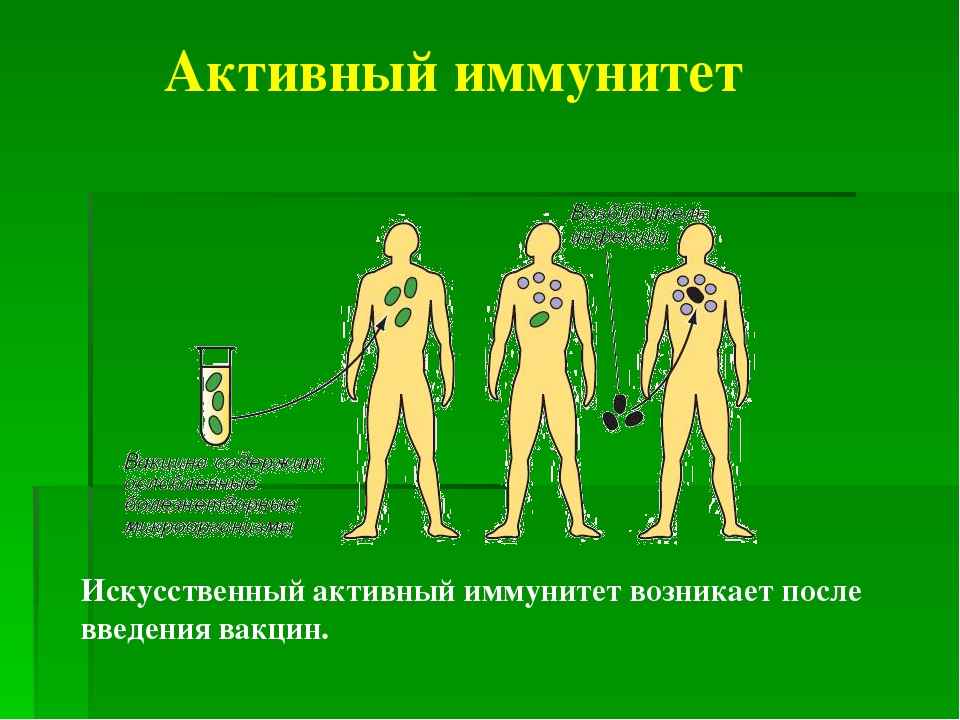
Стерильный и нестерильный иммунитет
После некоторых заболеваний иммунитет сохраняется пожизненно, например, при кори или ветряной оспе. Это так называемый стерильный иммунитет. А в некоторых случаях он сохраняется только до тех пор, пока в организме есть возбудитель (туберкулез, сифилис) — это нестерильный иммунитет.
Регуляция иммунитета
Работа иммунитета во многом определяется состоянием нервной и эндокринной систем организма. Стресс, депрессии угнетают иммунитет, что сопровождается не только повышенной восприимчивостью к различным заболеваниям, но и создает благоприятные условия для развития злокачественных новообразований.
Материал подготовлен на основе информации открытых источников
Искусственный и естественный иммунитеты. Факторы иммунитета.
Иммунитет человека – это единая, целостная система. Все ее клетки работают на один результат – здоровье организма. Тем не менее, условно ученые разделяют его на несколько видов для того, чтобы было проще изучать его и работать с ним. Современная наука выделяет врожденный и приобретенный виды иммунитета. Врожденный мы получаем от родителей, и на него в большой степени влияют генетические факторы. Он остается с нами на всю жизнь в неизменном виде. Другое дело – приобретенный иммунитет. На него можно и нужно воздействовать, развивать, укреплять, тренировать. Чтобы понять, каким образом это делать, нужно детально рассмотреть, как он классифицируется, и откуда берется.
Тем не менее, условно ученые разделяют его на несколько видов для того, чтобы было проще изучать его и работать с ним. Современная наука выделяет врожденный и приобретенный виды иммунитета. Врожденный мы получаем от родителей, и на него в большой степени влияют генетические факторы. Он остается с нами на всю жизнь в неизменном виде. Другое дело – приобретенный иммунитет. На него можно и нужно воздействовать, развивать, укреплять, тренировать. Чтобы понять, каким образом это делать, нужно детально рассмотреть, как он классифицируется, и откуда берется.
Приобретенный иммунитет делится на естественный и искусственный. Логично предположить, что естественный иммунитет приобретается благодаря определенным физиологическим процессам. Каждая болезнь, которую человек переносит, не проходит для организма бесследно. Антигены провоцируют выработку антител, клетки иммунитета, запоминают все, что им приходится делать, чтобы в следующий раз воспользоваться этой информацией. Таким образом, развивается естественный иммунитет. Он может быть активным или пассивным. После перенесенных болезней вырабатывается активный иммунитет. Пассивный естественный иммунитет вырабатывается вследствие передачи матерью иммунной информации новорожденному. Это происходит посредством грудного молока. Поэтому грудное вскармливание нельзя ничем заменить. Для ребенка это очень важная основа здоровья.
Он может быть активным или пассивным. После перенесенных болезней вырабатывается активный иммунитет. Пассивный естественный иммунитет вырабатывается вследствие передачи матерью иммунной информации новорожденному. Это происходит посредством грудного молока. Поэтому грудное вскармливание нельзя ничем заменить. Для ребенка это очень важная основа здоровья.
Искусственный иммунитет также может быть активным и пассивным. Когда человеку вводят вакцину, она активизирует выработку антител, как это происходит во время болезни. Это происходит благодаря тому, что в состав вакцин входят мертвые или ослабленные антигены, которые не могут вызвать болезнь, но могут вызвать иммунный ответ. Следствием всего этого является активный искусственный иммунитет. Бывает и обратная ситуация, когда человеку вводят сыворотку. Сыворотки – это вещества, которые содержит антигены против возбудителей определенных болезней. То есть, при проникновении определенного одноклеточного микроорганизма, иммунным клеткам не нужно формировать антигены, поскольку они уже есть в крови человека.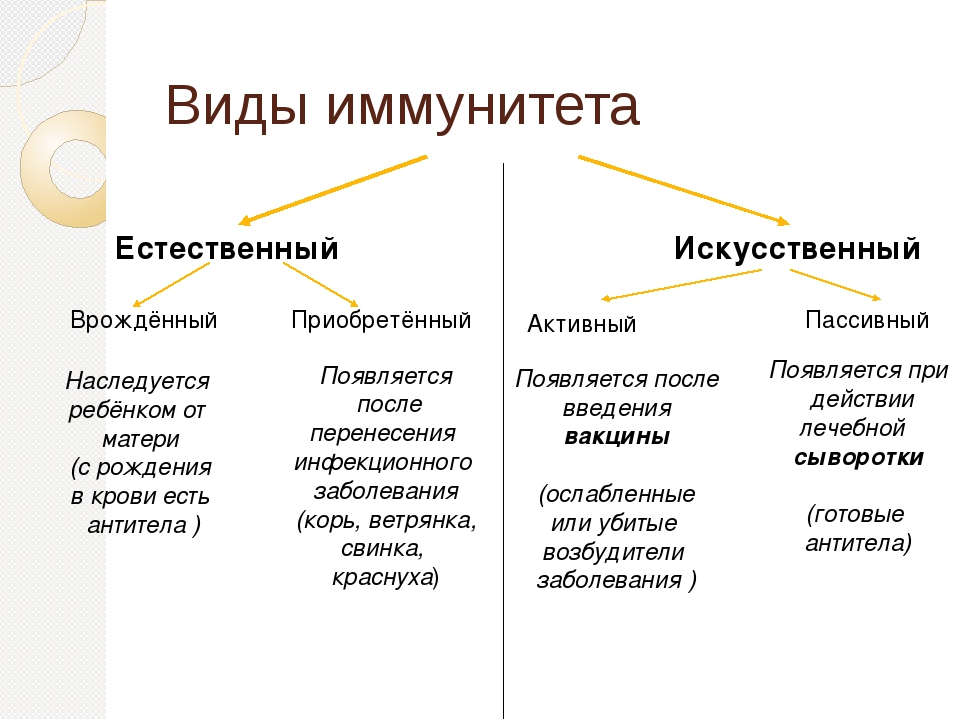 Так формируется пассивный искусственный иммунитет.
Так формируется пассивный искусственный иммунитет.
Факторы иммунитета
Факторы иммунитета – это те «инструменты», которые обеспечивают защиту организма. Они делятся на клеточные, гуморальные и факторы саморегуляции.
Клеточные факторы иммунитета – это кожа и слизистые оболочки, процесс фагоцитоза, клетки-убийцы и видовая реактивность клеток. Все это создает механический барьер для вражеских микроорганизмов, а также поглощает и уничтожает их.
Гуморальные факторы иммунитета – это разнообразные ферменты и другие вещества, которые вырабатываются Т-лимфоцитами и макрофагами. Они содержатся в крови и других биологических жидкостях организма.
Факторы саморегуляции – это способность организма запускать некоторые процессы, которые способствуют излечению от болезни. Это, например, повышение температуры теля, изменение pH поврежденных тканей, выделение слизи, мокроты и другое.
Повышение иммунитета народными средствами
Многие люди испытывают дефицит иммунитета, но прибегать к фармацевтическим препаратам не хотят, объясняя это тем, что лишняя «химия» организму ни к чему. Это мудрое решение, поэтому повышение иммунитета народными средствами не теряет своей актуальности. Надо сказать, что такой метод подходит не всем, и тут большую роль играет внушаемость человека, а также глубина проблемы. Конечно, если речь идет о непродолжительных сезонных простудах, которые не слишком часты, не вызывают осложнений и быстро проходят, то в этом случае повышение иммунитета народными средствами будет эффективным. Если же проблема в серьезном иммунодефиците, который характеризуется частыми инфекционными заболеваниями, непроходящими вялотекущими простудами, слабостью, сонливостью – то нужны более радикальные методы и серьезное обследование.
Это мудрое решение, поэтому повышение иммунитета народными средствами не теряет своей актуальности. Надо сказать, что такой метод подходит не всем, и тут большую роль играет внушаемость человека, а также глубина проблемы. Конечно, если речь идет о непродолжительных сезонных простудах, которые не слишком часты, не вызывают осложнений и быстро проходят, то в этом случае повышение иммунитета народными средствами будет эффективным. Если же проблема в серьезном иммунодефиците, который характеризуется частыми инфекционными заболеваниями, непроходящими вялотекущими простудами, слабостью, сонливостью – то нужны более радикальные методы и серьезное обследование.
Если вам интересно повышение иммунитета народными средствами, мы приведем несколько простых и действенных рецептов, проверенных временем.
2 столовых ложки хвои нужно прокипятить в 500 граммах воды полчаса. Дать настояться и добавить 2 столовые ложки меда, разделить на 2 приема в день.
Витаминное варенье для иммунитета можно приготовить из 500 граммов клюквы, 4 средних яблок и стакана грецких орехов.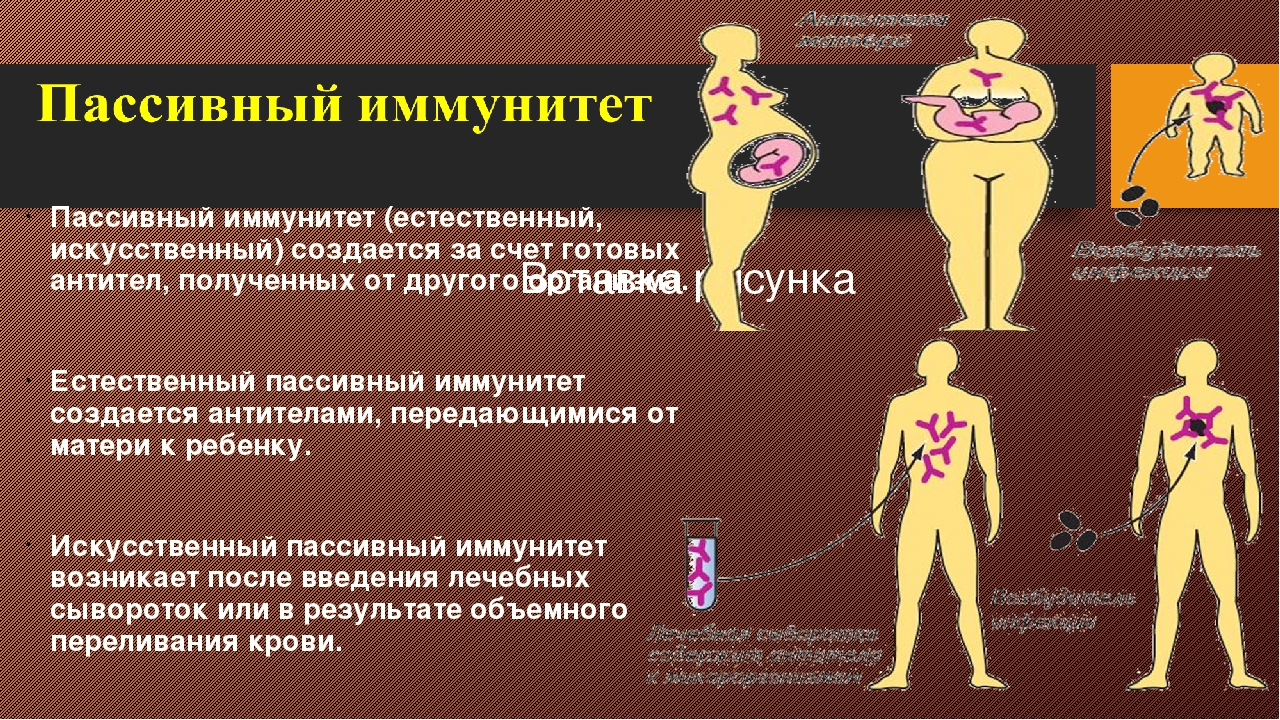 Все нужно измельчить, добавить 2 стакана сахара и полстакана воды. Варить все на медленном огне, чтобы прокипело. Потом разложить в банки и принимать по столовой ложке с чаем 2-3 раза в день.
Все нужно измельчить, добавить 2 стакана сахара и полстакана воды. Варить все на медленном огне, чтобы прокипело. Потом разложить в банки и принимать по столовой ложке с чаем 2-3 раза в день.
3 части сока алоэ, 5 частей меда и 7 частей кагора смешать и настоять в темном месте в течение недели. Принимать смесь по столовой ложке перед каждым основным приемом пищи.
Мы упомянули в этой статье, что иммунитет можно тренировать. Это действительно так, и сегодня для этого не обязательно переносить болезни или вводить дорогостоящие сыворотки и вакцины. Конечно, плановое вакцинирование согласно государственному календарю прививок – это необходимое мероприятие. Каждый обязан привиться и привить детей.
Говоря о тренировке иммунитета, мы имеем в виду снабжение его иммунной информацией, на основе которой работают клетки иммунной системы. Эта информация содержится на особых носителях, трансфер факторах, которые присущи всем млекопитающим. Носители эти состоят из 44 аминокислот – это длинные цепочки, которые способны вместить огромное количество информации. Это иммунная память млекопитающих, в которой сосредоточены знания иммунных клеток обо всех вредоносных микроорганизмах и методах борьбы с ними. Когда иммунитет обладает этими знаниями, он просто не подпускает одноклеточные на пушечный выстрел, сразу уничтожая их. Это самое совершенное оружие против болезней.
Это иммунная память млекопитающих, в которой сосредоточены знания иммунных клеток обо всех вредоносных микроорганизмах и методах борьбы с ними. Когда иммунитет обладает этими знаниями, он просто не подпускает одноклеточные на пушечный выстрел, сразу уничтожая их. Это самое совершенное оружие против болезней.
Трансфер факторы содержатся во многих биологических жидкостях, но основной их источник это молозиво любого млекопитающего. С молозивом матери передают детям иммунную память клеток, таким образом, закладывая прочный фундамент для их здоровья. Именно на этом и основано действие иммуномодулятора Трансфер фактор. Передавая иммунную память, он тренирует иммунитет человека. Это не стимуляция иммунитета, не повышение активности клеток – это разъяснение им их функций. Благодаря тому, что Трансфер фактор действует таким путем, он не представляет никакой опасности, поскольку побочных действий или привыкания вызвать не может. Кроме того, он изготавливается на основе натурального сырья – коровьего молозива, которое издавна использовалось нашими предками для укрепления здоровья. Трансфер факторы добываются из молозива благодаря запатентованной технологии ультрафильтрации.
Трансфер факторы добываются из молозива благодаря запатентованной технологии ультрафильтрации.
Безопасность Трансфер фактора подтверждена Минздравом России, который рекомендует использовать его вне зависимости от возраста, цели и диагноза. Он эффективен как профилактическое средство, и как дополнение к традиционному лечению. Трансфер фактор назначают даже младенцам и будущим мамам, что является лучшим подтверждением его безопасности.
описание, функции, виды и особенности.
Иммунитет — биологическая система защиты организма. Однако немногие знают об отличиях пассивного иммунитета от активного.
Свойства иммунитета
Иммунитет защищает организм от веществ и агентов, вызывающих болезни. Он определяет способность к их обнаружению и обезвреживанию, запоминанию чужеродных организмов, а также формированию клеток – клонов. Они могут бороться с тем или иным вредоносным биоматериалом.
Пассивный и активный иммунитет – отличия
Активный иммунитет развивается путем активизации собственных антител.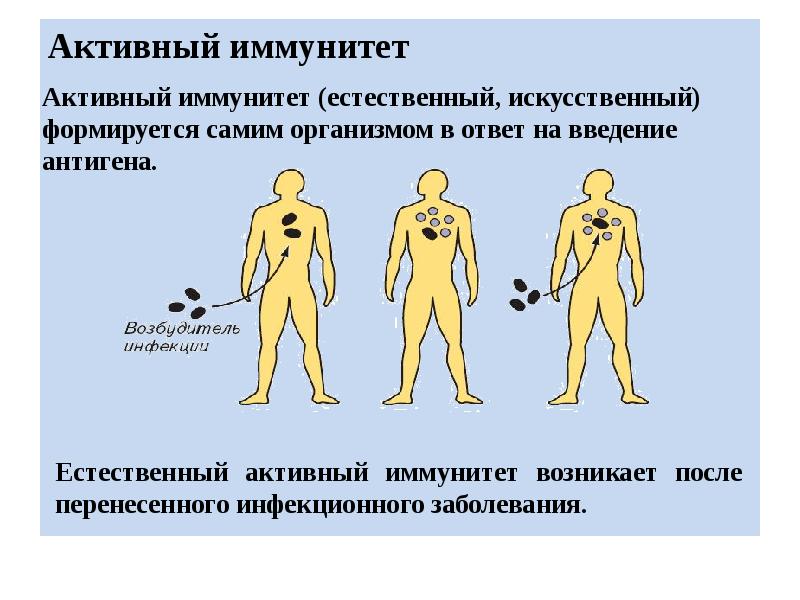 Он вырабатывается долгое время и сохраняется навсегда. Передается по наследству.
Он вырабатывается долгое время и сохраняется навсегда. Передается по наследству.
Пассивный иммунитет приобретается человеком при передаче различными способами специфических антител, задействованных в борьбе против конкретного вида антигенов. Он играет важную роль. Научившись вырабатывать пассивный иммунитет, человечество в прошлые столетия победило болезни, уносящие сотни тысяч жизней. Его выработка и сегодня – основной способ борьбы с опасными заболеваниями.
Пассивный иммунитет бывает естественным и искусственным.
Естественный иммунитет
Естественный иммунитет формируется, когда в организм попадают антитела, продуцированные другим организмом. Ранее считалось, что это происходит только в утробе матери.
В период развития плода материнские иммуноглобулины попадают в его кровь, и младенец рождается на свет уже с естественным иммунитетом, переданным ему матерью.
Защитные частицы новорожденный получает и с материнским молозивом. На его основе производят достаточно эффективные иммуномодулирующие препараты.
Формировать естественный иммунитет помогает и грудное молоко. Оно уступает молозиву по содержанию защитных компонентов, но в нем есть гликопротеины, передающиеся ребенку во время кормления.
Со временем естественная защита, предоставляемая младенцу матерью, постепенно ослабевает.
Искусственный иммунитет
Такая защита вырабатывается путем искусственной стимуляции иммунной системы. С этой целью в организм вводят определенные вакцины или сыворотки. В них присутствуют готовые иммунные частицы, способные противостоять определенному виду антигена.
Внимание! Защита, «созданная» искусственным путем, защищает 2-3 недели. Антитела имеют короткий срок жизни, но быстро формируют сопротивляемость.
Антитела вырабатываются при проникновении инфекции в организм. При этом повышается температура, ощущается недомогание. Справившись с «врагом», лимфоциты запоминают его и при следующей встрече вырабатывают нужные антитела.
Для формирования пассивного искусственного иммунитета человеку могут сделать инъекцию антисыворотки — суспензии частиц антител из крови гомогенизированных домашних животных. Тот же принцип действует, когда после змеиного укуса пострадавшему вводят небольшое количество яда в качестве противоядия.
Трансфер фактор
В середине 20 века открыли защитные частицы трансферфакторного типа. Это носители иммунной памяти организма. Они «записывают» и «хранят» информацию о контактах организма со всеми чужеродными агентами в течение жизни.
У всех позвоночных животных одинаковые трансферфакторы. Передавая их от одного организма другому, передают и весь иммунный опыт донора. Большим успехом ученых-иммунологов считается выделение ими трансферфакторных частиц. На их основе были разработаны специальные иммуномодуляторы. Их использование повышает иммунитет, пониженный из-за неблагоприятных факторов.
Большим успехом ученых-иммунологов считается выделение ими трансферфакторных частиц. На их основе были разработаны специальные иммуномодуляторы. Их использование повышает иммунитет, пониженный из-за неблагоприятных факторов.
Иммунитет: виды, разновидности иммунитета — клеточный и гуморальный, врожденный и приобретенный — 4 февраля 2021
Сильный иммунитет защищает от инфекций, сохраняет кожу упругой, десны, кости и нервы — крепкими, а настроение — бодрым. Иммунитет бывает активный, пассивный, врожденный, специфический, гуморальный, клеточный, приобретенный, но многие люди не понимают, в чем различия.
Чем отличаются виды иммунитета и как его нужно укреплять, рассказывает врач-иммунолог Борисова Татьяна Сергеевна, эксперт маркетплейса витаминов и натуральных товаров для здорового образа жизни iHerb.
Какой бывает иммунитет: врожденный и приобретенный
Существует две основных «категории» иммунитета — врожденный и приобретенный. У животных и растений первый считается ключевым, у людей эти виды примерно равны по значимости.
Врожденный, или неспецифический иммунитет — первая линия обороны организма. Он защищает организм с помощью различных видов фагоцитов, лейкоцитов, макрофагов и тучных клеток, которые участвуют в развитии аллергической реакции. Врожденный иммунитет срабатывает при первом проникновении микроба или бактерии. Но он не становится крепче или слабее: это своеобразная настройка, которая каждый раз работает одинаково.
shutterstock.comПриобретенный иммунитет, он же адаптивный или специфический, появился позже. Он активируется после врожденного, если возбудитель инфекции преодолел первую линию обороны. Основной механизм приобретенного иммунитета — выработка антител, которую обеспечивают лимфоциты. Этот иммунитет действует более избирательно и за счет иммунной памяти может стать крепче со временем. При первой встрече с антигеном часть лимфоцитов сохраняет информацию, и в следующий раз организм распознает его и реагирует быстрее, не позволяя болезни развиться. По такому принципу работает вакцинация.
Активный иммунитет вырабатывается после перенесенного заболевания или введения вакцины. Пассивный — с молоком матери, а во взрослом возрасте после введения сыворотки с готовыми антителами. Клеточный иммунный ответ происходит за счет фагоцитов и лимфоцитов, а гуморальный — за счет антител.
Врожденный и приобретенный иммунитет работают в тандеме, поэтому укрепить один из них нельзя. Не совсем правильно говорить «укрепить иммунитет», это как сказать «починить машину». Ведь ломается не машина, а конкретные детали и механизмы. То же самое с организмом: укрепить можно состояние органов иммунной системы и работу конкретных реакций.
Виды иммунитета: клеточный и гуморальный
Еще есть клеточный иммунитет, который связан с клетками организма. В его случае иммунный ответ организма происходит без участия антител и системы комплемента.
Т-лимфоциты в составе этого иммунитета вырабатывают рецепторы в мембранах клетки, которые реагируют на инородный раздражитель. Клеточный иммунитет «специализируется» на вирусах, грибах, опухолях различной этиологии, различных микроорганизмах, проникших в клетку.
Клеточный иммунитет «специализируется» на вирусах, грибах, опухолях различной этиологии, различных микроорганизмах, проникших в клетку.
Многие также слышали про гуморальный иммунитет. Главное отличие от клеточного — в местонахождении объектов воздействия. Гуморальному иммунитету помогают В-лимфоциты, которые образуются у взрослых людей в костном мозге. Активируют В-лимфоциты чужеродные агенты или Т-клетки, когда они встречаются с бактериями и патогенными агентами в кровяном или лимфатическом русле.
Как укрепить иммунитет
Поддерживайте уровень витаминов
Дефицит любого полезного вещества приводит к неполадкам разной степени в работе иммунной системы. Особенно она зависит от нескольких витаминов и микроэлементов.
Витамин С — участвует в выработке лимфоцитов, стимулирует активность макрофагов, выработку антител и интерферона, белка, который препятствует размножению вируса. Это мощный антиоксидант, который обеспечивает общую защиту клеток от внешних раздражителей.
Витамин D — стимулирует работу лимфоцитов, моноцитов, макрофагов. В этих клетках находятся рецепторы к витамину D. Стимулирует выработку антимикробных белков на слизистых в верхних дыхательных путях, защищая организм от заражения воздушно-капельным путем.
Витамин А — помогает формировать местный иммунитет, на коже и слизистых которые считаются первым и главным барьером на пути инфекции.
shutterstock.comЦинк, селен, медь и железо — ключевые микроэлементы для нормальной работы иммунной системы. Цинк препятствует воспалительным процессам в дыхательных путях и стимулирует активность лимфоцитов. Селен ускоряет распространение лимфоцитов и препятствует возникновению опухолей. Медь необходима для выработки и распределения в тканях нейтрофилов, а также для усвоения железа. Железо стимулирует активность нейтрофилов и макрофагов, участвует в созревании лимфоцитов. Важно контролировать уровень железа в организме. Если принимать препараты железа в период инфекции, состояние организма ухудшится.
Чтобы точно узнать, каких именно веществ не хватает в вашем организме, рекомендуется сдать анализы на уровень содержания основных витаминов и микроэлементов, а витаминные комплексы подбирать вместе с врачом.
Добавляйте в рацион больше клетчатки
В нашей стране большинство фруктов и овощей мы можем купить вне сезона, но это не очень полезно для здоровья. Зимой фрукты и овощи до того, как попасть на прилавки, долго лежат на складе или едут в контейнерах, выращиваются на почвах со стимуляторами. В результате в них содержится менее 50% полезных веществ. Мы получаем переизбыток сахара и фруктозы, к которой организм зимой не готов. Также образуется избыток лептинов, которые содержатся в свежих овощах. Организм способен нейтрализовать этот избыток около трех месяцев, но не весь год. Поэтому важно добавлять в рацион сезонные продукты, характерные для климата, где вы родились, заготовки, квашеные и маринованные овощи: лептины в их составе переработаны бактериями.
Сокращайте сладкие продукты. Сахар — питательная среда для роста патогенных бактерий и грибов. Также сахар поддерживает воспалительный процесс посредством работы инсулина. Хронические кандидозы часто выглядят как рецидивирующая молочница, перхоть, аллергия, насморк, усталость, туман в голове, колиты, панкреатиты и прочие воспалительные процессы. Выход: ограничить употребление сладкого. Особенно в сезон простуд.
Занимайтесь спортом
Кровь и лимфа застаиваются, если человек много сидит и ведет малоподвижный образ жизни. Застои нарушают циркуляцию лимфы и крови: иммунные клетки медленнее добираются до точки, куда проник возбудитель инфекции. Токсины, бактерии и вирусы остаются в организме, если лимфатическая система прекращает циркулировать и очищаться. Это может провоцировать синдром интоксикации, в более тяжелых случаях — реакцию Герксгеймера (среди симптомов — повышение температуры, озноб, снижение давления, тахикардия, тошнота, головная боль, боль в мышцах).
Регулярные упражнения обеспечивают нормальное кровообращение и вентиляцию легких. Тренировки не должны быть высокоинтенсивными, считается и получасовая прогулка в среднем темпе, и утренняя разминка. Признаком достаточности физической нагрузки считается легкий пот.
shutterstock.comСледите за качеством сна
Сон не только необходим для полноценного восстановления организма и нормальной работы нервной системы. Пока мы спим, лимфоциты обрабатывают информацию о вредоносных клетках и веществах и при следующей встрече быстрее их распознают. Во сне формируется иммунная память, без которой все, что иммунная система познала днем, пройдет мимо.
Это основные факторы нормальной работы иммунной системы. Чтобы организм был устойчив перед инфекциями и внешними раздражителями, недостаточно разобраться только со сном. Нужно учитывать все факторы сразу, и образ жизни будет здоровым.
Канал про ЗОЖ в телеграме! Подписывайся
Иммунитет — урок. Биология, Человек (8 класс).
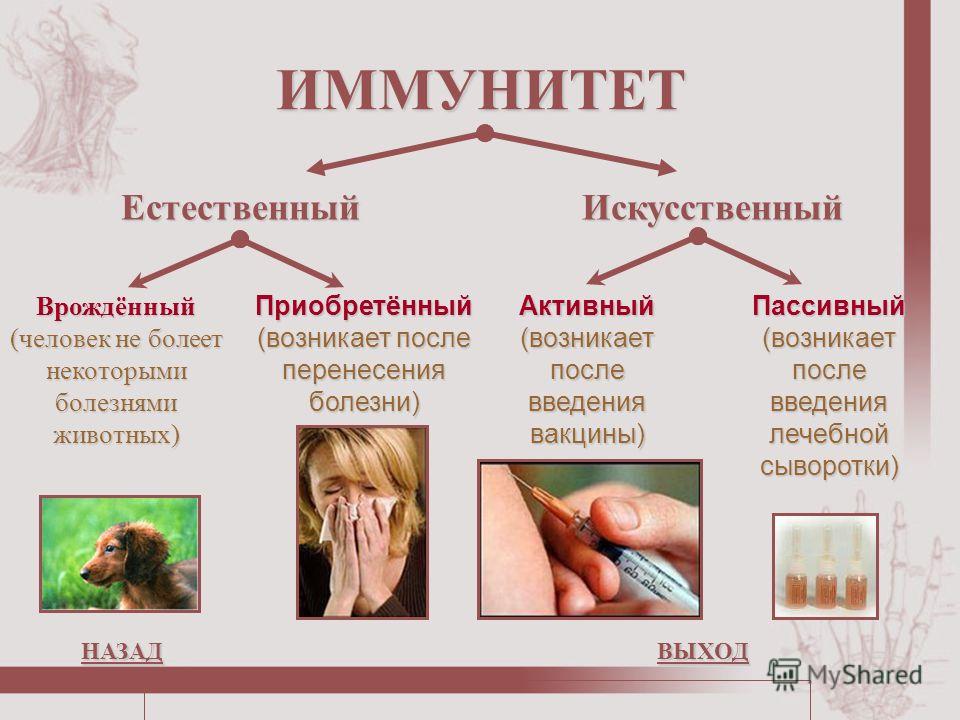
Фагоцитоз и выработка антител лейкоцитами — единый защитный механизм, названный иммунитетом.
Иммунитет — система защиты организма от чужеродных веществ и других организмов.
Иммунные механизмы обеспечивают защиту от болезнетворных вирусов и бактерий, уничтожают погибшие и переродившиеся клетки.
Иммунные реакции могут оказывать и отрицательное влияние. Так, они могут быть причиной осложнений при переливании крови и трансплантации органов.
Очень важную роль в формировании иммунитета играет тимус, или вилочковая железа. Эта железа находится за грудиной и хорошо функционирует только у детей.
Рис. \(1\). Тимус
Виды иммунитета
Защитные механизмы различаются по происхождению, способам воздействия на антиген и продолжительности действия.
Рис. \(2\). Схема «Виды иммунитета»
Естественный иммунитет
У людей есть врождённый иммунитет ко многим заболеваниям. Врождённый иммунитет передаётся по наследству от родителей.
Врождённый иммунитет передаётся по наследству от родителей.
Пример:
человек не болеет чумой собак, так у него с рождения имеется иммунитет к возбудителю этой болезни.
Если человека перенес инфекционную болезнь, то в его организме тоже формируется иммунитет (сохраняются клетки памяти, способные распознавать возбудителя болезни). Такой иммунитет получил название приобретённого. Если этот же микроб через некоторое время снова окажется в организме, он тут же уничтожается.Пример:
переболев в детстве ветрянкой, человек уже повторно не болеет этой болезнью.
Врождённый иммунитет и иммунитет, приобретённый после болезни, называют естественным.
Естественным является также иммунитет, полученный новорожденным ребёнком от матери. Через плаценту во время беременности, а после рождения с грудным молоком к ребёнку попадают антитела, которые защищают его в первый год жизни от инфекционных заболеваний.
Искусственный иммунитет
Для защиты от многих инфекционных заболеваний (оспы, коклюша, полиомиелита, дифтерии, гриппа и др. ), человеку делают прививки — вводят вакцину (убитых или сильно ослабленных возбудителей болезни) и таким образом создают искусственный иммунитет.
), человеку делают прививки — вводят вакцину (убитых или сильно ослабленных возбудителей болезни) и таким образом создают искусственный иммунитет.
При введении вакцины у человека возникает лёгкая реакция на возбудителя болезни и вырабатываются клетки памяти. При следующем попадании этого возбудителя клетки памяти быстро распознают его и выделяют антитела, которые препятствуют развитию заболевания. Это — активный иммунитет. Прививки спасли жизни многим людям.
Первую прививку провёл в \(1769\) г. английский врач Эдуард Дженнер. Это была прививка от оспы — тяжёлой вирусной болезни, оставляющей на коже многочисленные рубцы. Дженнер обратил внимание, что во время эпидемий оспы практически не заболевают крестьянки, которые часто заражались от животных «коровьей оспой». Дженнер ввёл восьмилетнему мальчику «коровью оспу», а через \(1,5\) месяца заразил его человеческой оспой. Ребёнок не заболел. Так появились прививки.
Если человек уже заболел, то используют лечебные сыворотки, содержащие готовые антитела. Для получения лечебной сыворотки берут плазму крови переболевших людей или животных. В этом случае говорят о пассивном иммунитете.
Пример:
лечебные сыворотки используют для спасения людей от смертельно опасных болезней, например ботулизма, дифтерии. Их используют также при укусах змей (кобры, гюрзы, эфы).
Сыворотка действует недолго. Через некоторое время антитела разрушаются и её действие прекращается.Лечебная сыворотка — это препарат плазмы крови без фибриногена, содержащий готовые антитела, которые образовались в крови животного (или человека), ранее заражённого данным возбудителем (перенёсшего данное заболевание).
Неспецифический и специфический иммунитет
Неспецифический иммунитет практически одинаков у всех представителей одного вида. Он направлен против любых чужеродных веществ и обеспечивает борьбу с инфекцией на ранних этапах её развития, когда специфический иммунитет ещё не сформировался.
Неспецифический иммунитет врождённый. Он обеспечивается кожным покровом и слизистыми оболочками.
Специфический иммунитет основан на распознавании конкретного антигена лимфоцитами и его уничтожении. У каждого человека этот тип иммунитета индивидуален. Он формируется постепенно в результате реакции иммунной системы на различные антигены, с которыми контактирует организм.
Специфический иммунитет обеспечивается клетками памяти (особыми лимфоцитами), которые сохраняются в организме после перенесённой инфекции или после прививки на долгое время. Эти клетки распознают возбудителя болезни при его повторном попадании в организм и быстро начинают вырабатывать антитела, препятствуя развитию болезни.
Источники:
Рис. 1. Тимус: https://www.shutterstock.com/da/image-illustration/male-anatomy-human-thymus-xray-view-83549896
Рис. 2. Схема «Виды иммунитета»: https://image.shutterstock.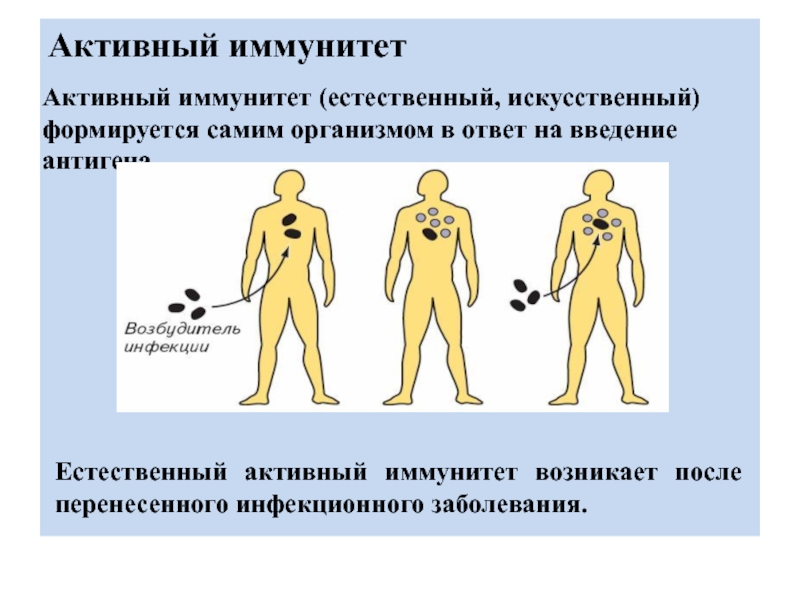 com/image-vector/illustration-biology-medical-acquired-immunity-600w-1663099516.jpg
com/image-vector/illustration-biology-medical-acquired-immunity-600w-1663099516.jpg
НЕПРАВДА: Вакцины, в отличие от природного инфицирования, не создают коллективный иммунитет
Проверка фейков в рамках партнерства с Facebook
В сети распространяют фейк, который манипулирует темой коллективного иммунитета и агитирует против вакцинации, убеждая, что прививки неэффективны, опасны и не способствуют развитию коллективного иммунитета.
Впрочем, это неправда. Далее апеллируем к основным ложным утверждениям.
Коллективный иммунитет можно развить двумя способами. Первый — так называемый естественный, когда большое количество людей переболело и развило индивидуальный иммунитет. Второй — путем массовой вакцинации, когда большая часть населения получила вакцину и так же развила индивидуальный иммунитет.
И заражения, и вакцины на клеточном уровне действуют по схожему принципу. Организм замечает угрозу — и B-лимфоциты вырабатывают против нее антитела, которые и обеспечивают иммунитет. В результате этот механизм запоминается, поэтому в случае нового заражения тело вспомнит, как себя защитить.
В результате этот механизм запоминается, поэтому в случае нового заражения тело вспомнит, как себя защитить.
Единственная разница в том, что прививки — это более слабая или неактивная версия возбудителя инфекции. Прививки только симулирует заболевание, а естественное заражение вызывает полноценную болезнь, которая может стать летальной. Именно поэтому вакцинация — безопасный способ развития коллективного иммунитета. Программы вакцинации ежегодно спасают 2-3 миллиона жизней.
Утверждение о возможности развития коллективного иммунитета исключительно естественным путем — ложное и представляет угрозу для общества.
После некоторых болезней, например, кори, пожизненный иммунитет вырабатывается, а после других, например, гриппа — нет. Марк Дженкинс, иммунолог из Университета Миннесоты, объясняет, что организм на самом деле не «забывает», как бороться с болезнью, на которую ранее переболел. Повторное инфицирование объясняют не потерей иммунитета, а мутацией патогена (то есть организм должен бороться с похожим, но другим патогеном), или же тем, что организм сохраняет меньшее количество клеток, которые готовы бороться с патогеном. Таким образом, вирус гриппа быстро мутирует — поэтому болезнь или вакцинация не защищает от гриппа в следующем сезоне. А вот вирус полиомиелита НЕ мутирует быстро, поэтому вакцинация позволила почти побороть болезнь.
Таким образом, вирус гриппа быстро мутирует — поэтому болезнь или вакцинация не защищает от гриппа в следующем сезоне. А вот вирус полиомиелита НЕ мутирует быстро, поэтому вакцинация позволила почти побороть болезнь.
Есть исследования, которые показывают, что естественный иммунитет может быть более длительным, чем искусственный (путем вакцинации). Например, в случае коклюша природный иммунитет длится 4-20 лет, а искусственный — 4-12 лет. Впрочем, ключевой вопрос — цена приобретения естественного иммунитета. Например, полиомиелит может парализовать на всю жизнь. Беременные, страдающие краснухой, могут родить детей с нарушениями слуха, зрения, сердца, легких, печени и других органов. Осложнением после кори может быть энцефалит — воспаление головного мозга, которое может привести к потере слуха и нарушению интеллектуального развития.
Из-за того, что искусственный иммунитет не гарантирует защиту на всю жизнь, проводят ревакцинацию. Ее необходимость зависит от свойств вакцины. Для некоторых вакцин уровень антител со временем может снижаться, что вызывает необходимость ревакцинации для поддержания иммунной реакции на высоком уровне и постоянной защиты организма от заболевания.
Для некоторых вакцин уровень антител со временем может снижаться, что вызывает необходимость ревакцинации для поддержания иммунной реакции на высоком уровне и постоянной защиты организма от заболевания.
Однако она нужна не для всех болезней и не каждые два года, как указано в публикации. В Украине все обязательные вакцины, кроме противотуберкулезной, вводят более одного раза. Некоторые из них создают базовый иммунитет после двух или трех доз, их введение — это первичный комплекс вакцинации.
Вакцины имеют доказанную эффективность, и защита от болезней не исчезает, если вовремя получать все дозы вакцины. Благодаря вакцинации оспа полностью исчезла, случаи заражения полиомиелитом упали на 99%, количество смертей от столбняка снизилась на 96%, от кори — на 75%. На графиках можно наглядно увидеть зависимость между ростом уровня вакцинации против дифтерии, коклюша и столбняка, и снижением заболеваемости этими болезнями.
Мифы о прививках мы разоблачали и раньше: здесь, здесь и здесь.
Количество смертей, вызванных вакцинацией — а не другими причинами, которые совпали по времени с вакцинацией — низкая. Даже если причиной смерти стала вакцина, то это чаще всего связано не с ее составом, производством или доставкой, а с врачебной халатностью. Поэтому на уровне населения считается, что низкий риск смерти компенсируется преимуществами, которые дает общая иммунизация.
Обобщенные исследования, в которых сравнивают именно уровень смертности среди вакцинированных и невакцинированных групп населения показывают, что общая смертность среди вакцинированных людей несколько ниже, чем среди населения в целом, и в целом имеет те же причины. То есть, за редкими случаями смертей, которые могут быть отнесены к побочным эффектам вакцин, исследования не выявляют какой-то специфической повышенной смертности вакцинированных людей.
Что касается побочных эффектов от вакцин, то тяжелые встречаются совсем редко, большинство — легкие, локальные и не требуют лечения. Это нормальная реакция организма, ведь после прививки он борется с возбудителем болезни и таким образом вырабатывает иммунитет.
Это нормальная реакция организма, ведь после прививки он борется с возбудителем болезни и таким образом вырабатывает иммунитет.
Из-за отсутствия коллективного иммунитета происходят вспышки и эпидемии болезней, которых можно было бы предотвратить путем вакцинации. Это, например, касается вспышек кори по всему миру в 2019 году, эпидемии дифтерии в постсоветских странах в 1990-1994, эпидемии краснухи в Японии в 2013 году, а также периодических вспышек других болезней в разных странах. Причина — недостаточный уровень вакцинации.
11.12C: Искусственный иммунитет — Биология LibreTexts
- Последнее обновление
- Сохранить как PDF
- Ключевые моменты
- Ключевые термины
Искусственный иммунитет – это средство, с помощью которого организму придается иммунитет к заболеванию путем преднамеренного воздействия небольших его количеств.
Цели обучения
- Описать искусственно приобретенный иммунитет и способы его получения
Ключевые моменты
- Наиболее распространенная форма искусственного иммунитета классифицируется как активная и осуществляется в виде прививок, обычно вводимых детям и молодым людям.
- Пассивная форма искусственного иммунитета включает в себя введение антитела в систему после того, как человек уже был заражен болезнью, что в конечном итоге облегчает текущие симптомы болезни и предотвращает повторное возникновение.
- Как только организм успешно избавится от болезни, вызванной определенным патогеном, повторное заражение тем же патогеном окажется безвредным.
Основные термины
- гамма-глобулин : класс белков в крови, идентифицируемый по их положению после электрофореза белков сыворотки, например антитела
- анафилактический шок : Тяжелая и быстрая системная аллергическая реакция на аллерген, сужающая трахею и препятствующая дыханию.

- коллективный иммунитет : защита, предоставляемая населению от эпидемии инфекционного заболевания, когда достаточное количество населения иммунизировано или иным образом вырабатывается иммунитет к нему
Иммунитет – это состояние защиты от инфекционного заболевания, обеспечиваемое либо иммунным ответом, вызванным иммунизацией, либо предшествующей инфекцией, либо другими неиммунологическими факторами.
Искусственный иммунитет может быть активным или пассивным.
Рис. Иммунитет : Естественный иммунитет возникает при контакте с возбудителем болезни, когда контакт не был преднамеренным, тогда как искусственный иммунитет развивается только при преднамеренном воздействии воздействия.Как естественный, так и искусственный иммунитет можно подразделить в зависимости от продолжительности действия защиты. Пассивный иммунитет недолговечен и обычно длится всего несколько месяцев, тогда как защита с помощью активного иммунитета длится намного дольше, а иногда и пожизненно.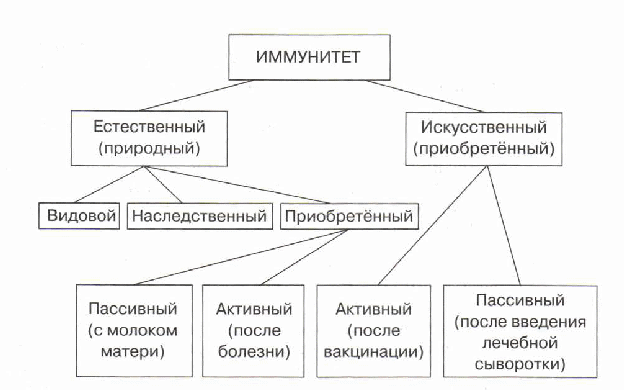
Искусственно приобретенный пассивный иммунитет — это немедленная, но кратковременная иммунизация, обеспечиваемая введением антител, таких как гамма-глобулин, которые не вырабатываются клетками реципиента. Эти антитела вырабатываются у другого человека или животного, а затем вводятся другому человеку.Антисыворотка — это общий термин, используемый для препаратов, содержащих антитела.
Искусственная активная иммунизация заключается в том, что микроб или его части вводятся человеку до того, как он сможет принять его естественным путем. Если используются целые микробы, они представляют собой предварительно обработанные аттенуированные вакцины. Эта вакцина стимулирует первичный ответ против антигена у реципиента, не вызывая симптомов заболевания.
Искусственная пассивная иммунизация обычно проводится путем инъекции и используется в случае недавней вспышки определенного заболевания или в качестве неотложного лечения токсичности, например, при столбняке.Антитела могут быть получены у животных, что называется «сывороточной терапией», хотя существует высокая вероятность анафилактического шока из-за иммунитета против самой сыворотки животных. Таким образом, гуманизированные антитела, продуцируемые культурой клеток in vitro, используются вместо них, если они доступны.
Таким образом, гуманизированные антитела, продуцируемые культурой клеток in vitro, используются вместо них, если они доступны.
Первое упоминание об искусственном иммунитете было связано с болезнью, известной как оспа. Люди подверглись воздействию незначительного штамма оспы в контролируемой среде. Как только их тела выработали естественный иммунитет или устойчивость к ослабленному штамму оспы, вероятность заражения более смертельными штаммами этой болезни значительно уменьшилась.По сути, пациентам давали болезнь, чтобы помочь бороться с ней в более позднем возрасте. Хотя этот метод был эффективным, у ученых того времени не было реальных научных знаний о том, почему он работал.
ЛИЦЕНЗИИ И СВИДЕТЕЛЬСТВА
CC ЛИЦЕНЗИОННЫЙ КОНТЕНТ, РАСПРОСТРАНЕННЫЙ РАНЕЕ
CC ЛИЦЕНЗИОННОЕ СОДЕРЖИМОЕ, ОПРЕДЕЛЕННОЕ АВТОРСТВО
Активный и пассивный иммунитет: различия и определение
Иммунитет определяется как способность организма защищать себя от инфекционного заболевания.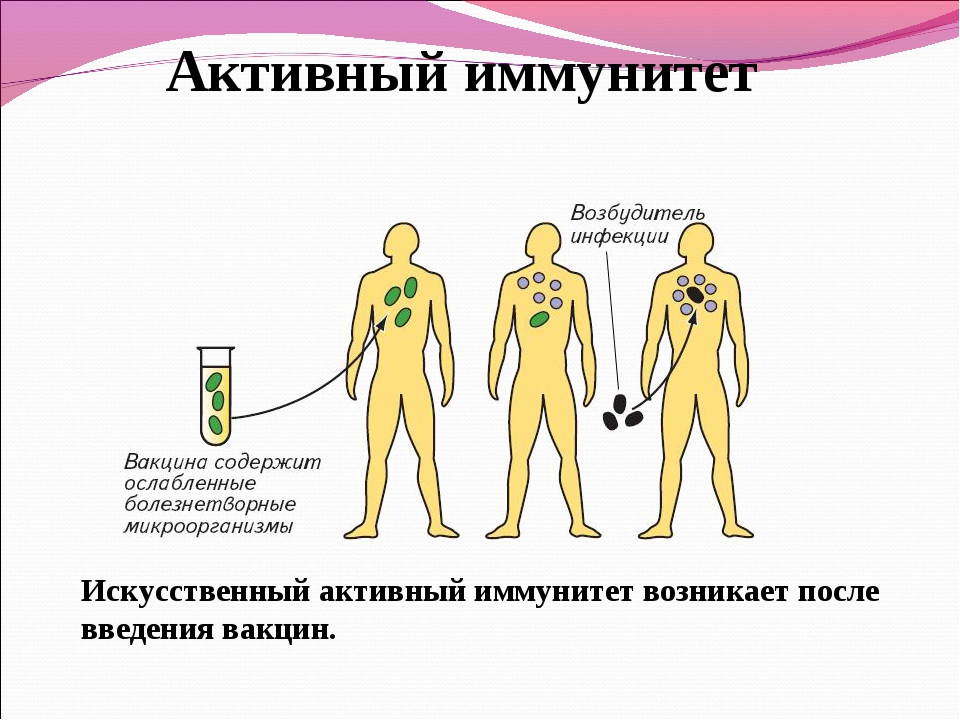 Когда вы невосприимчивы к болезни, ваша иммунная система может бороться с инфекцией от нее.
Когда вы невосприимчивы к болезни, ваша иммунная система может бороться с инфекцией от нее.
Иммунитет бывает врожденным или адаптивным. Врожденный иммунитет, также известный как естественный или генетический иммунитет, — это иммунитет, с которым организм рождается. Этот тип иммунитета закодирован в генах. Генетический иммунитет защищает организм на протяжении всей его жизни. Врожденный иммунитет состоит из:
- Внешняя защита : Известная как первая линия защиты, внешняя защита защищает организм от воздействия патогенов.Внешняя защита включает такие вещи, как кожа, слезы и желудочная кислота.
- Внутренняя защита : Известная как вторая линия защиты, внутренняя защита воздействует на патоген после его проникновения в организм. Внутренняя защита включает в себя такие вещи, как воспаление и лихорадка.
Адаптивный иммунитет, также известный как приобретенный иммунитет, является третьей линией защиты. Адаптивный иммунитет защищает организм от конкретного возбудителя. Адаптивный иммунитет далее делится на две подгруппы: активный иммунитет и пассивный иммунитет.В этой статье мы рассмотрим активный и пассивный иммунитет.
Адаптивный иммунитет далее делится на две подгруппы: активный иммунитет и пассивный иммунитет.В этой статье мы рассмотрим активный и пассивный иммунитет.
Что такое активный иммунитет?
Активный иммунитет определяется как иммунитет к патогену, возникающий после воздействия указанного патогена.
Когда организм подвергается воздействию нового возбудителя болезни, В-клетки, тип лейкоцитов, вырабатывают антитела, которые помогают уничтожить или нейтрализовать возбудитель болезни. Антитела представляют собой Y-образные белки, которые способны связываться с участками токсинов или патогенов, называемыми антигенами.
Антитела специфичны для конкретного заболевания, что означает, что каждое антитело защищает организм только от одного возбудителя заболевания. Например, антитела, вырабатываемые при обнаружении организмом вируса, вызывающего эпидемический паротит, не обеспечивают никакой защиты от вирусов простуды или гриппа.
Диаграмма, показывающая различные типы активного и пассивного иммунитета
Когда В-клетки сталкиваются с патогеном, они создают клетки памяти в дополнение к антителам. Клетки памяти представляют собой тип В-клеток, вырабатываемых после первичной инфекции, которые могут распознавать патоген.Клетки памяти могут сохраняться десятилетиями, ожидая в организме повторного вторжения патогена. Когда организм подвергается воздействию патогена во второй раз, иммунный ответ становится более устойчивым, быстро воздействуя на возбудителя болезни.
Клетки памяти представляют собой тип В-клеток, вырабатываемых после первичной инфекции, которые могут распознавать патоген.Клетки памяти могут сохраняться десятилетиями, ожидая в организме повторного вторжения патогена. Когда организм подвергается воздействию патогена во второй раз, иммунный ответ становится более устойчивым, быстро воздействуя на возбудителя болезни.
Иммунитет не возникает сразу после заражения. Для развития активного иммунитета могут потребоваться дни или недели после первого контакта. Но как только это произойдет, защита может длиться всю жизнь.
Активный иммунитет может возникнуть одним из двух способов: естественным путем или в результате иммунизации.
Естественный иммунитет
Естественный иммунитет возникает, когда человек заражается болезнью. Возьмем, к примеру, человека, который заразился ветряной оспой. После первоначального заражения организм вырабатывает иммунитет против болезни. Этот естественный активный иммунитет является причиной того, что люди, заболевшие ветряной оспой, в течение многих десятилетий невосприимчивы к этой болезни.
Иммунитет, вызванный вакциной
Также известный как искусственный активный иммунитет, человек может выработать устойчивость к болезни после иммунизации.Иммунизация определяется как процесс, посредством которого человек становится защищенным от определенного заболевания посредством введения вакцины.
Вакцины используют ослабленную или мертвую форму болезни для стимуляции иммунного ответа. Вакцины обычно вводят с помощью инъекции. Однако существуют вакцины, вводимые через рот или в виде назального спрея.
Когда иммунная система человека обнаруживает ослабленный или мертвый возбудитель, она начинает предпринимать шаги по его уничтожению. Это включает в себя формирование новых антител и клеток памяти, специфичных для этого патогена.В будущем, если организм подвергнется воздействию указанного возбудителя, будут созданы антитела для защиты организма.
Вакцинация и иммунитет необходимы для защиты больших групп людей от инфекционных заболеваний. Например, вакцина против гриппа ежегодно предотвращает заражение миллионов людей гриппом.
Что такое пассивный иммунитет?
Пассивный иммунитет — это защита от болезней, обеспечиваемая антителами, созданными вне организма. Пассивный иммунитет:
- Не требует предварительного контакта с возбудителем болезни
- Вступает в силу немедленно
- Непродолжительно (до нескольких месяцев)
Чем отличается искусственный пассивный иммунитет от естественного пассивного иммунитета?
Пассивный иммунитет бывает материнским или искусственным.
Материнский пассивный иммунитет или естественный пассивный иммунитет — это иммунитет, передающийся от матери к ребенку. Перед рождением ребенка через плаценту проходят антитела, чтобы защитить ребенка от болезней. После рождения младенец продолжает получать пассивный иммунитет к болезням за счет антител, обнаруженных в грудном молоке.
Искусственный пассивный иммунитет возникает из-за введения антител, созданных другим человеком или животным. Эти препараты, содержащие антитела, называются антисыворотками.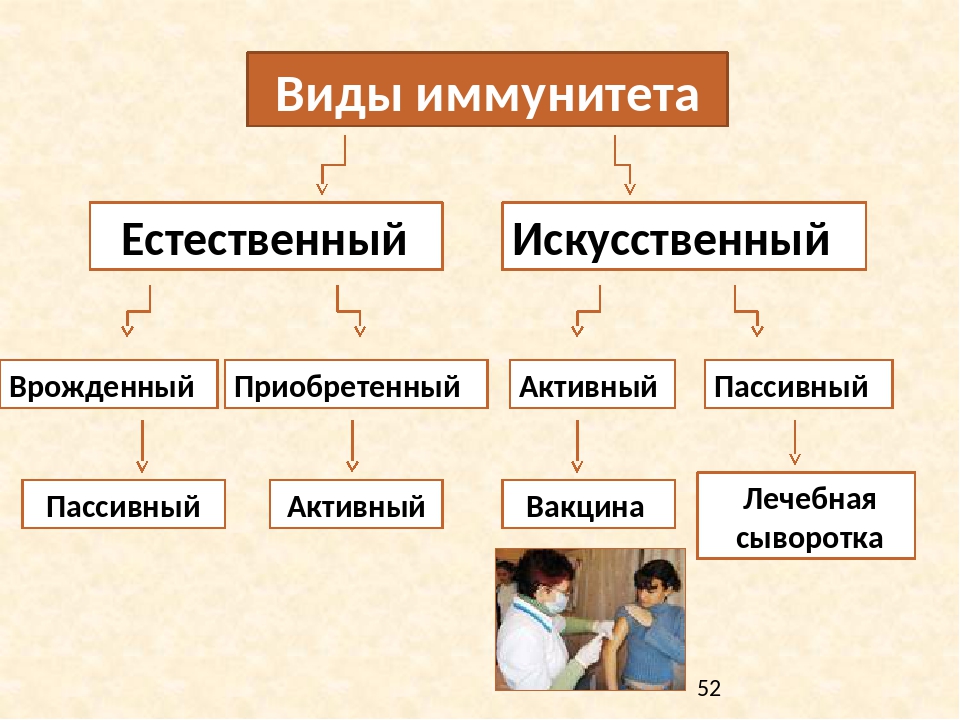 Вакцина против бешенства и противоядие от змей — два примера антисывороток, дающих пассивный иммунитет.
Вакцина против бешенства и противоядие от змей — два примера антисывороток, дающих пассивный иммунитет.
Active VS пассивный иммунитет
| 0 |
пассивный иммунитет | | | | введены из-за пределов тела | результаты | вступает в силу | со временем (обычно несколько недель) | Немедленно | Длительность действия | От долгосрочной до пожизненной | Краткосрочная | 9000 | Да | Нет | |
Пассивная иммунизация | История вакцин
В этой статье предполагается знакомство с терминами антитело, антиген, иммунитет, и патоген . См. определения в Глоссарии.
См. определения в Глоссарии.
Человек может стать невосприимчивым к определенному заболеванию несколькими способами. При некоторых заболеваниях, таких как корь и ветряная оспа, заболевание обычно приводит к пожизненному иммунитету к нему. Вакцинация – еще один способ стать невосприимчивым к болезни. Оба способа получения иммунитета, либо от болезни, либо от вакцинации, являются примерами активного иммунитета . Активный иммунитет возникает, когда иммунная система человека вырабатывает антитела и активирует другие иммунные клетки к определенным патогенам.Если человек снова столкнется с этим патогеном, долгоживущие специфические для него иммунные клетки уже будут готовы бороться с ним.
Другой тип иммунитета, называемый пассивным иммунитетом, возникает, когда человеку вводят чужие антитела. Когда эти антитела вводятся в организм человека, «одолженные» антитела помогают предотвратить или бороться с некоторыми инфекционными заболеваниями. Защита, обеспечиваемая пассивной иммунизацией, недолговечна и обычно длится всего несколько недель или месяцев.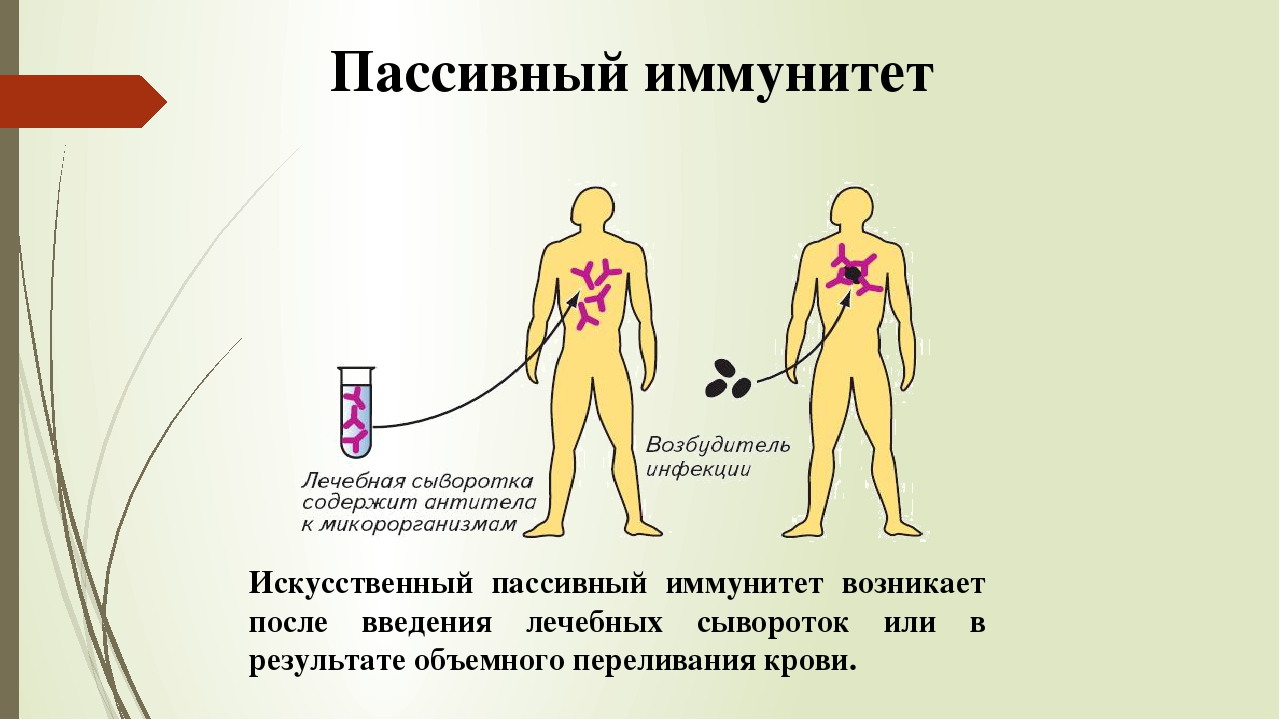 Но это помогает защитить сразу.
Но это помогает защитить сразу.
Натуральный Младенцы получают пользу от пассивного иммунитета, приобретаемого, когда материнские антитела и лейкоциты, борющиеся с патогенами, проникают через плаценту и достигают развивающихся детей, особенно в третьем триместре. Вещество, называемое молозивом, которое младенец получает во время кормления грудью в первые дни после рождения и до того, как мать начинает вырабатывать «настоящее» грудное молоко, богато антителами и обеспечивает защиту младенца.Грудное молоко, хотя и не так богато защитными компонентами, как молозиво, также содержит антитела, которые передаются грудному ребенку. Однако эта защита, обеспечиваемая матерью, недолговечна. В течение первых нескольких месяцев жизни уровень материнских антител у младенца падает, а защита ослабевает примерно к шестимесячному возрасту.
Искусственный Пассивный иммунитет можно индуцировать искусственно, когда антитела вводятся в виде лекарства неиммунному человеку. Эти антитела могут поступать из объединенных и очищенных продуктов крови иммунных людей или иммунных животных, отличных от человека, таких как лошади.Фактически, самые ранние содержащие антитела препараты, используемые против инфекционных заболеваний, были получены от лошадей, овец и кроликов.
Эти антитела могут поступать из объединенных и очищенных продуктов крови иммунных людей или иммунных животных, отличных от человека, таких как лошади.Фактически, самые ранние содержащие антитела препараты, используемые против инфекционных заболеваний, были получены от лошадей, овец и кроликов.
Антитела были впервые использованы для лечения заболеваний в конце 19 -го -го века, когда зарождалась область бактериологии. Первая история успеха связана с дифтерией, опасным заболеванием, которое закупоривает горло и дыхательные пути у тех, кто ею заразился.
В 1890 году Сибасабуро Китасато (1852-1931) и Эмиль фон Беринг (1854-1917) иммунизировали морских свинок против дифтерии термически обработанными продуктами крови животных, выздоровевших от болезни.Препараты содержали антитела к дифтерийному токсину, которые защищали морских свинок, если вскоре после этого они подверглись воздействию летальных доз дифтерийных бактерий и их токсина. Затем ученые показали, что они могут вылечить дифтерию у животного, вводя ему продукты крови иммунизированного животного. Вскоре они перешли к тестированию подхода на людях и смогли показать, что продукты крови иммунизированных животных могут лечить дифтерию у людей. Вещество, содержащее антитела, полученное из крови, было названо дифтерийным антитоксином, и государственные советы по здравоохранению и коммерческие предприятия начали производить и распространять его с 1895 года.Затем Китасато, фон Беринг и другие ученые сосредоточили свое внимание на лечении столбняка, оспы и бубонной чумы препаратами крови, содержащими антитела.
Затем ученые показали, что они могут вылечить дифтерию у животного, вводя ему продукты крови иммунизированного животного. Вскоре они перешли к тестированию подхода на людях и смогли показать, что продукты крови иммунизированных животных могут лечить дифтерию у людей. Вещество, содержащее антитела, полученное из крови, было названо дифтерийным антитоксином, и государственные советы по здравоохранению и коммерческие предприятия начали производить и распространять его с 1895 года.Затем Китасато, фон Беринг и другие ученые сосредоточили свое внимание на лечении столбняка, оспы и бубонной чумы препаратами крови, содержащими антитела.
Использование антител для лечения конкретных заболеваний привело к попыткам разработки иммунизаций против болезней. Джозеф Стоукс-младший, доктор медицины, и Джон Ниф, доктор медицины, провели испытания в Университете Пенсильвании по контракту с ВМС США во время Второй мировой войны, чтобы исследовать использование препаратов антител для предотвращения инфекционного гепатита (то, что мы сейчас называем гепатитом А). Их новаторская работа, наряду с достижениями в разделении компонентов крови, содержащих антитела, привела к многочисленным исследованиям эффективности препаратов антител для иммунизации против кори и инфекционного гепатита.
Их новаторская работа, наряду с достижениями в разделении компонентов крови, содержащих антитела, привела к многочисленным исследованиям эффективности препаратов антител для иммунизации против кори и инфекционного гепатита.
До того, как вакцина против полиомиелита была лицензирована, медицинские работники надеялись на использование гамма-глобулина (продукта крови, содержащего антитела) для предотвращения заболевания. Уильям М. Хэммон, доктор медицинских наук, из Высшей школы общественного здравоохранения Университета Питтсбурга, основываясь на работе Стоукса и Нифе, провел важные испытания для проверки этой идеи в 1951-52 гг.Он показал, что введение гамма-глобулина, содержащего известные антитела к полиовирусу, может предотвратить случаи паралитического полиомиелита. Однако ограниченная доступность гамма-глобулина и обеспечиваемая им краткосрочная защита означали, что это лечение нельзя было использовать в широких масштабах. Лицензирование инактивированной полиомиелитной вакцины Солка в 1955 году сделало ненужным использование гамма-глобулина для иммунизации против полиовируса.
Сегодня можно лечить больных дифтерией или цитомегаловирусом с помощью антител.Или лечение антителами может использоваться в качестве превентивной меры после воздействия патогена, чтобы попытаться остановить развитие болезни (например, при респираторно-синцитиальном вирусе [RSV], кори, столбняке, гепатите A, гепатите B, бешенстве или ветряной оспе). Лечение антителами может не использоваться в обычных случаях этих заболеваний, но оно может быть полезным для лиц с высоким риском, таких как люди с дефицитом иммунной системы.
Преимущества и недостатки пассивной иммунизации Вакцинам обычно требуется время (недели или месяцы) для выработки защитного иммунитета у человека, и может потребоваться введение нескольких доз в течение определенного периода времени для достижения оптимальной защиты.Пассивная иммунизация, однако, имеет преимущество в том, что она быстро действует, вызывая иммунный ответ в течение нескольких часов или дней, быстрее, чем вакцина. Кроме того, пассивная иммунизация может преодолеть ослабленную иммунную систему, что особенно полезно для тех, кто не реагирует на иммунизацию.
Кроме того, пассивная иммунизация может преодолеть ослабленную иммунную систему, что особенно полезно для тех, кто не реагирует на иммунизацию.
имеют определенные недостатки. Во-первых, антитела могут быть сложными и дорогостоящими в производстве. Хотя новые методы могут помочь в производстве антител в лаборатории, в большинстве случаев антитела к инфекционным заболеваниям необходимо получать из крови сотен или тысяч доноров-людей.Либо их необходимо получать из крови иммунных животных (как и антитела, нейтрализующие змеиные яды). В случае антител, полученных от животных, у реципиента могут развиться серьезные аллергические реакции. Еще одним недостатком является то, что многие виды лечения антителами необходимо вводить внутривенно, что является более длительной и потенциально сложной процедурой, чем введение вакцины. Наконец, иммунитет, обеспечиваемый пассивной иммунизацией, недолговечен: он не приводит к образованию долговременных иммунных клеток памяти.
В некоторых случаях пассивный и активный иммунитет могут использоваться вместе. Например, человек, укушенный бешеным животным, может получить антитела против бешенства (пассивная иммунизация для создания немедленного ответа) и вакцину против бешенства (активный иммунитет для получения длительного ответа на этот медленно размножающийся вирус).
Например, человек, укушенный бешеным животным, может получить антитела против бешенства (пассивная иммунизация для создания немедленного ответа) и вакцину против бешенства (активный иммунитет для получения длительного ответа на этот медленно размножающийся вирус).
Моноклональные антитела Все чаще используется технология для получения моноклональных антител (МАт) – «моно» означает, что они представляют собой чистый, единственный тип антител, нацеленных на один участок патогена, и «клональные», потому что они продуцируются из одной родительской клетки.Эти антитела имеют широкое потенциальное применение при инфекционных заболеваниях и других типах заболеваний.
Моноклональные антитела были впервые созданы исследователями Цезарем Мильштейном, доктором философии (1927–2002), и Джорджем Колером, доктором философии (1946–1995), которые объединили короткоживущие клетки селезенки мыши, продуцирующие антитела (которые подверглись воздействию определенного антигена). с долгоживущими опухолевыми клетками мыши. Объединенные клетки продуцировали антитела к целевому антигену. Мильштейн и Келер получили Нобелевскую премию по физиологии и медицине за свое открытие в 1984 году.
с долгоживущими опухолевыми клетками мыши. Объединенные клетки продуцировали антитела к целевому антигену. Мильштейн и Келер получили Нобелевскую премию по физиологии и медицине за свое открытие в 1984 году.
На сегодняшний день для профилактики инфекционного заболевания коммерчески доступен только один метод лечения MAb. Это препарат моноклональных антител для профилактики тяжелых заболеваний, вызванных РСВ, у детей из группы высокого риска. Врачи также все чаще используют MAb для борьбы с неинфекционными заболеваниями, такими как некоторые виды рака, рассеянный склероз, ревматоидный артрит, болезнь Крона и сердечно-сосудистые заболевания.
Ученые исследуют другие новые технологии для производства антител в лаборатории, такие как рекомбинантные системы с использованием дрожжевых клеток или вирусов и системы, объединяющие клетки человека и клетки мыши, или ДНК человека и ДНК мыши.
Угрозы биотерроризма В случае преднамеренного выброса инфекционного биологического агента эксперты по биобезопасности предположили, что пассивная иммунизация может сыграть роль в реагировании на чрезвычайные ситуации. Преимущество использования антител, а не вакцин для реагирования на биотеррор, заключается в том, что антитела обеспечивают немедленную защиту, тогда как защитный ответ, вызванный вакциной, не является немедленным и в некоторых случаях может зависеть от бустерной дозы, введенной позднее.
Преимущество использования антител, а не вакцин для реагирования на биотеррор, заключается в том, что антитела обеспечивают немедленную защиту, тогда как защитный ответ, вызванный вакциной, не является немедленным и в некоторых случаях может зависеть от бустерной дозы, введенной позднее.
Кандидатами на это потенциальное применение пассивной иммунизации являются ботулинический токсин, туляремия, сибирская язва и чума.Для большинства этих целей проводились исследования только на животных, поэтому использование пассивной иммунизации в случае потенциальных биотеррористических событий все еще находится на экспериментальной стадии.
Сводка Антитела были одним из первых средств, применявшихся против конкретных инфекционных заболеваний. По мере широкого применения антибиотиков и разработки вакцин использование пассивной иммунизации стало менее распространенным. Однако даже сегодня антитела играют роль в борьбе с инфекционными заболеваниями, когда врачи используют антитела для достижения пассивного иммунитета и лечения определенных заболеваний у пациентов. Ученые изучают новые способы пассивной иммунизации и лечения антителами, а также новые и более эффективные методы создания антител.
Ученые изучают новые способы пассивной иммунизации и лечения антителами, а также новые и более эффективные методы создания антител.
Casadevall, A. Пассивное введение антител (немедленный иммунитет) как специфическая защита от биологического оружия. Emerg Infect Dis [сериал онлайн] 8 августа 2002 г. Дата обращения 10.01.2018.
Центры по контролю и профилактике заболеваний. Типы иммунитета. Дата обращения 10.01.2018.
Келлер, М.А., Штим, Э.Р. Пассивный иммунитет в профилактике и лечении инфекционных заболеваний. Обзоры клинической микробиологии. , октябрь 2000 г., стр. 602-614, том. 13, вып. 4.
Feign, R.D., Cherry, J.D., Demmler, G.J., Kaplan, S.L. Учебник детских инфекционных болезней. 5 -е изд. , том. 2. Филадельфия: Сондерс, 2004.
. Kaempffert, W. Причина армейской желтухи теперь обнаружена и указаны средства контроля. New York Times, , 21 января 1945 г.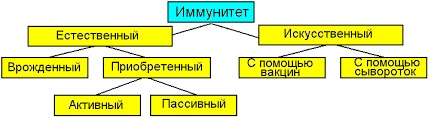 Дата обращения 10.01.2018.
Дата обращения 10.01.2018.
Kaempffert, W. Профилактика кори: гамма-глобулин, выделенный из крови, уничтожает микроб. New York Times , 14 мая 1944 г. По состоянию на 10 января 2018 г.
Ринальдо-младший, Ч.Р. Пассивная иммунизация против полиомиелита. Полевые испытания гамма-глобулина Hammon, 1951-1953 гг. Am J Pub Health. 2005 Май; 95(5):790-799. Дата обращения 10.01.2018.
Информационная страница Synagis (Palivizumab). Дата обращения 10.01.2018.
Последнее обновление 10 января 2018 г.
Анализ индивидуальных стратегий искусственного и естественного иммунитета при несовершенстве и долговечности защиты
.2021 21 января; 509:110531. doi: 10.1016/j.jtbi.2020.110531. Epub 2020 28 октября.Принадлежности Расширять
Принадлежности
- 1 Междисциплинарная аспирантура инженерных наук Университета Кюсю, Касуга-коен, Касуга-ши, Фукуока 816-8580, Япония; Кафедра математики Бангладешского инженерно-технологического университета, Дакка, Бангладеш.
 Electronic address: [email protected].
Electronic address: [email protected]. - 2 Faculty of Engineering Sciences, Kyushu University, Kasuga-koen, Kasuga-shi, Fukuoka 816-8580, Japan; Interdisciplinary Graduate School of Engineering Sciences, Kyushu University, Kasuga-koen, Kasuga-shi, Fukuoka 816-8580, Japan.
Item in Clipboard
K M Ariful Kabir et al.Дж Теор Биол. .
Показать детали Показать вариантыПоказать варианты
Формат АннотацияPubMedPMID
. 2021 21 января; 509:110531.
doi: 10.1016/j.jtbi.2020.110531.
Epub 2020 28 октября.
2021 21 января; 509:110531.
doi: 10.1016/j.jtbi.2020.110531.
Epub 2020 28 октября.Принадлежности
- 1 Междисциплинарная аспирантура инженерных наук Университета Кюсю, Касуга-коен, Касуга-ши, Фукуока 816-8580, Япония; Кафедра математики Бангладешского инженерно-технологического университета, Дакка, Бангладеш.Электронный адрес: [email protected].
- 2 Факультет инженерных наук, Университет Кюсю, Касуга-коен, Касуга-ши, Фукуока 816-8580, Япония; Междисциплинарная аспирантура инженерных наук Университета Кюсю, Касуга-коэн, Касуга-ши, Фукуока 816-8580, Япония.

Элемент в буфере обмена
Полнотекстовые ссылки Параметры отображения цитированияПоказать варианты
Формат АннотацияPubMedPMID
Абстрактный
В качестве защиты от инфекционных заболеваний иммунитет обеспечивается одним из двух основных защитных механизмов, а именно (i) устойчивостью, вызванной предшествующей инфекцией (известной как естественный иммунитет), или (ii) вакцинацией (известной как искусственный иммунитет).Для анализа создана модифицированная модель эпидемии СВИРС, которая интегрирует эффекты долговечности защиты и несовершенства в рамках процесса принятия решений человеком как игры вакцинации. Предполагается, что иммунизированные люди вновь становятся восприимчивыми по истечении срока их иммунитета, что зависит от продолжительности иммунитета. Текущая теория большинства игр с добровольной вакцинацией предполагает, что сезонные болезни, такие как грипп, контролируются временной вакциной, иммунитет от которой сохраняется только в течение одного сезона.Кроме того, устанавливается новая перспектива, включающая иммунную систему человека в сочетании с личным интересом принять вакцину и естественный иммунитет, полученный от инфекции, путем сочетания модели распространения болезни с эволюционным игровым подходом в течение длительного периода. Численное моделирование показывает, что более длительное затухание помогает значительно контролировать распространение болезни. Также открыт весь механизм активных и пассивных иммунитетов в том смысле, как они сосуществуют с естественным и искусственным иммунитетом.Таким образом, перспектива поиска оптимальной стратегии ликвидации болезни может помочь в разработке эффективных кампаний и политики вакцинации.
Текущая теория большинства игр с добровольной вакцинацией предполагает, что сезонные болезни, такие как грипп, контролируются временной вакциной, иммунитет от которой сохраняется только в течение одного сезона.Кроме того, устанавливается новая перспектива, включающая иммунную систему человека в сочетании с личным интересом принять вакцину и естественный иммунитет, полученный от инфекции, путем сочетания модели распространения болезни с эволюционным игровым подходом в течение длительного периода. Численное моделирование показывает, что более длительное затухание помогает значительно контролировать распространение болезни. Также открыт весь механизм активных и пассивных иммунитетов в том смысле, как они сосуществуют с естественным и искусственным иммунитетом.Таким образом, перспектива поиска оптимальной стратегии ликвидации болезни может помочь в разработке эффективных кампаний и политики вакцинации.
Ключевые слова: искусственный иммунитет; естественный иммунитет; игра вакцинация; Ослабевающий иммунитет.
Copyright © 2020 ООО «Эльзевир».Все права защищены.
Заявление о конфликте интересов
Декларация о конкурирующих интересах Авторы заявляют, что у них нет известных конкурирующих финансовых интересов или личных отношений, которые могли бы повлиять на работу, представленную в этой статье.
Похожие статьи
- Оптимальные индивидуальные стратегии вакцин против гриппа с несовершенной эффективностью и долговечностью защиты.
Сальварани Ф., Туринич Г. Сальварани Ф. и др. Math Biosci Eng. 2018 1 июня; 15 (3): 629-652. doi: 10.3934/mbe.2018028. Math Biosci Eng. 2018. PMID: 30380323
- [Технические рекомендации по сезонной вакцинации против гриппа в Китае (2018-2019 гг.
 )].
)].Фэн Л.З., Пэн З.Б., Ван Д.Ю., Ян П., Ян Дж., Чжан Ю.Ю., Чен Дж., Цзян С.К., Сюй Л.Л., Кан М., Чен Т., Чжэн Ю.М., Чжэн Д.Д., Цинь И., Чжао М.Дж., Тан Ю.Ю., Ли З.Дж. , Фэн ZJ.Фэн Л.З. и др. Чжунхуа Юй Фан И Сюэ За Чжи. 2018 6 ноября; 52 (11): 1101-1114. doi: 10.3760/cma.j.issn.0253-9624.2018.11.003. Чжунхуа Юй Фан И Сюэ За Чжи. 2018. PMID: 30419692 Китайский язык.
- Обсервационное исследование по изучению вертикально приобретенного пассивного иммунитета у младенцев от матерей, вакцинированных против h2N1v во время беременности.
Пулстон Р.Л., Багг Г., Хошлер К., Конье Дж., Торнтон Дж., Стефенсон И., Майлз П., Энстон Дж., Августин Г., Дэвис И., Замбон М., Николсон К.Г., Нгуен-Ван-Там Д.С.Пулстон Р.Л. и соавт. Оценка медицинских технологий. 2010 Декабрь; 14(55):1-82. doi: 10.3310/hta14550-01. Оценка медицинских технологий.
 2010.
PMID: 21208547
2010.
PMID: 21208547 - [Технические рекомендации по вакцинации против сезонного гриппа в Китае (2020-2021 гг.)].
Национальный консультативный комитет по иммунизации (NIAC) Техническая рабочая группа (TWG) TWG по вакцинации против гриппа. Национальный консультативный комитет по иммунизации (NIAC) Техническая рабочая группа (TWG) TWG по вакцинации против гриппа.Чжунхуа Лю Син Бин Сюэ За Чжи. 2020 10 октября; 41 (10): 1555-1576. doi: 10.3760/cma.j.cn112338-20200904-01126. Чжунхуа Лю Син Бин Сюэ За Чжи. 2020. PMID: 33297613 Китайский язык.
- Текущие вызовы: от пути «первородного антигенного греха» к разработке универсальных противогриппозных вакцин.
Бисвас А., Чакрабарти А.К., Датта С. Бисвас А. и др. Int Rev Immunol.
 2020;39(1):21-36. дои: 10.1080/08830185.2019.1685990. Epub 2019 9 ноября.
Int Rev Immunol. 2020.
PMID: 31707873
Обзор.
2020;39(1):21-36. дои: 10.1080/08830185.2019.1685990. Epub 2019 9 ноября.
Int Rev Immunol. 2020.
PMID: 31707873
Обзор.
Цитируется
1 артикул- Просоциальное поведение ношения маски во время эпидемии: эволюционное объяснение.
Кабир КМА, Риса Т., Танимото Дж.Кабир КМА и др. Научный представитель 2021 г. 16 июня; 11 (1): 12621. doi: 10.1038/s41598-021-92094-2. Научный представитель 2021. PMID: 34135413 Бесплатная статья ЧВК.
Типы публикаций
- Поддержка исследований, за пределами США Правительство
Условия MeSH
- Грипп человека* / профилактика и контроль
LinkOut — дополнительные ресурсы
Полнотекстовые источники
Прочие литературные источники
Медицинские
Исследовательские материалы
Укажите
КопироватьФормат: ААД АПА ГНД НЛМ
Активный и пассивный иммунитет, типы вакцин, вспомогательные вещества и лицензирование | Медицина труда
Аннотация
Abstract Иммунитет – это состояние защиты от инфекционного заболевания, обеспечиваемое либо иммунным ответом, вызванным иммунизацией или предшествующей инфекцией, либо другими неиммунологическими факторами. В этой статье рассматриваются активный и пассивный иммунитет и различия между ними: также описываются четыре различных коммерчески доступных типа вакцин (живая аттенуированная, убитая/инактивированная, субъединичная и токсоидная); также рассматривается, как эти разные вакцины вызывают адаптивный иммунный ответ.
В этой статье рассматриваются активный и пассивный иммунитет и различия между ними: также описываются четыре различных коммерчески доступных типа вакцин (живая аттенуированная, убитая/инактивированная, субъединичная и токсоидная); также рассматривается, как эти разные вакцины вызывают адаптивный иммунный ответ.
Введение
В первой статье этой серии были рассмотрены те механизмы хозяина, которые защищают от микробной инвазии. Как ограниченная эффективность против определенных патогенов, так и процессы уклонения от патогенов означают, что некоторые инфекционные заболевания все еще встречаются часто; некоторые из них связаны с профессиональной деятельностью, поскольку риск для медицинских работников особенно хорошо задокументирован [1,2].Поскольку определенные профессиональные инфекции можно предотвратить с помощью иммунизации, в этой статье будет рассмотрено, как различные типы вакцин модулируют адаптивные реакции для обеспечения дополнительной защиты. Однако сначала будут рассмотрены термины активный и пассивный иммунитет.
Однако сначала будут рассмотрены термины активный и пассивный иммунитет.
Активный и пассивный иммунитет
Под активным иммунитетом понимается процесс воздействия на организм антигена для выработки адаптивного иммунного ответа: для развития ответа требуются дни/недели, но он может сохраняться длительное время — даже на протяжении всей жизни.Активный иммунитет обычно классифицируют как естественный или приобретенный. Дикое заражение, например, вирусом гепатита А (HAV) и последующее выздоровление вызывает естественный активный иммунный ответ, обычно приводящий к пожизненной защите. Аналогичным образом введение двух доз вакцины против гепатита А вызывает приобретенный активный иммунный ответ, приводящий к длительной (возможно, пожизненной) защите. Вакцина против гепатита А была лицензирована только в конце 1980-х годов, поэтому последующие исследования продолжительности защиты ограничены <25 годами — отсюда предостережение относительно продолжительности защиты.
Пассивный иммунитет относится к процессу выработки антител IgG для защиты от инфекции; он дает немедленную, но недолгую защиту — от нескольких недель до 3 или 4 месяцев максимум. Пассивный иммунитет обычно классифицируют как естественный или приобретенный. Перенос материнских противостолбнячных антител (в основном IgG) через плаценту обеспечивает естественный пассивный иммунитет новорожденного в течение нескольких недель/месяцев, пока такие антитела не разрушатся и не исчезнут. Напротив, приобретенный пассивный иммунитет относится к процессу получения сыворотки от иммунных лиц, ее объединения, концентрации фракции иммуноглобулина и последующего введения ее для защиты восприимчивого человека.
Ниже перечислены четыре наиболее часто используемых препарата иммуноглобулина.
(i) Иммуноглобулин против гепатита В человека Ph.Eur.* Лаборатория биологических продуктов: Иммуноглобулин против гепатита В человека представлен в виде двух флаконов по 200 и 500 МЕ. Каждый миллилитр содержит 10–100 мг/мл человеческого белка, из которых не менее 95% составляют гаммаглобулины (IgG).
 Этот продукт готовят из плазмы от проверенных доноров, отобранных в США. В одном миллилитре содержится не менее 100 МЕ антител к гепатиту В.Его профессиональное использование предназначено для немедленной защиты неиммунных медицинских работников, подвергшихся воздействию вирусов гепатита В (вместе с соответствующей программой вакцинации).
Этот продукт готовят из плазмы от проверенных доноров, отобранных в США. В одном миллилитре содержится не менее 100 МЕ антител к гепатиту В.Его профессиональное использование предназначено для немедленной защиты неиммунных медицинских работников, подвергшихся воздействию вирусов гепатита В (вместе с соответствующей программой вакцинации).(ii) Человеческий антирабический иммуноглобулин Ph.Eur.* Bio Products Laboratory: Человеческий антирабический иммуноглобулин представлен в виде флакона размером 500 МЕ. Каждый миллилитр содержит 40–180 мг/мл человеческого белка, из которых не менее 95% составляют гаммаглобулины (IgG). Этот продукт готовят из плазмы от проверенных доноров, отобранных в США.Один миллилитр содержит не <150 МЕ антител против бешенства. Он дается как часть постконтактной профилактики неиммунным лицам, подвергшимся воздействию бешенства.
(iii) Иммуноглобулин против столбняка человека Ph.Eur.* Лаборатория биологических продуктов: Иммуноглобулин против столбняка человека представлен в виде флакона размером 250 МЕ.
 Каждый миллилитр содержит 40–180 мг/мл человеческого белка, из которых не менее 95% составляют гаммаглобулины (IgG). Этот продукт готовят из плазмы от проверенных доноров, отобранных в США.Один миллилитр содержит не <100 МЕ противостолбнячных антител. Маловероятно, что этот препарат будет использоваться для медицинских работников; его вводят как при лечении ран, склонных к столбняку, при сильном загрязнении почвы/навоза, так и при лечении всех ран, если считается, что человек не имеет иммунитета.
Каждый миллилитр содержит 40–180 мг/мл человеческого белка, из которых не менее 95% составляют гаммаглобулины (IgG). Этот продукт готовят из плазмы от проверенных доноров, отобранных в США.Один миллилитр содержит не <100 МЕ противостолбнячных антител. Маловероятно, что этот препарат будет использоваться для медицинских работников; его вводят как при лечении ран, склонных к столбняку, при сильном загрязнении почвы/навоза, так и при лечении всех ран, если считается, что человек не имеет иммунитета.(iv) Человеческий иммуноглобулин Varicella-Zoster Ph.Eur.* Bio Products Laboratory: Каждый флакон содержит 250 мг белка (40–180 мг/мл), из которых не менее 95% составляют гаммаглобулины (IgG).Этот продукт готовят из плазмы от проверенных доноров, отобранных в США. Один миллилитр содержит не менее 100 МЕ антител к ветряной оспе. Он дается как часть постконтактной профилактики определенным неиммунным лицам, подвергшимся воздействию ветряной оспы.
Более подробная информация обо всех этих продуктах доступна на сайте http://www. emc.medicines.org.uk.
emc.medicines.org.uk.
Типы вакцин
Можно ожидать, что большинство рабочих, родившихся в Великобритании, были привиты против дифтерии, столбняка, коклюша и полиомиелита.В зависимости от их возраста и пола они также могли болеть корью, эпидемическим паротитом, краснухой, Haemophilus influenzae типа b (Hib) и Neisseria meningitidis типа C (Men C).
Эти различные имеющиеся в продаже вакцины можно разделить на один из четырех типов в зависимости от природы вакцинных антигенов: живые аттенуированные, убитые инактивированные, токсоидные и субъединичные. Субъединичные вакцины можно далее подразделить на вакцины, в которых антиген получают с использованием технологии рекомбинантной ДНК, и вакцины, основанные на нормальных процессах бактериологического роста.
Кроме того, все вакцины содержат другие вещества (называемые вспомогательными веществами), которые присутствуют, поскольку они улучшают иммунный ответ (адъювант), необходимы для обеспечения стабильности продукта (стабилизаторы и консерванты), являются средством доставки вакцины (носитель) или являются остатком производственного процесса (например, антибиотики или компоненты клеточной культуры).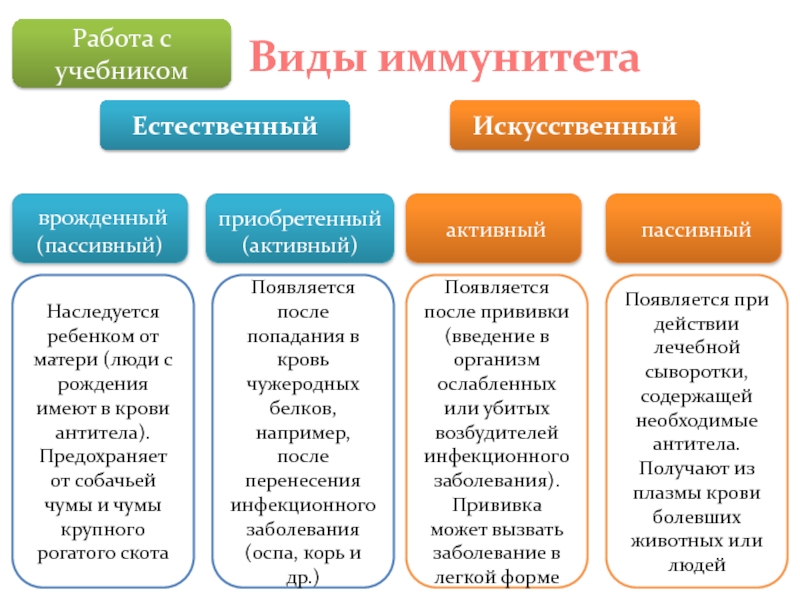
Токсоидные вакцины
Некоторые патогены вызывают заболевание, выделяя экзотоксин: к ним относятся столбняк, дифтерия, ботулизм и холера, кроме того, некоторые инфекции, например, коклюш, по-видимому, частично опосредованы токсином [3,4].
При столбняке основной токсин (называемый тетаноспазмином) связывается со специфическими мембранными рецепторами, расположенными только на пресинаптических двигательных нервных клетках. Последующая интернализация и миграция этого токсина в центральную нервную систему блокирует метаболизм глицина, необходимого для нормального функционирования нейронов гамма-аминомасляной кислоты (ГАМК). Поскольку ГАМК-нейроны являются тормозными для двигательных нейронов, их нефункционирование приводит к избыточной активности двигательных нейронов, при этом мышцы, снабжаемые этими нервами, сокращаются чаще, чем обычно, вызывая мышечные спазмы, которые являются характерным признаком столбняка.
Вакцина против столбняка производится путем выращивания высокотоксигенного штамма Clostridium tetani в полусинтетической среде: рост бактерий и последующий лизис высвобождают токсин в супернатант, а обработка формальдегидом превращает токсин в анатоксин путем изменения определенных аминокислот и вызывая незначительные молекулярные конформационные изменения. Затем ультрафильтрация удаляет ненужные белки, оставшиеся в результате производственного процесса, для получения конечного продукта.Токсоид физико-химически подобен нативному токсину, что индуцирует перекрестно реагирующие антитела, но изменения, вызванные обработкой формальдегидом, делают его нетоксигенным [5–7].
Затем ультрафильтрация удаляет ненужные белки, оставшиеся в результате производственного процесса, для получения конечного продукта.Токсоид физико-химически подобен нативному токсину, что индуцирует перекрестно реагирующие антитела, но изменения, вызванные обработкой формальдегидом, делают его нетоксигенным [5–7].
После глубокого подкожного/внутримышечного (п/к) введения противостолбнячной вакцины молекулы анатоксина поглощаются в месте вакцинации незрелыми дендритными клетками: внутри этой клетки они перерабатываются через эндосомальный путь (с участием фаголизосом), где они связаны с молекулами главного комплекса гистосовместимости типа II (MHC II); затем комплекс MHC II:анатоксин мигрирует на поверхность клетки.Пока этот процесс происходит внутри клетки, уже активированная зрелая дендритная клетка мигрирует по лимфатическим каналам в дренирующий лимфатический узел, где они сталкиваются с наивными Т-хелперами типа 2 (T H 2), каждая из которых имеет свой собственный уникальный Т-клеточный рецептор. (ТКР). Идентификация и последующее связывание MHC II:toxoid со специфическим рецептором T H 2 затем активирует наивные Т-клетки, вызывая их пролиферацию.
(ТКР). Идентификация и последующее связывание MHC II:toxoid со специфическим рецептором T H 2 затем активирует наивные Т-клетки, вызывая их пролиферацию.
Одновременно молекулы анатоксина, не поглощенные дендритными клетками, проходят по лимфатическим каналам к тем же дренирующим лимфатическим узлам, где они вступают в контакт с В-клетками, каждая из которых имеет свой уникальный В-клеточный рецептор (BCR).Связывание с В-клеткой через специфический рецептор иммуноглобулина, который распознает столбнячный анатоксин, приводит к интернализации анатоксина, процессингу через эндосомальный путь и представлению на клеточной поверхности в виде комплекса MHC II:анатоксин, как это происходит в дендритной клетке.
Эти два процесса происходят в одной и той же части лимфатического узла, в результате чего В-клетка с комплексом MHC II:анатоксин на своей поверхности теперь вступает в контакт с активированным T H 2, чьи рецепторы специфичны для этого комплекса . Процесс, называемый сцепленным распознаванием, приводит к тому, что T H 2 активирует В-клетку, чтобы она стала плазматической клеткой с первоначальной продукцией IgM, а затем происходит переключение изотипа на IgG; кроме того, часть В-клеток становится клетками памяти.
Процесс, называемый сцепленным распознаванием, приводит к тому, что T H 2 активирует В-клетку, чтобы она стала плазматической клеткой с первоначальной продукцией IgM, а затем происходит переключение изотипа на IgG; кроме того, часть В-клеток становится клетками памяти.
Описанный выше механизм описывает адаптивный иммунный ответ на белковый антиген-подобный столбнячный анатоксин; такие антигены называются Т-зависимыми вакцинами, поскольку участие Т-хелперных клеток необходимо для генерируемого иммунного ответа.Полисахаридные антигены, напротив, вызывают несколько иной ответ, как будет описано в разделе, посвященном субъединичным вакцинам.
Таким образом, обоснование вакцинации против столбняка основано на выработке антител против анатоксина, обладающих повышенной способностью связывать токсин по сравнению с участками связывания рецепторов токсина на нервных клетках; в случае воздействия C. tetani этот большой комплекс токсин:антитело не может связываться с рецептором, таким образом нейтрализуя токсин и предотвращая развитие заболевания.
Дифтерийный и коклюшный анатоксины (в бесклеточных коклюшных вакцинах) представляют собой две коммерчески доступные анатоксинные вакцины, против которых антитела вырабатываются точно так же, как описано выше. Вакцины против столбняка и дифтерии (вместе с инактивированной вакциной против полиомиелита) должны предлагаться на производстве работникам, не прошедшим пятидозовую программу. Подходящим препаратом в Великобритании будет Revaxis, который содержит не <2 МЕ очищенного дифтерийного анатоксина, не <20 МЕ очищенного столбнячного анатоксина, 40 единиц D-антигена инактивированного полиомиелита типа 1, 8 единиц типа 2 и 32 типа 3; анатоксины адсорбируются на гидроксиде алюминия в качестве адъюванта (см. ниже).
Токсоидные вакцины, как правило, не обладают высокой иммуногенностью, если только не используются большие количества или несколько доз: одна проблема с использованием больших доз заключается в том, что может быть индуцирована толерантность к антигену. Таким образом, чтобы гарантировать, что адаптивный иммунный ответ достаточно эффективен для обеспечения длительного иммунитета, в вакцину включают адъювант. Для вакцин против дифтерии, столбняка и бесклеточного коклюша используется соль алюминия (либо гидроксид, либо фосфат); это работает путем образования депо в месте инъекции, что приводит к устойчивому высвобождению антигена в течение более длительного периода времени, активируя клетки, участвующие в адаптивном иммунном ответе.Алюминиевые адъюванты также легко поглощаются незрелыми дендритными клетками и облегчают процессинг антигена в селезенке/лимфатических узлах, где происходят необходимые межклеточные взаимодействия, приводящие к развитию высокоаффинных клонов В-клеток, продуцирующих антитела [9–11]. .
Для вакцин против дифтерии, столбняка и бесклеточного коклюша используется соль алюминия (либо гидроксид, либо фосфат); это работает путем образования депо в месте инъекции, что приводит к устойчивому высвобождению антигена в течение более длительного периода времени, активируя клетки, участвующие в адаптивном иммунном ответе.Алюминиевые адъюванты также легко поглощаются незрелыми дендритными клетками и облегчают процессинг антигена в селезенке/лимфатических узлах, где происходят необходимые межклеточные взаимодействия, приводящие к развитию высокоаффинных клонов В-клеток, продуцирующих антитела [9–11]. .
Токсоидные вакцины обладают тремя основными преимуществами. Во-первых, они безопасны, потому что не могут вызвать болезнь, которую предотвращают, и нет возможности возврата к вирулентности. Во-вторых, поскольку вакцинные антигены не размножаются активно, они не могут распространяться среди неиммунизированных людей.В-третьих, они обычно стабильны и долговечны, поскольку менее чувствительны к изменениям температуры, влажности и света, которые могут возникнуть, когда вакцины используются в обществе.
Токсоидные вакцины имеют два недостатка. Во-первых, им обычно требуется адъювант и требуется несколько доз по причинам, рассмотренным выше. Во-вторых, более распространены местные реакции в месте введения вакцины — это может быть связано с адъювантом или реакцией типа III (Артуса) — последние обычно начинаются в виде покраснения и уплотнения в месте инъекции через несколько часов после вакцинации и обычно проходят в течение 48 часов. –72 ч.Реакция возникает в результате того, что избыток антител в этом месте образует комплекс с молекулами анатоксина и активирует комплемент по классическому пути, вызывая острую местную воспалительную реакцию.
Убитые/инактивированные вакцины
Термин «убитый» обычно относится к бактериальным вакцинам, тогда как «инактивированный» относится к вирусным вакцинам [3,4]. Брюшной тиф был одной из первых произведенных убитых вакцин и использовался в британских войсках в конце 19 века. Полиомиелит и гепатит А в настоящее время являются основными инактивированными вакцинами, используемыми в Великобритании; во многих странах цельноклеточная коклюшная вакцина по-прежнему является наиболее широко используемой убитой вакциной.
Адаптивный иммунный ответ на убитую/инактивированную вакцину очень похож на анатоксинную вакцину, за исключением того, что генерируемый ответ антител направлен против гораздо более широкого спектра антигенов. Таким образом, после инъекции весь организм фагоцитируется незрелыми дендритными клетками; переваривание внутри фаголизосомы дает ряд различных антигенных фрагментов, которые представлены на клеточной поверхности в виде отдельных комплексов MHC II:антигенный фрагмент. В дренирующем лимфатическом узле ряд T H 2, каждый из которых имеет TCR для отдельного антигенного фрагмента, будет активирован за счет презентации активированной зрелой дендритной клеткой.В-клетки, каждая из которых имеет BCR для отдельного антигенного фрагмента, будут связывать антигены, которые дрейфуют по лимфатическим каналам: отдельные антигены будут интернализованы и представлены в виде MHC II: антигенного фрагмента; это приведет к связанному распознаванию с соответствующим T H 2. Высвобождение T H 2 IL2, IL4, IL5 и IL6 индуцирует активацию, дифференцировку и пролиферацию B-клеток с последующим переключением изотипа (IgM на IgG) и образование ячеек памяти.
Высвобождение T H 2 IL2, IL4, IL5 и IL6 индуцирует активацию, дифференцировку и пролиферацию B-клеток с последующим переключением изотипа (IgM на IgG) и образование ячеек памяти.
Этот процесс занимает минимум 10–14 дней, но при последующем воздействии на организм индуцируется вторичный ответ посредством активации различных В-клеток памяти, что приводит к высоким уровням различных молекул IgG в течение 24–48 часов.
Гепатит А является примером инактивированной вакцины, которую могут использовать специалисты по гигиене труда. Это штамм HAV, инактивированный формалином, адаптированный к клеточной культуре; вакцинация вырабатывает нейтрализующие антитела, а защитная эффективность превышает 90%. Следует рассмотреть вопрос о вакцинации работников лабораторий, работающих с ВГА, и санитарных работников, контактирующих со сточными водами. Кроме того, вакцинация может быть предложена персоналу, работающему с детьми, которые не приучены к туалету, или проживающим в жилых помещениях с низкими гигиеническими стандартами. Первичная иммунизация ревакцинацией в период от 6 до 12 месяцев после первой должна обеспечить защиту минимум на 25 лет [3].
Первичная иммунизация ревакцинацией в период от 6 до 12 месяцев после первой должна обеспечить защиту минимум на 25 лет [3].
Убитые/инактивированные вакцины обладают теми же преимуществами, что и анатоксины, за исключением того, что в них присутствуют все антигены, связанные с инфекцией, и против каждого из них вырабатываются антитела.
Убитые/инактивированные вакцины имеют ряд недостатков. Обычно требуется несколько доз, потому что микробы не могут размножаться в организме хозяина, и поэтому одна доза не дает сильного сигнала адаптивной иммунной системе; подходы к преодолению этого включают использование нескольких доз и введение вакцины с адъювантом [8].Местные реакции в месте введения вакцины встречаются чаще — это часто связано с адъювантом. Использование убитых микробов для вакцин неэффективно, потому что некоторые антитела будут вырабатываться против частей патогена, которые не играют никакой роли в возникновении заболевания. Некоторые из антигенов, содержащихся в вакцине, особенно белки на поверхности, могут на самом деле подавлять адаптационный ответ организма — предположительно, их присутствие — это эволюционное развитие, которое помогает патогену преодолевать защитные силы организма. И, наконец, убитые/инактивированные вакцины не дают цитотоксических Т-клеток, которые могут иметь важное значение для остановки инфекций внутриклеточными патогенами, особенно вирусами.
И, наконец, убитые/инактивированные вакцины не дают цитотоксических Т-клеток, которые могут иметь важное значение для остановки инфекций внутриклеточными патогенами, особенно вирусами.
Субъединичные вакцины
Субъединичные вакцины являются развитием подхода с использованием убитых вакцин: однако вместо выработки антител против всех антигенов патогена используется определенный антиген (или антигены), так что, когда антитело, продуцируемое В-клеткой, связывается с ним, инфекция предотвращается; поэтому ключом к созданию эффективной субъединичной вакцины является идентификация этого конкретного антигена или комбинации антигенов [3,4].Гепатит В и Haemophilus influenzae b (Hib) являются примерами субъединичных вакцин, в которых используется только один антиген; грипп является примером субъединичной вакцины с двумя антигенами (гемагглютинин и нейраминидаза).
Адаптивный иммунный ответ на субъединичную вакцину варьируется в зависимости от того, является ли вакцинный антиген белком или полисахаридом.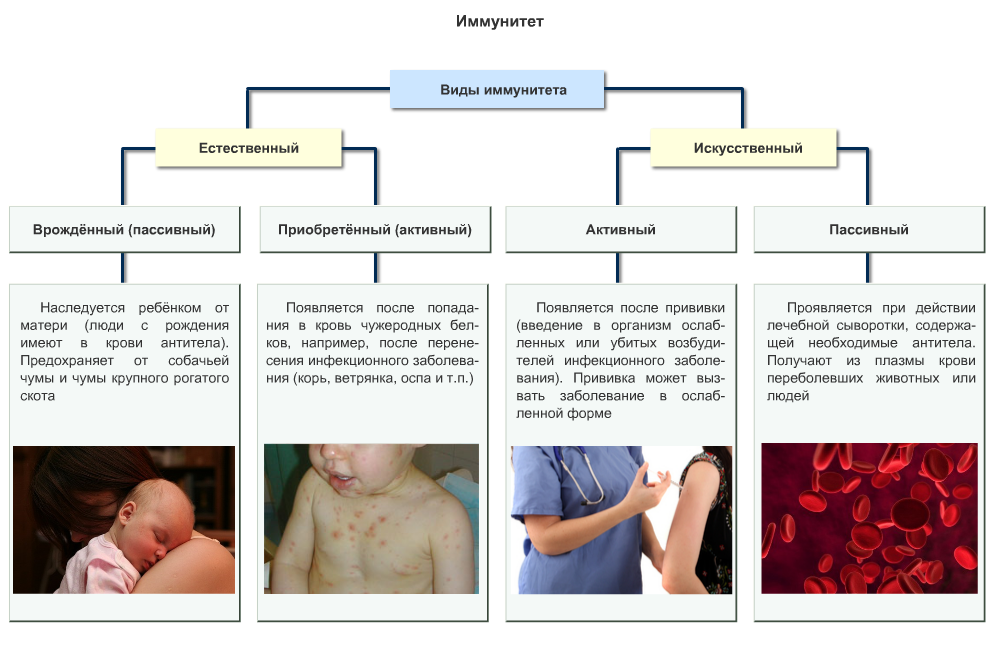 ), тогда как полисахариды вызывают Т-независимый ответ.
), тогда как полисахариды вызывают Т-независимый ответ.
Примером Т-независимой субъединичной вакцины, которую можно вводить в профессиональных условиях, является Пневмовакс, состоящий из капсульного полисахарида 23 распространенных пневмококковых серотипов, который использует капсулярный полисахарид в качестве вакцинного антигена. Вакцину вводят глубоко подкожно или внутримышечно. В месте инъекции некоторые молекулы полисахаридов фагоцитируются незрелыми дендритными клетками (и макрофагами), которые впоследствии мигрируют в местные лимфатические узлы, где встречаются с наивными T H 2.Однако TCR распознает только белковые молекулы, поэтому, хотя он представлен зрелой дендритной клеткой и представлен молекулами MHC II, T H 2 не активируется.
Одновременно нефагоцитированные молекулы полисахаридов проходят по лимфатическим каналам к тем же дренирующим лимфатическим узлам, где они сталкиваются с В-клетками, каждая из которых имеет свой уникальный BCR.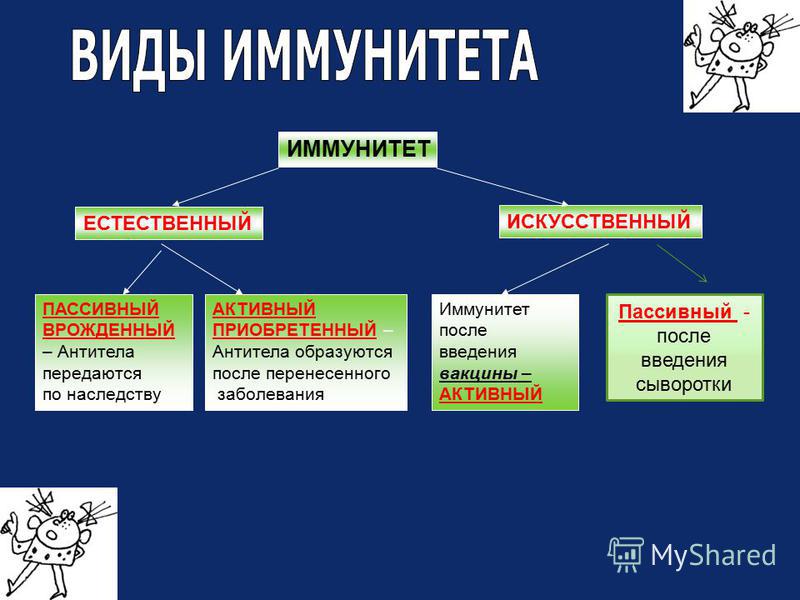 Поскольку вакцинный антиген состоит из линейных повторов одного и того же капсулярного полисахарида высокой молекулярной массы, он с высокой авидностью связывается с несколькими рецепторами на В-клетке с соответствующей специфичностью.Такое мультивалентное связывание способно активировать В-клетки без необходимости участия T H 2, что приводит к продукции IgM. Поскольку, однако, T H 2 не участвует, происходит лишь ограниченное переключение изотипа, так что продуцируются лишь небольшие количества IgG и формируется небольшое количество В-клеток памяти. У адекватно иммунизированного человека, когда Streptococcus pneumoniae пересекает слизистые барьеры, специфические антитела IgM в сыворотке связываются с капсулярным полисахаридом патогена, способствуя лизису, опосредованному комплементом.IgM очень эффективно активирует комплемент; он значительно менее способен действовать как нейтрализующее или опсонизирующее антитело.
Поскольку вакцинный антиген состоит из линейных повторов одного и того же капсулярного полисахарида высокой молекулярной массы, он с высокой авидностью связывается с несколькими рецепторами на В-клетке с соответствующей специфичностью.Такое мультивалентное связывание способно активировать В-клетки без необходимости участия T H 2, что приводит к продукции IgM. Поскольку, однако, T H 2 не участвует, происходит лишь ограниченное переключение изотипа, так что продуцируются лишь небольшие количества IgG и формируется небольшое количество В-клеток памяти. У адекватно иммунизированного человека, когда Streptococcus pneumoniae пересекает слизистые барьеры, специфические антитела IgM в сыворотке связываются с капсулярным полисахаридом патогена, способствуя лизису, опосредованному комплементом.IgM очень эффективно активирует комплемент; он значительно менее способен действовать как нейтрализующее или опсонизирующее антитело.
Пневмовакс следует предлагать работникам с хроническими заболеваниями органов дыхания, сердца, почек и печени, аспленией или гипоспленией, иммуносупрессией или потенциальной ликвореей: для лиц с хроническими заболеваниями почек и дисфункцией селезенки, у которых ослабление иммунного ответа может следует ожидать дальнейших доз каждые 5 лет.
Т-независимые вакцины могут быть преобразованы в эффективные Т-зависимые вакцины путем их ковалентного связывания (процесс, называемый конъюгацией) с молекулой белка [9–11].После фагоцитоза незрелыми дендритными клетками конъюгированные молекулы белков и полисахаридов представлены как комплексами MHC II: белок, так и комплексами MHC II: полисахарид на клеточной поверхности. Миграция в дренирующий лимфатический узел перенесет эту активированную зрелую дендритную клетку в область, богатую Т-клетками, и приведет к активации T H 2 с высокой специфичностью в отношении белка-носителя.
Одновременное прохождение вакцинного антигена по дренирующим лимфатическим каналам в богатую В-клетками область дренирующих лимфатических узлов приводит к связыванию между конъюгатом полисахарид: белок и В-клеткой, BCR которой обладает высокой специфичностью к полисахариду.Комплекс полисахарид: белок интернализуется, подвергается фагоцитозу, и белок экспрессируется в виде комплекса клеточной поверхности с MHC II. Затем происходит связанное распознавание между активированной Т Н 2 с высокой специфичностью в отношении белка-носителя и этой В-клеткой. Вовлечение T H 2 приводит к костимуляции и высвобождению цитокинов, что приводит к образованию IgM, затем IgG и образованию клеток памяти.
Затем происходит связанное распознавание между активированной Т Н 2 с высокой специфичностью в отношении белка-носителя и этой В-клеткой. Вовлечение T H 2 приводит к костимуляции и высвобождению цитокинов, что приводит к образованию IgM, затем IgG и образованию клеток памяти.
Преимущества субъединичных вакцин такие же, как у анатоксинов, с дополнительным преимуществом, заключающимся в том, что можно отличить вакцинированных людей от инфицированных — например, при вакцинации против гепатита В возможен только адаптивный иммунный ответ на поверхностный антиген, тогда как при инфекции core Возникают ответы и e .
Субъединичные вакцины имеют те же недостатки, что и анатоксинные вакцины, а именно необходимость использования адъюванта (и часто многократных доз) вместе с частым возникновением местных реакций в месте инъекции.
Активный ослабленный
Вариоляция, процедура, разработанная в Китае и Индии ∼1000 г.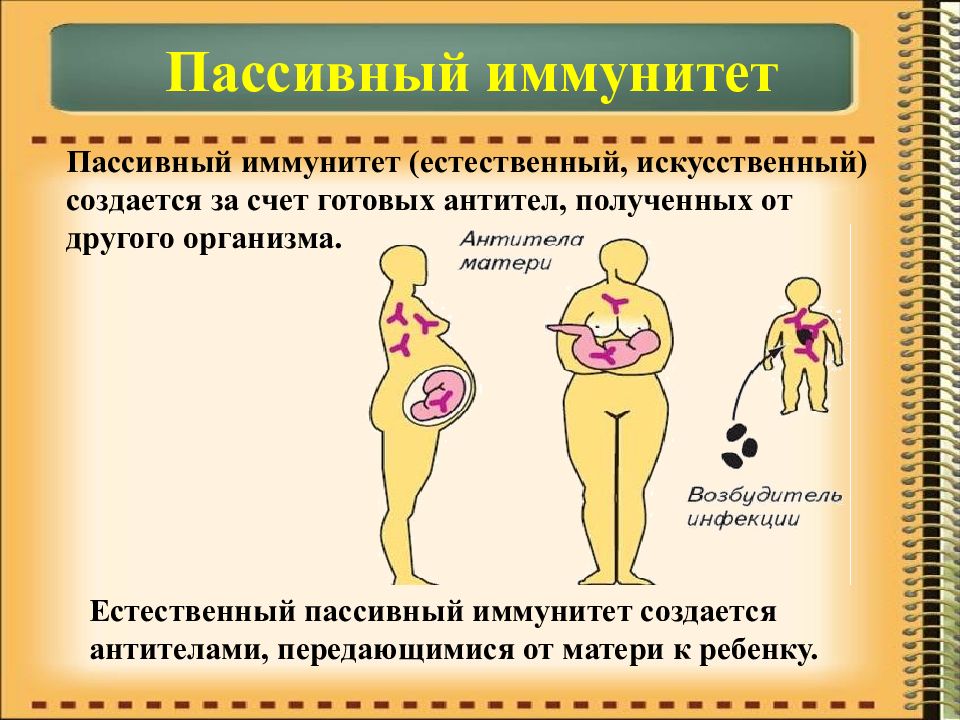 н.э., для выработки иммунитета использовалась живая вакцина против оспы – с использованием нескольких различных методов «здоровые люди» подвергались воздействию вируса оспы от человека с более легкой формой оспы – предположительно в ожидании, что это вызовет менее тяжелое заболевание у реципиента — ранняя форма «затухания» [3,4].
н.э., для выработки иммунитета использовалась живая вакцина против оспы – с использованием нескольких различных методов «здоровые люди» подвергались воздействию вируса оспы от человека с более легкой формой оспы – предположительно в ожидании, что это вызовет менее тяжелое заболевание у реципиента — ранняя форма «затухания» [3,4].
Существует несколько подходов к аттенуации вирусного патогена для применения у людей. Один предполагает выращивание вируса на чужом хозяине — например, вирус кори культивируют в фибробластах куриного яйца — репликация вируса в таких условиях приводит к появлению ряда мутантных типов: затем отбираются мутанты с повышенной вирулентностью для чужеродного хозяина. в качестве потенциальных вакцинных штаммов, поскольку они обычно проявляют пониженную вирулентность для человека-хозяина, и это особенно полезный подход для РНК-вирусов, которые имеют высокую скорость мутации.Молекулярная основа аттенуации в этих обстоятельствах неизвестна, поскольку процесс в значительной степени носит эмпирический характер и невозможно определить, какие из наблюдаемых изменений геномных нуклеотидов связаны со сниженной вирулентностью.
Альтернативный подход заключается в выращивании дикого вируса в искусственной питательной среде при температуре ниже, чем в человеческом организме — со временем может появиться штамм, который хорошо растет при этой более низкой температуре, но размножается в организме человека так медленно, что адаптивный иммунитет ответные меры способны устранить его до того, как вирус сможет распространиться и вызвать инфекцию — примером этого является адаптированная к холоду живая аттенуированная вакцина против гриппа.
Живые аттенуированные вакцины, которые могут использоваться на производстве, включают вакцины против кори, эпидемического паротита, краснухи и ветряной оспы. На примере кори вакцину вводят глубоко подкожно/внутримышечно, при этом вирионы проникают в различные типы клеток с помощью эндоцитоза, опосредованного рецепторами. В цитозоле происходит протеолитическая деградация вирусных белков; полученные пептиды затем загружаются на молекулы главного комплекса гистосовместимости типа I, и этот комплекс экспонируется на поверхности клетки.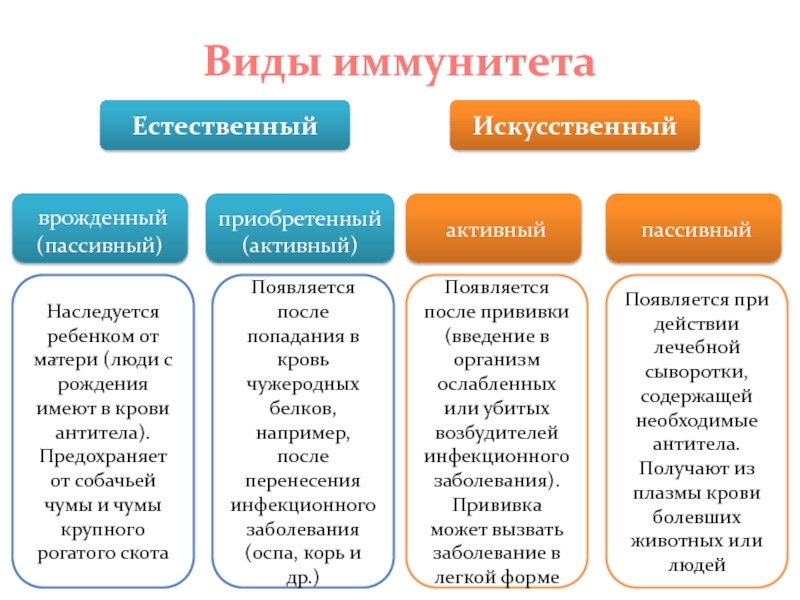 Циркулирующие цитотоксические Т-клетки (Tc) с соответствующими высокоспецифичными TCR способны распознавать комплекс и высвобождать цитокины, которые инструктируют (инфицированные) клетки подвергаться запрограммированному самоубийству (апоптозу) [12].Похоже, что некоторые Tc становятся клетками памяти, но основа этого не до конца понятна.
Циркулирующие цитотоксические Т-клетки (Tc) с соответствующими высокоспецифичными TCR способны распознавать комплекс и высвобождать цитокины, которые инструктируют (инфицированные) клетки подвергаться запрограммированному самоубийству (апоптозу) [12].Похоже, что некоторые Tc становятся клетками памяти, но основа этого не до конца понятна.
Кроме того, незрелые дендритные клетки будут фагоцитировать вирусную вакцину, инициируя тот же процесс, ранее описанный для белковых антигенов, который приводит к продукции плазматических клеток, нейтрализующих IgG-антитела и В-клетки памяти.
У адекватно иммунизированного человека при вдыхании дикого вируса кори срабатывают оба механизма защиты — так, при локальном размножении вируса в месте заражения Тс способны убивать инфицированные клетки; для вируса, который уклоняется от этого и распространяется через кровоток, антитела IgG связываются с ним и предотвращают заболевание, нейтрализуя прикрепление к клетке-мишени [9].
Одним из недостатков живых аттенуированных вакцин является возможность того, что они могут вызвать болезнь, от которой они предназначены защищать, либо потому, что они возвращаются к вирулентности, либо потому, что у некоторых людей (например, у тех, у кого иммуносупрессия) они недостаточно аттенуированы.
Заключение
Доступные в настоящее время коммерческие вакцины получают из живых аттенуированных, убитых/инактивированных препаратов, анатоксинов или субъединичных препаратов. Т-независимые антигены (обычно полисахариды) могут быть преобразованы в эффективные Т-зависимые вакцины путем конъюгации молекулы полисахарида с белком-носителем.
Препараты гаммаглобулина (IgG) против ветряной оспы и вируса гепатита В являются примерами пассивного иммунитета, который широко применяется в сфере гигиены труда.
Конфликт интересов
Не объявлено.
Каталожные номера
1..Профессиональные инфекции у медицинских работников. Часть I
,Ann Intern Med
,1996
, vol.125
(стр.826
—834
)2..Профессиональные инфекции у медицинских работников. Часть II
,Ann Intern Med
,1996
, vol.
125
(стр.917
—928
)3., , , . ,Вакцины нового поколения
,1997
2-е изданиеMarcel Dekker, Inc
4., , . ,Зеленая книга — Иммунизация против инфекционных заболеваний
, изд. 5 2006 г., , , .Химическая характеристика столбнячного токсина и анатоксина
,Eur J Biochem
,1970
, vol.17
(стр.100
—105
)6..От «дифтерийного» яда к молекулярной токсикологии
,Am Soc Microbiol News
,1, 90
53
(стр.547
—550
) 7., , .Иммунохимия столбнячного токсина
,Eur J Biochem
,1973
, vol.39
(стр.171
—181
)8., , , , , .Роль алюминийсодержащих адъювантов в интернализации антигена дендритными клетками in vitro
,Вакцина
,2005
, vol.23
(стр.1588
—1595
)9., , . ,Клеточная и молекулярная иммунология
,2000
4-е изд.
Филадельфия
W.B. Saunders и Company
10.TAK, SAUNDERS
,Иммунный ответ: базовые и клинические принципы
,2006
Elsevier
11.Janeway
11.Janeway, Travers
,Иммунобиология: иммунная система в здоровье и болезни
,1997
3-е изд.Current Biology Ltd/Garland Publishing
12., , , и другие.SLAM (CD150)-независимое проникновение вируса кори, выявленное с помощью рекомбинантного вируса, экспрессирующего зеленый флуоресцентный белок
76
(стр.6743
—6749
)© Автор, 2007 г. Опубликовано Oxford University Press от имени Общества медицины труда. Все права защищены. Чтобы получить разрешение, отправьте электронное письмо по адресу: [email protected]
.Иммунная система (для родителей) — Nemours KidsHealth
Что такое иммунная система?
Иммунная система – это защита организма от инфекций. Иммунная система (ih-MYOON) атакует микробы и помогает нам оставаться здоровыми.
Иммунная система (ih-MYOON) атакует микробы и помогает нам оставаться здоровыми.
Какие части иммунной системы?
Многие клетки и органы работают вместе, чтобы защитить тело. Лейкоциты, также называемые лейкоцитами (LOO-kuh-sytes), играют важную роль в иммунной системе.
Некоторые типы лейкоцитов, называемые фагоцитами (FAH-guh-sytes), пережевывают вторгшиеся организмы. Другие, называемые лимфоцитами (LIM-fuh-sytes), помогают организму запомнить захватчиков и уничтожить их.
Одним из типов фагоцитов является нейтрофил (NOO-truh-fil), который борется с бактериями. Когда у кого-то может быть бактериальная инфекция, врачи могут назначить анализ крови, чтобы увидеть, не вызвала ли она в организме большое количество нейтрофилов. Другие типы фагоцитов выполняют свою работу, чтобы убедиться, что организм реагирует на захватчиков.
Два вида лимфоцитов: В-лимфоциты и Т-лимфоциты . Лимфоциты начинают свой путь в костном мозге и либо остаются там и созревают в В-клетки, либо попадают в вилочковую железу, чтобы созревать в Т-клетки.В-лимфоциты подобны военной разведывательной системе организма — они находят свои цели и посылают средства защиты, чтобы зафиксировать их. Т-клетки как солдаты — они уничтожают захватчиков, которых находит система разведки.
Лимфоциты начинают свой путь в костном мозге и либо остаются там и созревают в В-клетки, либо попадают в вилочковую железу, чтобы созревать в Т-клетки.В-лимфоциты подобны военной разведывательной системе организма — они находят свои цели и посылают средства защиты, чтобы зафиксировать их. Т-клетки как солдаты — они уничтожают захватчиков, которых находит система разведки.
Как работает иммунная система?
Когда организм обнаруживает чужеродные вещества (называемые антигенами), иммунная система начинает распознавать антигены и избавляться от них.
В-лимфоциты запускаются для производства антител (также называемых иммуноглобулинами ).Эти белки фиксируются на определенных антигенах. После того, как они сделаны, антитела обычно остаются в нашем организме на случай, если нам снова придется бороться с тем же микробом. Вот почему тот, кто заболел какой-либо болезнью, например ветряной оспой, обычно не заболевает снова.
Таким же образом иммунизация (вакцины) предотвращает некоторые заболевания.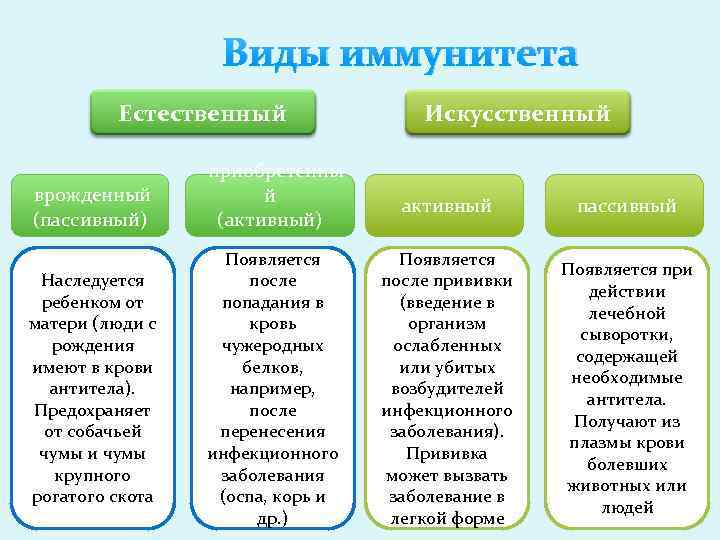 Иммунизация знакомит организм с антигеном таким образом, чтобы никто не заболел. Но это позволяет организму вырабатывать антитела, которые защитят человека от будущей атаки микроба.
Иммунизация знакомит организм с антигеном таким образом, чтобы никто не заболел. Но это позволяет организму вырабатывать антитела, которые защитят человека от будущей атаки микроба.
Хотя антитела могут распознавать антиген и связываться с ним, они не могут уничтожить его без посторонней помощи. Это работа Т-клеток . Они уничтожают антигены, помеченные антителами, или клетки, инфицированные или каким-либо образом измененные. (Некоторые Т-клетки на самом деле называются «клетками-киллерами».) Т-клетки также помогают другим клеткам (например, фагоцитам) выполнять свою работу.
Антитела также могут:
- нейтрализуют токсины (ядовитые или повреждающие вещества), вырабатываемые различными организмами
- активируют группу белков, называемых комплементарными , которые являются частью иммунной системы.Комплемент помогает убивать бактерии, вирусы или инфицированные клетки.
Эти специализированные клетки и части иммунной системы обеспечивают защиту организма от болезней. Эта защита называется иммунитетом.
Эта защита называется иммунитетом.
У человека есть три типа иммунитета — врожденный, адаптивный и пассивный:
- Врожденный иммунитет: Каждый рождается с врожденным (или естественным) иммунитетом, типом общей защиты. Например, кожа действует как барьер, препятствующий проникновению микробов в организм.И иммунная система распознает, когда определенные захватчики являются чужеродными и могут быть опасными.
- Адаптивный иммунитет: Адаптивный (или активный) иммунитет развивается на протяжении всей нашей жизни. У нас развивается адаптивный иммунитет, когда мы подвергаемся воздействию болезней или когда нас иммунизируют против них с помощью вакцин.
- Пассивный иммунитет: Пассивный иммунитет «заимствован» из другого источника и действует недолго. Например, антитела в грудном молоке матери дают ребенку временный иммунитет к заболеваниям, которым подвергалась мать.
Для развития иммунной системы требуется время, и ей нужны вакцины. Своевременно получая все рекомендованные вашему ребенку вакцины, вы можете помочь своему ребенку сохранить здоровье настолько, насколько это возможно.
Своевременно получая все рекомендованные вашему ребенку вакцины, вы можете помочь своему ребенку сохранить здоровье настолько, насколько это возможно.
Естественный иммунитет против вакциноприобретенного иммунитета: что лучше?
Иммунитет лучше приобрести через инфекцию или вакцинацию?
Иммунная система человека вырабатывает одни и те же антитела в ответ, скажем, на инфекцию ветряной оспы и вакцинацию против ветряной оспы.Люди, переболевшие ветряной оспой, и люди, получившие вакцину против ветряной оспы, хорошо защищены от инфекции в будущем. В обоих случаях организм «помнит» и может быстро выработать иммунный ответ для атаки на вирус ветряной оспы, если он снова встретится, даже через 20 лет после заражения или вакцинации.
Некоторые люди считают, что естественный иммунитет, развившийся после заражения, предпочтительнее иммунитета, приобретенного с помощью вакцин. Оба типа иммунитета (естественный и приобретенный) имеют свои плюсы и минусы.Узнайте больше о естественном и приобретенном иммунитете, в том числе о том, что известно о естественном иммунитете и вакцинном иммунитете для COVID-19.
Оба типа иммунитета (естественный и приобретенный) имеют свои плюсы и минусы.Узнайте больше о естественном и приобретенном иммунитете, в том числе о том, что известно о естественном иммунитете и вакцинном иммунитете для COVID-19.
В отношении некоторых инфекционных заболеваний, против которых существуют вакцины, естественное инфицирование вызывает более сильный иммунитет, чем иммунитет, приобретенный в результате вакцинации. По данным Детской больницы Филадельфии (CHOP), «иммунитет от болезни часто следует за единичной естественной инфекцией, [но] иммунитет от вакцин обычно возникает только после нескольких доз.Так обстоит дело с ветряной оспой — обычно вы получаете иммунитет уже после одного приступа ветряной оспы, но людям нужны две дозы вакцины против ветряной оспы, чтобы выработать эффективный и продолжительный иммунитет.
Одна из причин, по которой естественный иммунитет настолько силен, заключается в том, что люди обычно не заболевают в ответ на контакт с микробами, если только они не подвергаются воздействию большого количества вирусов или бактерий. Иммунная система сильно реагирует на эту высокую «дозу» микробов. Эта мощная реакция также отвечает за многие неприятные симптомы, которые вы чувствуете, когда вы больны, такие как усталость, лихорадка и озноб.
Иммунная система сильно реагирует на эту высокую «дозу» микробов. Эта мощная реакция также отвечает за многие неприятные симптомы, которые вы чувствуете, когда вы больны, такие как усталость, лихорадка и озноб.
С другой стороны, бесчисленное множество микробов, таких как вирус папилломы человека (ВПЧ), эволюционируют, чтобы избежать обнаружения иммунной системой. Здоровая иммунная система в конечном итоге избавляет от ВПЧ в 90% случаев, но люди с ослабленным иммунитетом особенно уязвимы к длительной инфекции, а также к повторному заражению.
Самым большим недостатком естественной инфекции является то, что невозможно заранее узнать, насколько серьезной будет инфекция. У большинства людей ветрянка вызывает дискомфорт.Но у некоторых людей также развивается инфекция легких, отек головного мозга или опасная для жизни инфекция крови. До того, как прививки от ветряной оспы стали широко доступны, примерно 10 000 человек в Соединенных Штатах ежегодно госпитализировались с осложнениями ветряной оспы, и около 100 человек ежегодно умирали от ветряной оспы.
Вакцины стимулируют выработку организмом антител и клеток памяти, необходимых для борьбы с конкретными инфекциями.Вакцина против ветряной оспы содержит небольшое количество ослабленного (аттенуированного) вируса ветряной оспы — достаточное для того, чтобы иммунная система начала вырабатывать антитела, но недостаточное для того, чтобы в организме появились волдыри от ветряной оспы. Вакцины против полиомиелита и гриппа содержат мертвые (инактивированные или «убитые») вирусы; они не могут вызвать болезнь, но запускают иммунную систему. Вакцины мРНК COVID-19 (и вакцина против вирусного вектора от Johnson & Johnson) учат клетки вырабатывать шиповидные белки, подобные белкам коронавируса, а затем организм вырабатывает антитела против этих белков.
Хотя побочные эффекты, такие как болезненность и лихорадка, являются обычным явлением после вакцинации, большинство людей после вакцинации не чувствуют себя такими паршивыми, как при заражении инфекцией.
В некоторых случаях вакцинный иммунитет сильнее естественного. Согласно CHOP, вакцины против ВПЧ, столбняка, Haemophilus influenzae типа b (Hib) и пневмококка вызывают лучший иммунный ответ, чем естественная инфекция.
Натуральный и натуральныйвакцинный иммунитет к COVID-19Исследователи все еще изучают естественный и индуцированный вакциной иммунитет к COVID-19. В настоящее время поставщики медицинских услуг считают, что как инфекция COVID-19, так и вакцинация против COVID-19 создают иммунитет, который, вероятно, длится не менее восьми месяцев. Этот иммунитет не является полным; можно заразиться COVID-19 после вакцинации против COVID-19 или более раннего приступа инфекции, хотя эти случаи обычно не являются тяжелыми.
Как инфекция COVID-19, так и вакцинация вызывают выработку специализированных иммунных клеток, необходимых для длительного иммунитета.Этот тип иммунитета может не предотвратить заражение или повторное заражение, но снижает вероятность развития у вас тяжелого случая COVID-19.
Точная продолжительность и сила иммунитета в любом случае пока не известны, поскольку COVID-19 все еще является новым заболеванием. Что действительно известно исследователям, так это то, что вакцинация против COVID-19 после заражения может «заострить иммунитет», и это хорошо. Вакцинация после выздоровления от COVID-19 увеличивает выработку противовирусных антител и снижает частоту повторного заражения.
Что говорят эксперты в области здравоохранения о естественном и приобретенном иммунитете Вакциноприобретенный иммунитет безопаснее естественного иммунитета. Для всех болезней, которые можно предотвратить с помощью вакцин, риск развития серьезного побочного эффекта, связанного с вакциной, намного меньше, чем риск серьезных осложнений в случае инфицирования. Любой, кто заражается COVID-19, имеет определенный уровень риска госпитализации и долгосрочных побочных эффектов, включая синдром пост-COVID-19 (или «долгосрочный COVID»), но для некоторых риск выше, чем для других.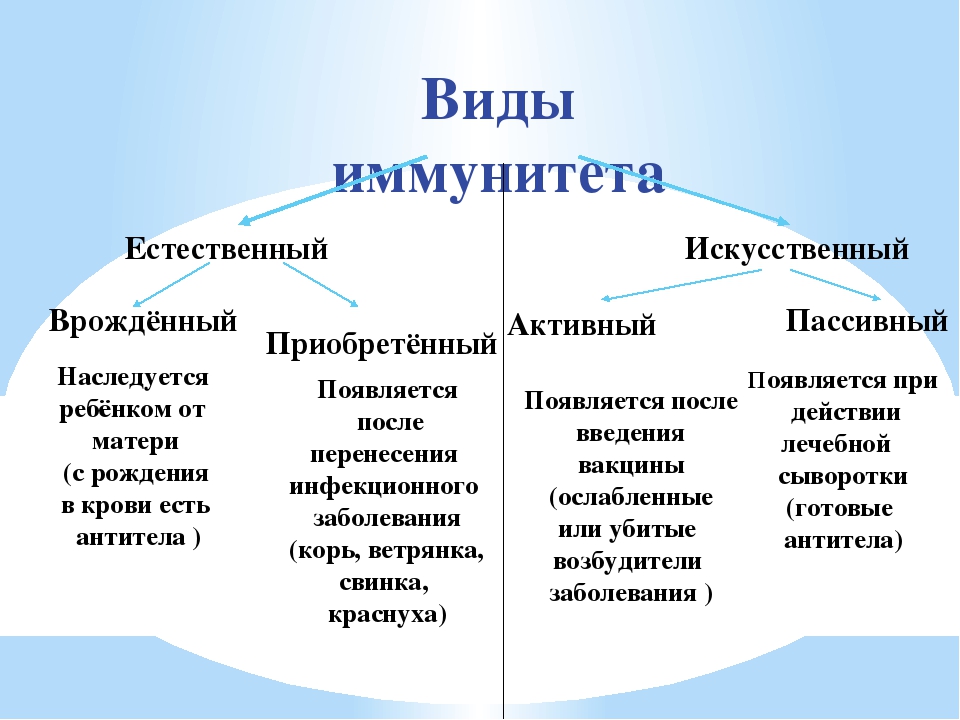 Существуют известные факторы риска тяжелого течения COVID-19, такие как болезни сердца, но у тысяч людей, не имеющих ни одного из этих факторов риска, развилась тяжелая форма COVID-19. Человеку, получившему вакцину против COVID-19, вряд ли потребуется госпитализация или у него разовьется пост-COVID-19-синдром.
Существуют известные факторы риска тяжелого течения COVID-19, такие как болезни сердца, но у тысяч людей, не имеющих ни одного из этих факторов риска, развилась тяжелая форма COVID-19. Человеку, получившему вакцину против COVID-19, вряд ли потребуется госпитализация или у него разовьется пост-COVID-19-синдром.
В большинстве случаев эксперты в области здравоохранения рекомендуют вакцинацию вместо естественной инфекции, если она доступна. Если у вас есть вопросы о естественном и приобретенном иммунитете, поговорите со своим лечащим врачом.
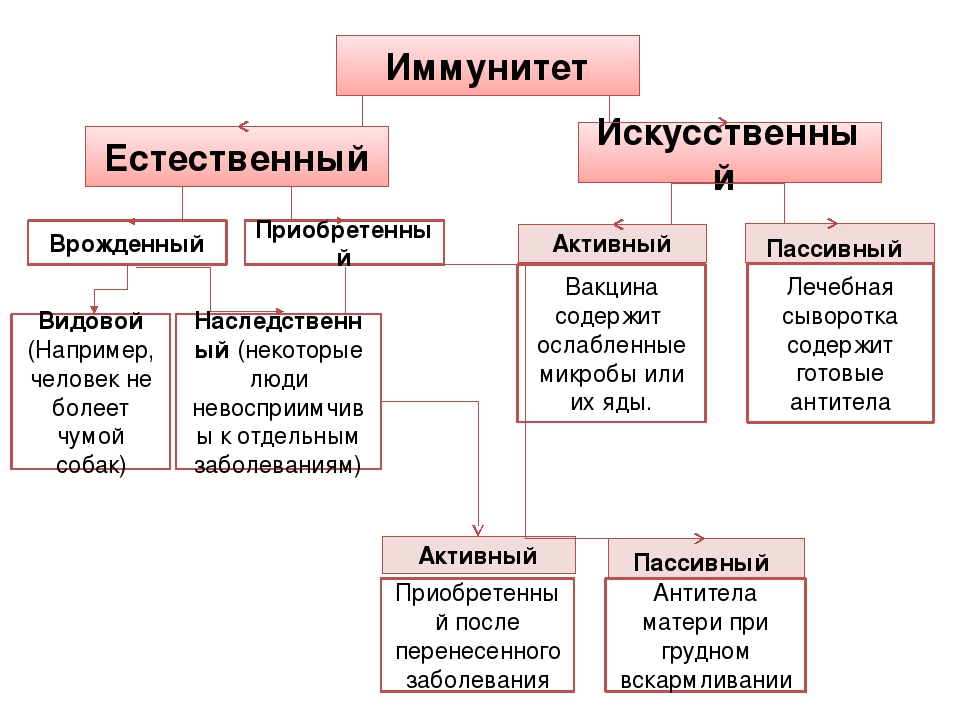



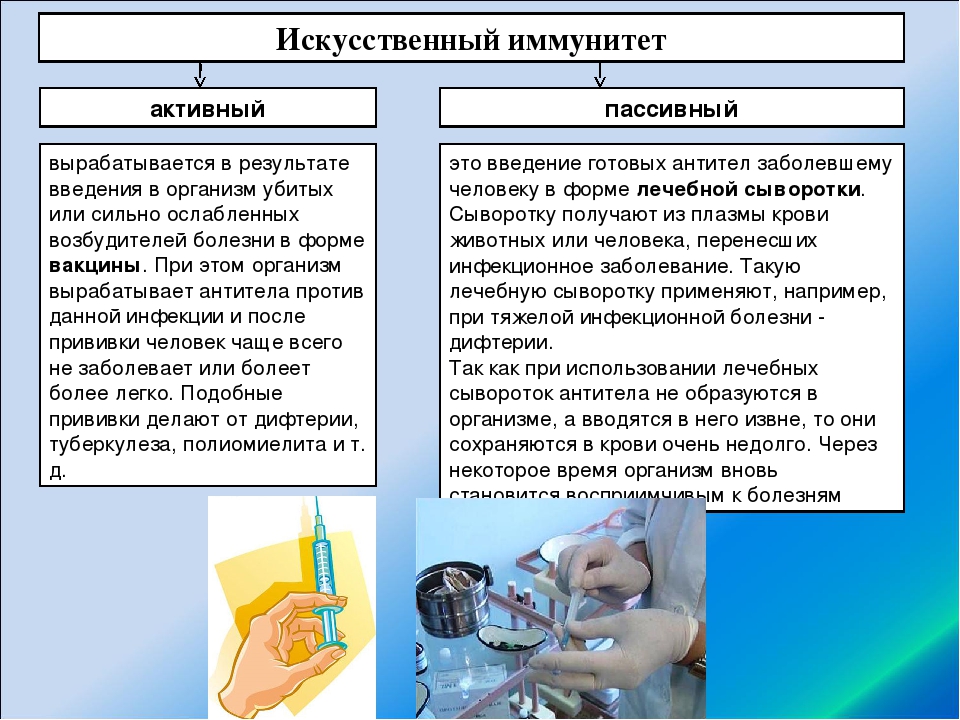


 Electronic address:
Electronic address: 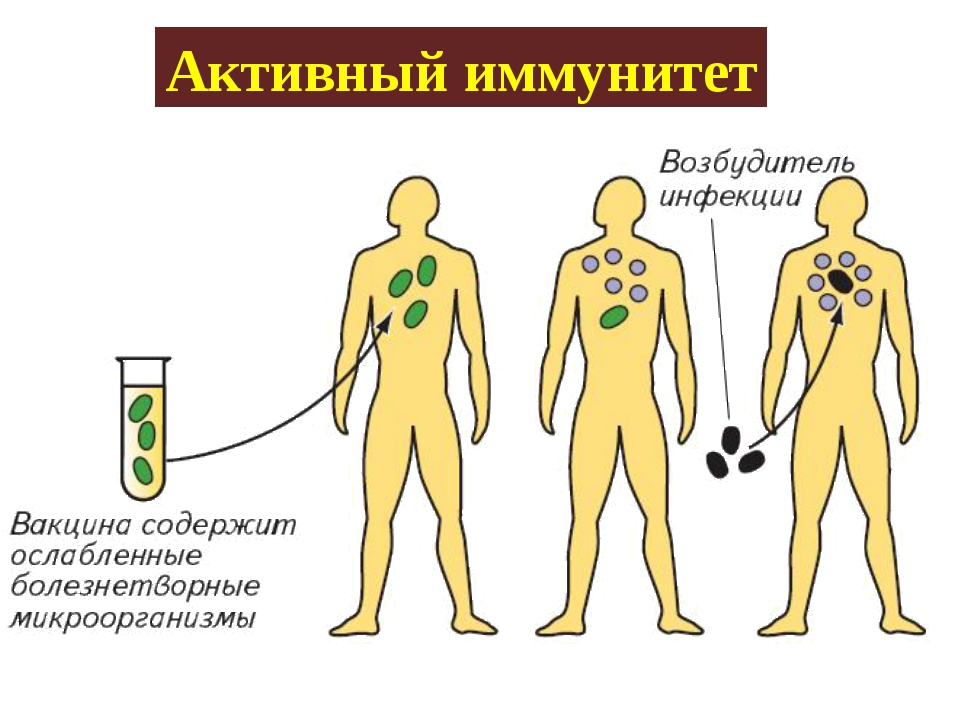
 )].
)]. 2010.
PMID: 21208547
2010.
PMID: 21208547 2020;39(1):21-36. дои: 10.1080/08830185.2019.1685990. Epub 2019 9 ноября.
Int Rev Immunol. 2020.
PMID: 31707873
Обзор.
2020;39(1):21-36. дои: 10.1080/08830185.2019.1685990. Epub 2019 9 ноября.
Int Rev Immunol. 2020.
PMID: 31707873
Обзор. Этот продукт готовят из плазмы от проверенных доноров, отобранных в США. В одном миллилитре содержится не менее 100 МЕ антител к гепатиту В.Его профессиональное использование предназначено для немедленной защиты неиммунных медицинских работников, подвергшихся воздействию вирусов гепатита В (вместе с соответствующей программой вакцинации).
Этот продукт готовят из плазмы от проверенных доноров, отобранных в США. В одном миллилитре содержится не менее 100 МЕ антител к гепатиту В.Его профессиональное использование предназначено для немедленной защиты неиммунных медицинских работников, подвергшихся воздействию вирусов гепатита В (вместе с соответствующей программой вакцинации). Каждый миллилитр содержит 40–180 мг/мл человеческого белка, из которых не менее 95% составляют гаммаглобулины (IgG). Этот продукт готовят из плазмы от проверенных доноров, отобранных в США.Один миллилитр содержит не <100 МЕ противостолбнячных антител. Маловероятно, что этот препарат будет использоваться для медицинских работников; его вводят как при лечении ран, склонных к столбняку, при сильном загрязнении почвы/навоза, так и при лечении всех ран, если считается, что человек не имеет иммунитета.
Каждый миллилитр содержит 40–180 мг/мл человеческого белка, из которых не менее 95% составляют гаммаглобулины (IgG). Этот продукт готовят из плазмы от проверенных доноров, отобранных в США.Один миллилитр содержит не <100 МЕ противостолбнячных антител. Маловероятно, что этот препарат будет использоваться для медицинских работников; его вводят как при лечении ран, склонных к столбняку, при сильном загрязнении почвы/навоза, так и при лечении всех ран, если считается, что человек не имеет иммунитета.