Химический состав клетки. Биоэлементы
Вспомните!
1. Что такое химический элемент?
Определенный вид атома
2. Какие химические элементы преобладают в земной коре?
Наибольшее распространение в земной коре имеют 46 элементов, из них 8 составляют 97,2—98,8% ее массы, 2 (кислород й кремний) — 75% от общей массы Земли.
Распределение химических элементов в процентах от массы земном коры (по А. Е. Ферсману) следующее в %:
Кислород 49,13
Кремний 26,00
Алюминий 7,45
Железо 4,20
Кальций 3,25
Натрий 2,40
Первые 13 элементов (за исключением титана), наиболее часто встречающиеся в земной коре, входят в состав органического вещества растений, участвуют во всех жизненно необходимых процессах и играют важную роль в плодородии почв.
3. Что вам известно о роли таких химических элементов, как иод, кальций, железо, в жизнедеятельности организмов?
Биологическая роль кальция. Прежде всего, кальций является важнейшим структурным компонентом костей и зубов. Также кальций регулирует проницаемость клеточных мембран, а также инициирует ответы клеток на различные внешние стимулы. Присутствие кальция в клетки или во внеклеточной среде обуславливает дифференцировку клетки, а также сокращение мышц, секрецию и перистальтику. Кальций регулирует активность многих ферментов (включая ферменты систем свертывания крови). Кальций регулирует работу некоторых эндокринных желез, обладает десенсибилизирующим и противовоспалительным эффектом.
Основные функции кальция в организме:
– структурный компонент костей и зубов
– участвует в мышечных сокращениях
– регулирует проницаемость клеточных мембран
– участвует проводимости сигнала по нервным клеткам
– регулирует сердечную деятельность
– участвует в свертывании крови
Биологическая роль йода.
– стимулирует рост и развитие организма
– регулирует рост и дифференцировку тканей
– повышает артериальное давление, а также частоту и силу сердечных сокращений
– регулирует (увеличивает) скорость протекания многих биохимических реакций
– регулирует обмен энергии, повышает температуру тела
– регулирует белковый, жировой, водно-электролитный обмен
– регулирует обмен витаминов
– повышает потребление тканями кислорода
Железо входит в группу эссенциальных (жизненно важных) микроэлементов.
Ранее из-за относительно высокого содержания его в организме (4,0-4,5 грамма в теле взрослого человека) его относили к макроэлементам. Однако 75-80% железа сосредоточено в гемоглобине крови и еще примерно 20% железа запасается в печени и селезенке. В остальных же тканях его концентрация сопоставима с микроэлементами.
В остальных же тканях его концентрация сопоставима с микроэлементами.
Биологическая роль железа
– обеспечивает транспорт кислорода (входит в состав гемоглобина)
– обеспечивает транспорт электронов в окислительно-восстановительных реакциях организма (входит в состав цитохромов и железосеропротеидов)
– участвует в формировании активных центров окислительно-восстановительных ферментов
Вопросы для повторения и задания
1. В чём заключается сходство биологических систем и объектов неживой природы?
В живой природе обнаружено около 90 химических элементов, т. е. большая часть всех известных на сегодняшний день. Никаких специальных элементов, характерных только для живых организмов, не существует, и это является одним из доказательств общности живой и неживой природы. Но количественное содержание тех или иных элементов в живых организмах и в окружающей их неживой среде существенно отличается.
2. Перечислите биоэлементы и объясните, каково их значение в образовании живой материи.
Макроэлементы. I группа. Главными компонентами всех органических соединений, выполняющих биологические функции, являются кислород, углерод, водород и азот. Все углеводы и липиды содержат водород, углерод и кислород, а в состав белков и нуклеиновых кислот, кроме этих компонентов, входит азот. На долю этих четырёх элементов приходится 98% от массы живых клеток. II группа. К группе макроэлементов относятся также фосфор, сера, калий, магний, натрий, кальций, железо, хлор. Эти химические элементы являются обязательными компонентами всех живых организмов. Содержание каждого из них в клетке составляет от десятых до сотых долей процента от общей массы.
3. Что такое микроэлементы? Приведите примеры и охарактеризуйте биологическое значение этих элементов.
Существует большая группа химических элементов, которые содержатся в организмах в очень низких концентрациях. Это алюминий, медь, марганец, цинк, молибден, кобальт, никель, иод, селен, бром, фтор, бор и многие другие. На долю каждого из них приходится не более тысячных долей процента, а общий вклад этих элементов в массу клетки — около 0,02%. В растения и микроорганизмы микроэлементы поступают из почвы и воды, а в организм животных — с пищей, водой и воздухом. Роль и функции элементов этой группы в различных организмах весьма разнообразны. Как правило, микроэлементы входят в состав биологически активных соединений (ферментов, витаминов и гормонов), и их действие проявляется главным образом в том, как они влияют на обмен веществ. Кобальт входит в состав витамина В12 и принимает участие в синтезе гемоглобина, его недостаток приводит к анемии.
Молибден в составе ферментов участвует в фиксации азота у бактерий и обеспечивает работу устьичного аппарата у растений.
Медь является компонентом фермента, участвующего в синтезе меланина (пигмента кожи), влияет на рост и размножение растений, на процессы кроветворения у животных организмов.
Иод у всех позвоночных животных входит в состав гормона щитовидной железы — тироксина. Бор влияет на ростовые процессы у растений, его недостаток приводит к отмиранию верхушечных почек, цветков и завязей.
Цинк действует на рост животных и растений, а также входит в состав гормона поджелудочной железы — инсулина.
Так, например, марганец улучшает усвоение организмом меди, а фтор влияет на метаболизм стронция. Обнаружено, что некоторые организмы интенсивно накапливают определённые элементы.
Например, многие морские водоросли накапливают иод, хвощи — кремний, лютики — литий, а моллюски отличаются повышенным содержанием меди.
Микроэлементы широко используют в современном сельском хозяйстве в виде микроудобрений для повышения урожайности культур и в качестве добавок к кормам для увеличения продуктивности животных. Применяют микроэлементы и в медицине.
Применяют микроэлементы и в медицине.
4. Как отразится на жизнедеятельности клетки и организма недостаток какого-либо микроэлемента? Приведите примеры таких явлений.
Нехватка селена приводит к возникновению у человека и животных раковых заболеваний. Каждый элемент играет свою определённую, очень важную роль в обеспечении жизнедеятельности организма. Как правило, биологический эффект того или иного микроэлемента зависит от присутствия в организме других элементов, т. е. каждый живой организм — это уникальная сбалансированная система, нормальная работа которой зависит, в том числе, и правильного соотношения её компонентов на любом уровне организации.
5. Расскажите об ультрамикроэлементах. Каково их содержание в организме? Что известно об их роли в живых организмах?
Существует группа химических элементов, которые содержатся в организмах в следовых, т. е. ничтожно малых, концентрациях. К ним относят золото, бериллий, серебро и другие элементы. Физиологическая роль этих компонентов в живых организмах пока окончательно не установлена.
К ним относят золото, бериллий, серебро и другие элементы. Физиологическая роль этих компонентов в живых организмах пока окончательно не установлена.
6. Приведите примеры известных вам биохимических эндемий. Объясните причины их происхождения.
Резкий недостаток или, наоборот, избыток какого-либо химического элемента вызывает в пределах таких зон возникновение биогеохимических эндемий — заболеваний растений, животных и человека. Во многих районах нашей страны — на Урале и Алтае, в Приморье и в Ростовской области количество иода в почве и в воде значительно снижено. Если человек не получает с пищей нужного количества иода, у него снижается синтез тироксина. Щитовидная железа, пытаясь компенсировать нехватку гормона, разрастается, что приводит к образованию так называемого эндемического зоба. Особенно тяжёлые последствия от недостатка иода возникают у детей. Сниженное количество тироксина приводит к резкому отставанию в умственном и физическом развитии.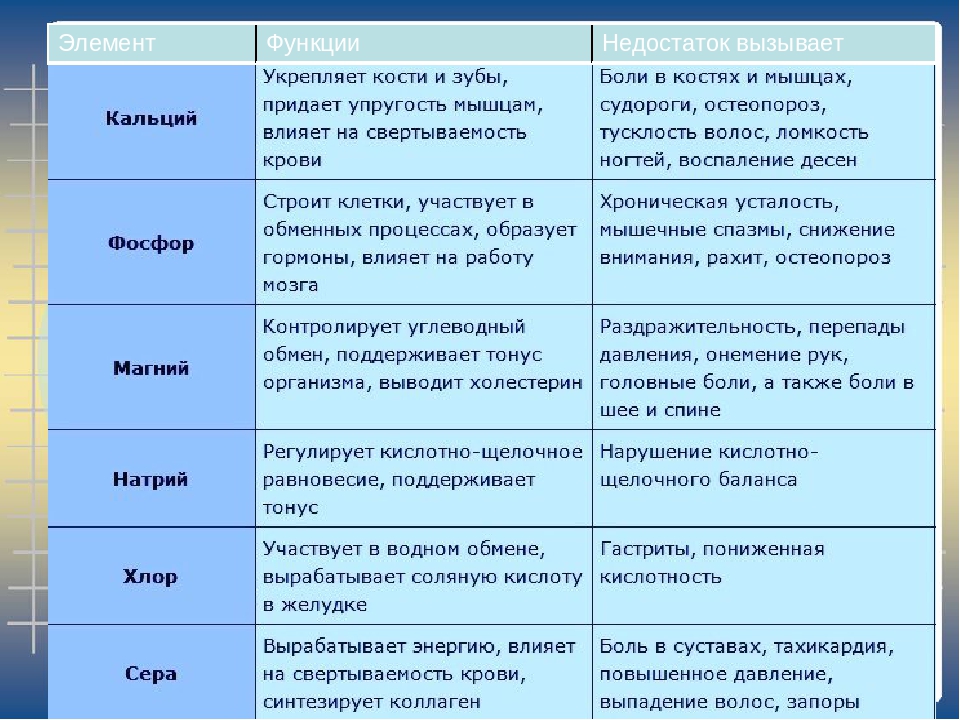 Чтобы предотвратить заболевания щитовидной железы, врачи рекомендуют подсаливать пищу специальной солью, обогащённой иодидом калия, употреблять рыбные блюда и морскую капусту.
Чтобы предотвратить заболевания щитовидной железы, врачи рекомендуют подсаливать пищу специальной солью, обогащённой иодидом калия, употреблять рыбные блюда и морскую капусту.
7. Составьте схему, иллюстрирующую элементный химический состав живых организмов.
Подумайте! Вспомните!
1. По какому принципу все химические элементы, входящие в состав живой природы, разделяют на макроэлементы, микроэлементы и ультрамикроэлементы? Предложите свою, альтернативную, классификацию химических элементов, основанную на другом принципе.
По процентному содержанию в живых клетках.
Классификация:
— биогенные элементы,
— абиогенные элементы.
Классификация:
— ионы металлов
— ионы неметаллов (бескислородные)
— ионы кислотных остатков кислородсодержащих кислот.
2. Иногда в учебниках и пособиях вместо словосочетания «элементный химический состав» можно встретить выражение «элементарный химический состав». Объясните, в чём некорректность такой формулировки.
Элементный – означает, состоящий из элементов, в данном случае химических, а элементарный – означает, слишком простой, поверхностный, ограниченный.
3. Выясните, существуют ли какие-либо особенности химического состава воды в местности, где вы живёте (например, избыток железа или нехватка фтора и т. д.). Используя дополнительную литературу и ресурсы Интернета, определите, какое влияние это может оказать на организм человека.
Некоторые водные ресурсы Челябинской области
Озеро Смолино. По химическому составу вода в озере относится к хлоридному классу, группе магния. Минерализация озерной воды высокая – 1400–1840 мг/л. Среднегодовые концентрации металлов составили: меди – 5,5 ПДК, цинка – 6,1 ПДК, марганца в северной части акватории – 6,4. Озеро Первое. По химическому составу вода в озере относится к хлоридному классу с переходом в гидрокарбонатный, группу кальция. Минерализация озерной воды повышенная – 602–983 мг/л. Среднегодовые концентрации трудноокисляемых органических соединений (ХПК) составило 1,8 ПДК, фторидов – 2,6 ПДК, меди – 5,3 ПДК, цинка – 5,8 ПДК, марганца в северной части акватории – 5,2 ПДК, в южной – 3,7 ПДК. Озеро Чебаркуль. По химическому составу вода в озере относилась к гидрокарбонатному классу, группе кальция. Среднегодовые концентрации составили: органических соединений по БПК5 – 1 ПДК, ХПК – 2,1 ПДК, азота аммония – 0,7 ПДК, азота нитритов и меди – 2 ПДК, цинка – 2,5 ПДК, марганца – 4,3 ПДК. Озеро Тургояк. Озеро Тургояк не испытывает техногенной нагрузки и используется в рекреационных целях. По химическому составу вода в озере относилась к гидрокарбонатному классу, группе кальция. Содержание в воде биогенных компонентов, нефтепродуктов, СПАВ, фторидов не превышало рыбохозяйственных нормативов, средняя концентрация органических соединений по ХПК превышала ПДК в 1,4 раза, марганца – 1,2 ПДК, меди – 2,8 ПДК, цинка – 3,4 ПДК.
Озеро Первое. По химическому составу вода в озере относится к хлоридному классу с переходом в гидрокарбонатный, группу кальция. Минерализация озерной воды повышенная – 602–983 мг/л. Среднегодовые концентрации трудноокисляемых органических соединений (ХПК) составило 1,8 ПДК, фторидов – 2,6 ПДК, меди – 5,3 ПДК, цинка – 5,8 ПДК, марганца в северной части акватории – 5,2 ПДК, в южной – 3,7 ПДК. Озеро Чебаркуль. По химическому составу вода в озере относилась к гидрокарбонатному классу, группе кальция. Среднегодовые концентрации составили: органических соединений по БПК5 – 1 ПДК, ХПК – 2,1 ПДК, азота аммония – 0,7 ПДК, азота нитритов и меди – 2 ПДК, цинка – 2,5 ПДК, марганца – 4,3 ПДК. Озеро Тургояк. Озеро Тургояк не испытывает техногенной нагрузки и используется в рекреационных целях. По химическому составу вода в озере относилась к гидрокарбонатному классу, группе кальция. Содержание в воде биогенных компонентов, нефтепродуктов, СПАВ, фторидов не превышало рыбохозяйственных нормативов, средняя концентрация органических соединений по ХПК превышала ПДК в 1,4 раза, марганца – 1,2 ПДК, меди – 2,8 ПДК, цинка – 3,4 ПДК.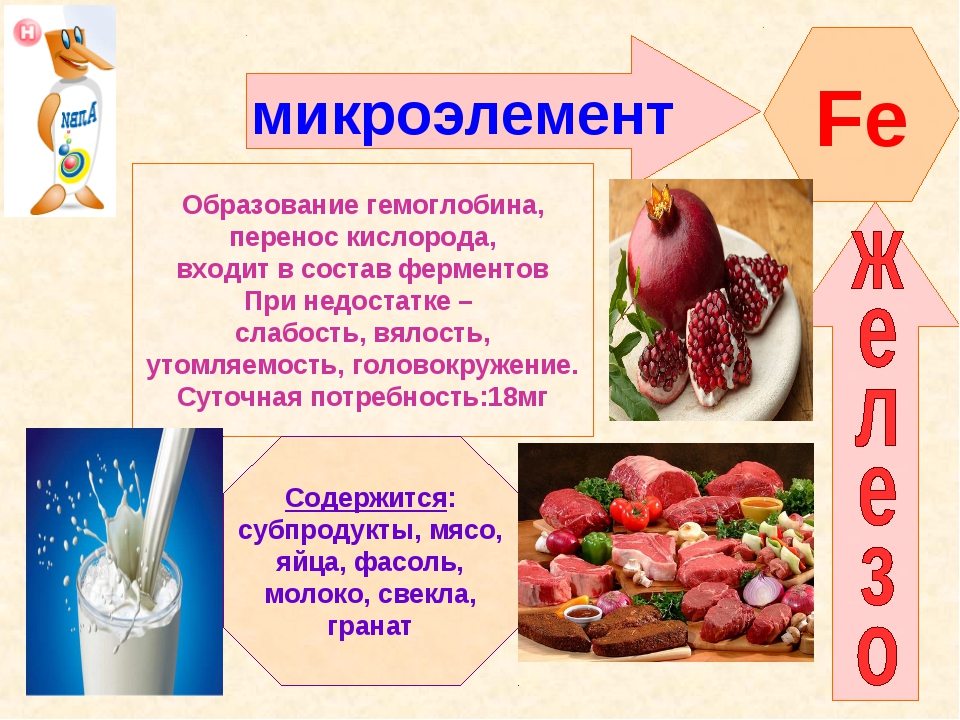
Избыток марганца
Токсической дозой для человека считается 40 мг марганца в день, летальная — не установлена. Не было выявлено фактов отравления человека марганцем из пищевых продуктов, зафиксированы случаи острой интоксикации марганцевой пылью на производстве. Развиваются тяжелые нарушения психики, в том числе галлюцинации – «марганцевое безумие», гипермоторика, гиперраздражительность. Появлению симптомов при хроническом отравлении предшествует несколько лет.
Симптомы избытка марганца:
Упадок сил, повышенная утомляемость, вялость, снижение памяти, депрессивные состояния. Двигательные нарушения: расстройства мышечного тонуса, походки, атрофия мышц, скованность и замедленность движений, парестезии. Энцефалопатия, паркинсонизм. Интерстициальные заболевания лёгких, манганокониоз.
Избыток цинка в организме
Доза цинка свыше 200 мг в сутки является рвотным средством.Продолжительный прием добавок цинка, превышающих 150 мг в день, становится причиной ухудшения работы иммунитета и появления эрозий в желудке. Среди признаков острого отравления цинком отмечались: боли в области эпигастрии, рвота, тошнота, диарея. Хроническая интоксикация приводила к вторичному дефициту меди.
Среди признаков острого отравления цинком отмечались: боли в области эпигастрии, рвота, тошнота, диарея. Хроническая интоксикация приводила к вторичному дефициту меди.
Причины избытка цинка в организме:
Чрезмерное количество поступления цинка в организм, к примеру, в процессе контакта с соединениями микроэлемента в условиях производства.Неконтролируемый прием препаратов цинка, включая цинковые мази.Нарушения цинкового обмена.
Симптомы избытка цинка:
Снижение работы иммунной системы, развитие аутоиммунных реакций. Патологические состояния ногтей, кожи, волос. Боли в области желудка, тошнота. Понижение уровня кадмия, меди, железа в организме. Нарушения работы печени, поджелудочной железы, простаты.
Избыток меди в организме
Токсичной дозой является количество 200 – 250 мг в сутки. Случаи острого отравления медью были зафиксированы: в попытках самоубийства; при наружном использовании; при случайном употреблении детьми; при приеме загрязненной питьевой воды или воды и напитков из медных контейнеров; у рабочих, трудившихся на виноградниках и применяющих соединения из меди в качестве пестицидов.
Причины избытка меди:
Избыточное поступление микроэлемента в организм: в условиях производства через вдыхание пыли и паров соединений меди, в быту — в результате отравлений растворами соединений меди, применения посуды из меди. Нарушения обмена микроэлемента.
Симптомы избытка меди:
Нарушения работы ЦНС: депрессивные состояния, бессонница, снижение памяти. «Медная лихорадка» при вдыхании паров: значительное повышение температуры, обильное потоотделение, озноб, спазмы в икроножных мышцах. Пыль и окись меди провоцирует слезотечение, раздражение слизистых оболочек и конъюнктивы, чихание, жжение в зеве, головную боль, слабость, боли в мышцах, желудочно-кишечные расстройства. Нарушения работы почек и печени. Развитие цирроза печени и вторичное поражение головного мозга, обусловленное наследственным нарушением белкового обмена и обмена меди — болезнь Вильсона-Коновалова. Эта наследственная патология, связанная с процессом накопления меди в печени. Аллергические дерматозы: нейродермит, экземы, крапивница. Повышение вероятности развития атеросклероза. Эритроцитолиз (разрушение эритроцитов с выделением гемоглобина), гемоглобин в моче, малокровие. Отложение избытка микроэлемента в ткани головного мозга, в печени, миокарде, коже, поджелудочной железе.
Аллергические дерматозы: нейродермит, экземы, крапивница. Повышение вероятности развития атеросклероза. Эритроцитолиз (разрушение эритроцитов с выделением гемоглобина), гемоглобин в моче, малокровие. Отложение избытка микроэлемента в ткани головного мозга, в печени, миокарде, коже, поджелудочной железе.
2.2 Химический состав клетки
Вопрос 1. В чем заключается сходство биологических систем и объектов неживой природы?
Основное сходство — это родство химического состава. Подавляющее большинство известных на сегодняшний день химических элементов обнаружено как в живых организмах, так и в неживой природе. Атомов, характерных только для живых систем, не существует. Однако содержание конкретных элементов в живой и неживой природе резко различается. Организмы (от бактерий до позвоночных) способны избирательно накапливать элементы, которые необходимы для жизнедеятельности.
Интересно, что неживые объекты могут проявлять отдельные свойства, более характерные для живого. Так, кристаллы минералов способны к росту и обмену веществ с окружающей средой, а фосфор может «запасать» энергию света. Но всей совокупностью черт, присущих живому организму, не обладает ни одна неорганическая система.
Так, кристаллы минералов способны к росту и обмену веществ с окружающей средой, а фосфор может «запасать» энергию света. Но всей совокупностью черт, присущих живому организму, не обладает ни одна неорганическая система.
Вопрос 2. Перечислите биоэлементы и объясните, каково их значение в образовании живой материи.
К биоэлементам (органогенам) относят кислород, углерод, водород, азот, фосфор и серу. Они составляют основу белков, липидов, углеводов, нуклеиновых кислот и других органических веществ. Для всех органических молекул особое значение имеют атомы углерода, образующие каркас. К этому каркасу присоединяются разнообразные химические группы, образованные другими биоэлементами. В зависимости от состава и расположения таких групп органические молекулы приобретают индивидуальные свойства и функции. Например, аминокислоты в большом количестве содержат азот, а нуклеиновые кислоты — фосфор.
Вопрос 3. Что такое микроэлементы? Приведите примеры и охарактеризуйте биологическое значение этих элементов.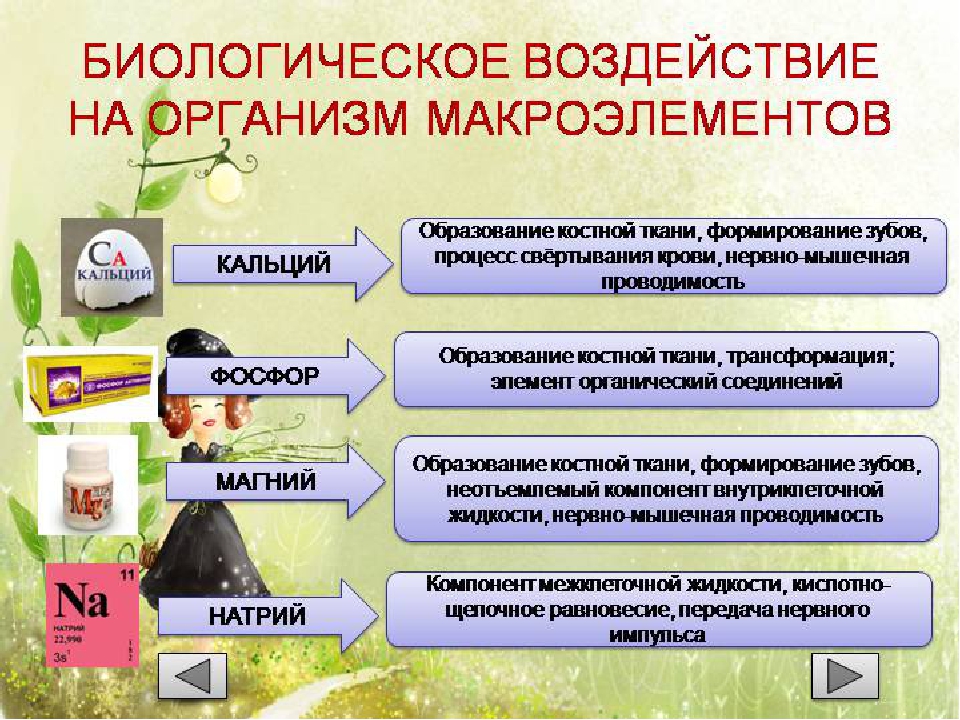
Многие химические элементы содержатся в живых системах в очень малых количествах (доли процента от общей массы). Такие вещества называют микроэлементами. В их числе медь, марганец, цинк, молибден, кобальт, иод, бром, фтор и многие другие. Растения, грибы, бактерии получают микроэлементы из почвы и воды; животные — в основном с пищей. В большинстве своем микроэлементы входят в состав белков и биологически активных веществ (гормонов, витаминов). Например, цинк содержится в гормоне поджелудочной железы инсулине, а иод — в тироксине (гормоне щитовидной железы). Кобальт является важнейшей составной частью витамина В12. Железо входит в состав примерно семидесяти белков организма, медь — в состав двадцати белков и т. д.
Вопрос 4. Как отразится на жизнедеятельности клетки и организма недостаток какого-либо микроэлемента? Приведите примеры таких явлений.
Недостаток какого-либо микроэлемента приводит к уменьшению синтеза того органического вещества, в состав которого этот микроэлемент входит.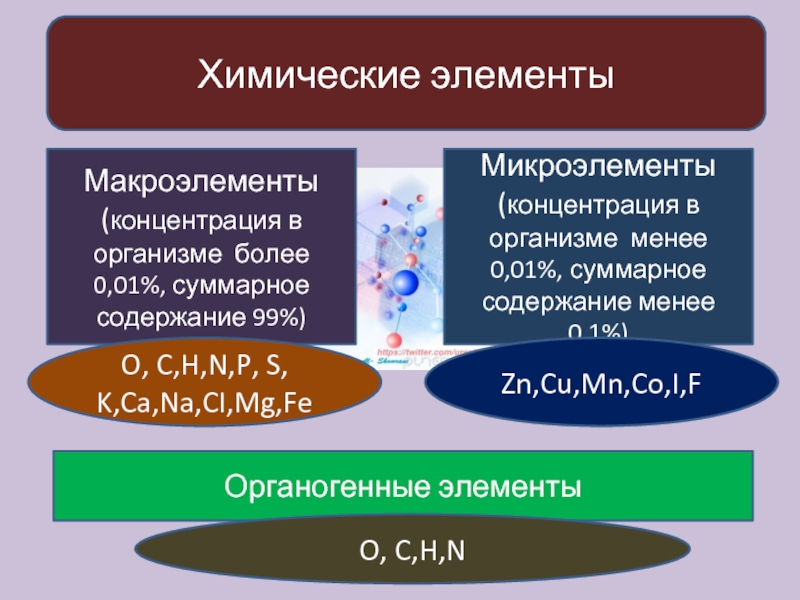 В результате нарушаются процессы роста, обмена веществ, воспроизведения и т. п. Например, дефицит иода в пище приводит к общему падению активности организма и разрастанию щитовидной железы — эндемическому зобу. Недостаток бора вызывает отмирание верхушечных почек у растений. Нехватка селена может привести к возникновению раковых заболеваний у человека и животных. По аналогии с авитаминозами такие заболевания называют микроэлементозами.
В результате нарушаются процессы роста, обмена веществ, воспроизведения и т. п. Например, дефицит иода в пище приводит к общему падению активности организма и разрастанию щитовидной железы — эндемическому зобу. Недостаток бора вызывает отмирание верхушечных почек у растений. Нехватка селена может привести к возникновению раковых заболеваний у человека и животных. По аналогии с авитаминозами такие заболевания называют микроэлементозами.
Вопрос 5. Расскажите об ультрамикроэлементах. Каково их содержание в организме? Что известно об их роли в живых организмах?
Ультрамикроэлементы — это элементы, которые содержатся в клетке в ничтожно малых количествах (концентрация каждого не превышает одной миллионной доли процента). К ним относят уран, радий, золото, серебро, ртуть, бериллий, мышьяк и др. Физиологическая роль большинства из них не установлена. Не исключено, что она вообще отсутствует, и тогда часть ультрамикроэлементов являются просто примесями живых организмов. Вместе с тем, например, известно, что мышьяк входит в состав ферментов, защищающих мембраны наших клеток от окисления, и необходим для их нормальной работы.
Вместе с тем, например, известно, что мышьяк входит в состав ферментов, защищающих мембраны наших клеток от окисления, и необходим для их нормальной работы.
Вопрос 6. Приведите примеры известных вам биохимических эндемий. Объясните причины их происхождения.
Биохимические эндемии — это заболевания растений, животных и человека, связанные с явным недостатком либо избытком какого-либо химического элемента в окружающей среде. В результате развиваются микроэлементозы или некоторые другие нарушения. Так, во многих районах нашей страны значительно снижено количество иода в воде и почве. Нехватка иода приводит к падению синтеза гормона тироксина, щитовидная железа, пытаясь компенсировать его нехватку, разрастается (развивается эндемический зоб). Другими примерами могут служить дефицит селена в почве ряда районов Монголии, а также избыток ртути в воде некоторых горных рек Чили и Цейлона.
2.2 Химический состав клетки
4. 8 (95%) 12 votes
8 (95%) 12 votes На этой странице искали :
- в чем заключается сходство биологических систем и объектов неживой природы
- перечислите биоэлементы и объясните каково их значение в образовании живой материи
- приведите примеры известных вам биохимических эндемий
- перечислите биоэлементы и объясните каково их значение
- что такое биохимические эндемии и каковы причины их происхождения
Сохрани к себе на стену!
Химический состав клетки | Параграф 2. 2
«Биология. Общая биология. Базовый уровень. 10-11 классы». В.И. Сивоглазов (гдз)
Вопрос 1. В чем заключается сходство биологических систем и объектов неживой природы?
Основное сходство — это родство химического состава. Подавляющее большинство известных на сегодняшний день химических элементов обнаружено как в живых организмах, так и в неживой природе. Атомов, характерных только для живых систем, не существует. Однако содержание конкретных элементов в живой и неживой природе резко различается. Организмы (от бактерий до позвоночных) способны избирательно накапливать элементы, которые необходимы для жизнедеятельности.
Атомов, характерных только для живых систем, не существует. Однако содержание конкретных элементов в живой и неживой природе резко различается. Организмы (от бактерий до позвоночных) способны избирательно накапливать элементы, которые необходимы для жизнедеятельности.
Можно однако выделить совокупность свойств, которые присущи всем живым существам и отличают их от тел неживой природы. Для живых объектов характерна особая форма взаимодействия с окружающей средой — обмен веществ. Основу его составляют взаимосвязанные и сбалансированные процессы ассимиляции (анаболизм) и диссимиляции (катаболизм). Эти процессы направлены на обновление структур организма, а также на обеспечение различных сторон его жизнедеятельности необходимыми питательными веществами и энергией. Обязательным условием обмена веществ служит поступление извне определенных химических соединений, т. е. существование организма как открытой системы.
Интересно, что неживые объекты могут проявлять отдельные свойства, более характерные для живого. Так, кристаллы минералов способны к росту и обмену веществ с окружающей средой, а фосфор может «запасать» энергию света. Но всей совокупностью черт, присущих живому организму, не обладает ни одна неорганическая система.
Так, кристаллы минералов способны к росту и обмену веществ с окружающей средой, а фосфор может «запасать» энергию света. Но всей совокупностью черт, присущих живому организму, не обладает ни одна неорганическая система.
Вопрос 2. Перечислите биоэлементы и объясните, каково их значение в образовании живой материи.
К биоэлементам (органогенам) относят кислород, углерод, водород, азот, фосфор и серу. Они составляют основу белков, липидов, углеводов, нуклеиновых кислот и других органических веществ. Для всех органических молекул особое значение имеют атомы углерода, образующие каркас. К этому каркасу присоединяются разнообразные химические группы, образованные другими биоэлементами. В зависимости от состава и расположения таких групп органические молекулы приобретают индивидуальные свойства и функции. Например, аминокислоты в большом количестве содержат азот, а нуклеиновые кислоты — фосфор.
В клетках некоторых организмов обнаружено повышенное содержание отдельных химических элементов. Например, бактерии способны накапливать марганец, морские водоросли — йод, ряска -радий, моллюски и ракообразные — медь, позвоночные — железо.
Например, бактерии способны накапливать марганец, морские водоросли — йод, ряска -радий, моллюски и ракообразные — медь, позвоночные — железо.
Химические элементы входят в состав органических соединений. Углерод, кислород и водород участвуют в построении молекул углеводов и жиров. В молекулы белков помимо этих элементов входят азот и сера, а в молекулы нуклеиновых кислот фосфор и азот. Ионы железа и меди включены в молекулы окислительных ферментов, магний — в молекулу хлорофилла, железо входит в состав гемоглобина, йод — в состав гормона щитовидной железы — тироксина, цинк — в состав инсулина — гормона поджелудочной железы, кобальт — в состав витамина В12.
Химические элементы, принимающие участие в процессах обмена веществ и обладающие выраженной биологической активностью, называют биогенными.
Вопрос 3. Что такое микроэлементы? Приведите примеры и охарактеризуйте биологическое значение этих элементов.
Многие химические элементы содержатся в живых системах в очень малых количествах (доли процента от общей массы). Такие вещества называют микроэлементами.
Такие вещества называют микроэлементами.
Микроэлементы: Си, В, Со, Мо, Мn, Ni, Вг, Т.п. I и другие. На их долю в клетке суммарно приходится более 0,1%; концентрация каждого не превышает 0,001%. Это ионы металлов, входящие в состав биологически активных веществ (гормонов, ферментов и др.). Растения, грибы, бактерии получают микроэлементы из почвы и воды; животные — в основном с пищей. В большинстве своем микроэлементы входят в состав белков и биологически активных веществ (гормонов, витаминов). Например, цинк содержится в гормоне поджелудочной железы инсулине, а иод — в тироксине (гормоне щитовидной железы). Кобальт является важнейшей составной частью витамина В12. Железо входит в состав примерно семидесяти белков организма, медь — в состав двадцати белков и т. д.
В клетках некоторых организмов обнаружено повышенное содержание отдельных химических элементов. Например, бактерии способны накапливать марганец, морские водоросли — йод, ряска -радий, моллюски и ракообразные — медь, позвоночные — железо. Ультрамикроэлементы: уран, золото, бериллий, ртуть, цезий, селен и другие. Их концентрация не превышает 0,000001%. Физиологическая роль многих из них не установлена.
Ультрамикроэлементы: уран, золото, бериллий, ртуть, цезий, селен и другие. Их концентрация не превышает 0,000001%. Физиологическая роль многих из них не установлена.
Вопрос 4. Как отразится на жизнедеятельности клетки и организма недостаток какого-либо микроэлемента? Приведите примеры таких явлений.
Недостаток какого-либо микроэлемента приводит к уменьшению синтеза того органического вещества, в состав которого этот микроэлемент входит. В результате нарушаются процессы роста, обмена веществ, воспроизведения и т. п. Например, дефицит иода в пище приводит к общему падению активности организма и разрастанию щитовидной железы — эндемическому зобу. Недостаток бора вызывает отмирание верхушечных почек у растений. Основной функцией железа в организме является перенос кислорода и участие в окислительных процессах (посредством десятков окислительных ферментов). Железо входит в состав гемоглибина, миоглобина, цитохромов. Железо играет важную роль в процессах выделения энергии, в обеспечении имунных реакций организма, в метаболизме холестерина. При недостатке цинка нарушается дифференцировка клеток, выработка инсулина, всасывание витамина Е, нарушается регенерация кожных клеток. Немаловажную роль цинк играет в переработке алкоголя, поэтому недостаток его в организме вызывает предрасположенность к алкоголизму (особенно у детей и подростков). Цинк входит в состав инсулина. ряда ферментов, участвует в кроветворении.
При недостатке цинка нарушается дифференцировка клеток, выработка инсулина, всасывание витамина Е, нарушается регенерация кожных клеток. Немаловажную роль цинк играет в переработке алкоголя, поэтому недостаток его в организме вызывает предрасположенность к алкоголизму (особенно у детей и подростков). Цинк входит в состав инсулина. ряда ферментов, участвует в кроветворении.
Нехватка селена может привести к возникновению раковых заболеваний у человека и животных. По аналогии с авитаминозамитакие заболевания называют микроэлементозами.
Вопрос 5. Расскажите об ультрамикроэлементах. Каково их содержание в организме? Что известно об их роли в живых организмах?
Ультрамикроэлементы — это элементы, которые содержатся в клетке в ничтожно малых количествах (концентрация каждого не превышает одной миллионной доли процента). К ним относят уран, радий, золото, серебро, ртуть, бериллий, мышьяк и др.
Мышьяк относят к условно эссенциальным, иммунотоксичным элементам. Известно, что мышьяк с белками (цистеином, глутамином), липоевой кислотой. Мышьяк оказывает влияние на окислительные процессы в митохондриях и принимает участие во многих других важных биологических процессах, он входит в состав ферментов, защищающих мембраны наших клеток от окисления, и необходим для их нормальной работы.
Известно, что мышьяк с белками (цистеином, глутамином), липоевой кислотой. Мышьяк оказывает влияние на окислительные процессы в митохондриях и принимает участие во многих других важных биологических процессах, он входит в состав ферментов, защищающих мембраны наших клеток от окисления, и необходим для их нормальной работы.
В организме литий способствует высвобождению магния из клеточных «депо» и тормозит передачу нервного импульса, тем самым снижая. возбудимость нервной системы. литий также влияет на нейроэндокринные процессы, жировой и углеводный обмен.
Ванадий принимает участие в регуляции углеводного обмена и сердечно-сосудистой системы также входит в метаболизме тканей костей и зубов. Физиологическая роль большинства из ультраэлементов не установлена. Не исключено, что она вообще отсутствует, и тогда часть ультрамикроэлементов являются просто примесями живых организмов. Многие ультрамикроэлементы токсичны для человека и животных в определённых концентрациях, например, серебро, титан, мышьяк и др.
Вопрос 6. Приведите примеры известных вам биохимических эндемий. Объясните причины их происхождения.
Биохимические эндемии — это заболевания растений, животных и человека, связанные с явным недостатком либо избытком какого-либо химического элемента в окружающей среде. В результате развиваются микроэлементозы или некоторые другие нарушения. Так, во многих районах нашей страны значительно снижено количество иода в воде и почве. Нехватка иода приводит к падению синтеза гормона тироксина, щитовидная железа, пытаясь компенсировать его нехватку, разрастается (развивается эндемический зоб). Другими примерами могут служить дефицит селена в почве ряда районов Монголии, а также избыток ртути в воде некоторых горных рек Чили и Цейлона. Наблюдается избыток фтора в воде многих районов, что приводит к заболеванию зубов — флюорозов.
Одной из форм биохимических эндемий можно считаь избыток радиоактивных элементов в районе Чернобыльской АЭС и мест, подвергшихся интенсивному радиооблучению, например,
Микроэлементы.
 Общая информация
Общая информацияХимические элементы в свободном состоянии и в виде множества химических соединений входят в состав всех клеток и тканей человеческого организма. Они являются строительным материалом, важнейшими катализаторами различных биохимических реакций, непременными и незаменимыми участниками процессов роста и развития организма, обмена веществ, адаптации к меняющимся условиям окружающей среды.
Физиологическое действие различных элементов зависит от их дозы. Поэтому токсичные элементы (мышьяк, ртуть, сурьма, кадмий и др.) при низких концентрациях могут действовать на организм как лекарство (оказывая тем самым саногенетическое воздействие), тогда как натрий, калий, кальций, железо, магний и ряд других элементов в высоких концентрациях могут обладать выраженным токсическим эффектом.
Для осуществления жизненно важных функций у каждого элемента существует оптимальный диапазон концентраций. При дефиците или избыточном накоплении элементов в организме могут происходить серьезные изменения, обуславливающие нарушение активности прямо или косвенно зависящих от них ферментов.
В организме химические элементы находятся преимущественно в виде соединений, избыточное образование или распад которых может приводить к нарушению так называемого металло-лигандного гомеостаза, а в дальнейшем и к развитию патологических изменений. Элементы – металлы и лиганды (например, глутаминовая, аспарагиновая, липоевая, аскорбиновая кислоты) могут выступать в качестве активаторов или ингибиторов различных ферментов, что обусловливает их существенную роль в развитии и терапии различных заболеваний.
Для систематизации сведений о содержании и физиологической роли химических элементов в организме в последние десятилетия был предложен ряд классификаций. Не рассматривая их подробно, остановимся лишь на некоторых принципиальных моментах.
Один из принципов классификации – разделение химических элементов на группы, в зависимости от уровня их содержания в организме человека.
Первую группу такой классификации составляют «макроэлементы», концентрация которых в организме превышает 0,01%. К ним относятся O, C, H, N, Ca, P, K, Na, S, Cl, Mg. В абсолютных значениях (из расчета на среднюю массу тела человека в 70 кг), величины содержания этих элементов колеблются в пределах от сорока с лиш ним кг (кислород) до нескольких г (магний). Некоторые элементы этой группы называют «органогенами» (O, H, С, N, P, S) в связи с их ведущей ролью в формировании структуры тканей и органов.
К ним относятся O, C, H, N, Ca, P, K, Na, S, Cl, Mg. В абсолютных значениях (из расчета на среднюю массу тела человека в 70 кг), величины содержания этих элементов колеблются в пределах от сорока с лиш ним кг (кислород) до нескольких г (магний). Некоторые элементы этой группы называют «органогенами» (O, H, С, N, P, S) в связи с их ведущей ролью в формировании структуры тканей и органов.
Вторую группу составляют «микроэлементы» (концентрация от 0,00001% до 0,01%). В эту группу входят: Fe, Zn, F, Sr, Mo, Cu, Br, Si, Cs, I, Mn, Al, Pb, Cd, B, Rb. Эти элементы содержатся в организме в концентрациях от сотен мг до нескольких г. Однако, несмотря на малое содержание, микроэлементы не случайные ингредиенты биосубстратов живого организма, а компоненты сложной физиологической системы, участвующей в регулировании жизненных функций организма на всех этапах его развития.
В третью группу включены «ультрамикроэлементы», концентрация которых ниже 0,000001%. Это Se, Co, V, Cr, As, Ni, Li, Ba, Ti, Ag, Sn, Be, Ga, Ge, Hg, Sc, Zr, Bi, Sb, U, Th, Rh. Содержание этих элементов в теле человека измеряется в мг и мкг. На данный момент установлено важнейшее значение для организма многих элементов из этой группы, таких как, селен, кобальт, хром и др.
Содержание этих элементов в теле человека измеряется в мг и мкг. На данный момент установлено важнейшее значение для организма многих элементов из этой группы, таких как, селен, кобальт, хром и др.
В основе другой классификации лежат представления о физиологической роли химических элементов в организме. Согласно такой классификации макроэлементы, составляющие основную массу клеток и тканей, являются “структурными” элементами. К «эссенциальным» (жизненно-необходимым) микроэлементам относят Fe, I, Cu, Zn, Co, Cr, Mo, Se, Mn, к “условно-эссенциальным” – As, B, Br, F, Li, Ni, Si, V. Жизненная необходимость или эссенциальность (от англ. essential – “необходимый”), является важнейшим для жизнедеятельности живых организмов свойством химических элементов. Химический элемент считается эссенциальным, если при его отсутствии или недостаточном поступлении в организм нарушается нормальная жизнедеятельность, прекращается развитие, становится невозможной репродукция. Восполнение недостающего количества такого элемента устраняет клинические проявления его дефицита и возвращает организму жизнеспособность.
К “токсичным” элементам отнесены Al, Cd, Pb, Hg, Be, Ba, Bi, Tl, к “потенциально-токсичным” – Ag, Au, In, Ge, Rb, Ti, Te, U, W, Sn, Zr и др. Результатом воздействия этих элементов на организм является развитие синдромов интоксикаций (токсикопатий).
Оценка элементного статуса человека является основным вопросом определения влияния на здоровье человека дефицита, избытка или нарушения тканевого перераспределения макро- и микроэлементов. Определение элементного состава биосред используется:
- при мониторинге состояния здоровья, оценке уровня работоспособности и эффективности лечения;
- при формировании групп риска по гипо- и гиперэлементозам;
- при подборе рациональной диеты как здоровому, так и больному человеку;
- в скрининг-диагностических исследованиях больших групп населения;
- при картировании территорий по нозологическим и системным формам патологии у детей и других возрастных групп населения;
- при оценке взаимозависимости многосторонних связей цепи “человек–среда обитания”;
- при составлении карт экологического природного и техногенного неблагополучия регионов;
- при изучении воздействия на организм вредных привычек;
- экспертно-криминалистических исследованиях (идентификация личности в судебной медицине, метод выбора в подтверждение исследований по молекуле ДНК и генному коду).

Методы определения микроэлементов в биосубстратах Масс-спектрометрия с индуктивно связанной аргоновой плазмой (ИСП-МС), атомно-абсорбционная спектрофотометрия с электротермической атомизацией (ААС-ЭТА).
Условия взятия и хранения материала для исследования
Взятие и подготовка крови для получения плазмы и сыворотки проводится по общепринятым методикам. Если при заборе проб используют перчатки, то они должны быть не опудренные и не содержать латекса (напр., нитриловые). Кровь может быть получена из локтевой вены или из пальцев рук (капиллярная). Объем отобранной крови должен составлять не менее 1 мл. Образцы сыворотки или плазмы крови хранятся в обычном холодильнике до 3–5 сут (от 0 до 4 °С) либо замораживаются (до -18 °С), либо лиофилизуются, или высушиваются в сушильном шкафу (для длительного хранения). Для длительного хранения образцы помещаются в одноразовые полипропиленовые пробирки с герметичными крышками.
Взятие биологических образцов крови и мочи проводят в соответствии с МУК 4.1.1482-08, МУК 4.1.1483-08.
Значение макро и микроэлементов в жизни растений
- Макроэлементы и их значение для растений
- Микроэлементы
- Питание для растений
В зеленых насаждениях обнаружены многие химические элементы. Макроэлементы содержатся в значительных концентрациях, микроэлементы – в тысячных долях процента.
Макроэлементы и их значение для растений
Макроэлементы представляют особую важность для роста и развития растений на всех стадиях жизненного цикла. К ним относят те, которые содержатся в культурах в значительных количествах — это азот, фосфор, калий, сера, магний и железо. При их дефиците представители флоры плохо развиваются, что сказывается на урожайности. Признаки нехватки многократно используемых макроэлементов проявляются прежде всего на старых листьях.
Азот
Главный ответственный за питание корней элемент. Он участвует в реакциях фотосинтеза, регулирует обмен веществ в клетках, а также способствует росту новых побегов. Этот элемент особенно необходим для растений на стадии вегетации. При нехватке азота рост насаждений замедляется или останавливается вовсе, цвет листьев и стеблей становится бледнее. Из-за переизбытка азота позднее развиваются соцветия и плоды. Насаждения, которых перекормили азотом имеют ботву темно-зеленого цвета, и излишне толстые стебли. Период вегетации удлиняется. Слишком сильное перенасыщение азотом приводит к гибели флоры в течение нескольких дней.
Фосфор
Участвует в большинстве протекающих в растениях процессах. Обеспечивает нормальное развитие и функционирование корневой системы, образование крупных соцветий, способствует вызреванию плодов.
Нехватка фосфора негативно сказывается на цветении и процессе созревания. Цветки получаются мелкими, плоды часто с дефектами. Литья могут окрашиваться в красновато-коричневый оттенок. Если же фосфор в избытке, замедляется обмен веществ в клетках, растения становятся чувствительными к нехватке воды, они хуже усваивают такие питательные элементы, как железо, цинк и калий. В результате листья желтеют, опадают, срок жизни растения сокращается.
Литья могут окрашиваться в красновато-коричневый оттенок. Если же фосфор в избытке, замедляется обмен веществ в клетках, растения становятся чувствительными к нехватке воды, они хуже усваивают такие питательные элементы, как железо, цинк и калий. В результате листья желтеют, опадают, срок жизни растения сокращается.
Калий
Процент калия в растениях больше по сравнению с кальцием и магнием. Этот элемент задействован в синтезировании крахмала, жиров, белков и сахарозы. Он защищает от обезвоживания, укрепляет ткани, предупреждает преждевременное увядания цветков, повышает сопротивляемость культур к различного рода патогенам.
Растения, обедненные калием, можно узнать по отмершим краям листьев, коричневым пятнам и куполообразной их форме. Это происходит вследствие нарушения процессов производства, накопления в зеленых частях насаждений продуктов распада, аминокислот и глюкозы. Если калий в избытке, наблюдается замедление всасывания растением азота. Это приводит к остановке роста, деформациям листьев, хлорозу, а на запущенных стадиях к отмиранию листьев. Поступление магния и кальция также затрудняется.
Это приводит к остановке роста, деформациям листьев, хлорозу, а на запущенных стадиях к отмиранию листьев. Поступление магния и кальция также затрудняется.
Магний
Участвует в реакциях с образованием хлорофилла. Является одним из его составных элементов. Способствует синтезу фитинов, содержащихся в семенах и пектинов. Магний активизирует работу энзимов, при участии которых происходит образование углеводов, протеинов, жиров, органических кислот. Он участвует в транспорте питательных веществ, способствует более скорому вызреванию плодов, улучшению их качественных и количественных характеристик, повышению качества семян.
Если растения испытывают дефицит магния, их листья желтеют, так как молекулы хлорофилла разрушаются. Если недостаток магния своевременно не восполнить, растение начнет отмирать. Избыток магния у растений наблюдаются редко. Однако, если доза внесенных препаратов магния слишком большая, замедляется всасываемость кальция и калия.
Сера
Является составным элементов протеинов, витаминов, аминокислот цистина и метионина. Участвует в процессах образования хлорофилла. Растения, которые испытывают серное голодание, нередко заболевают хлорозом. Болезнь поражает главным образом молодые листья. Избыток серы приводит к пожелтению краев листьев, их подворачиванию вовнутрь. Впоследствии края обретают коричневый оттенок и отмирают. В некоторых случаях возможно окрашивание листьев в сиреневый оттенок.
Железо
Является составным компонентом хлоропластов, участвует в производстве хлорофилла, обмене азота и серы, клеточном дыхании. Железо – необходимый компонент многих растительных ферментов. Этот тяжелый металл играет наиболее важную роль. Его содержание в растении достигает сотых долей процента. Неорганические соединения железа ускоряют биохимические реакции.
При дефиците этого элемента растения нередко заболевают хлорозом. Нарушаются дыхательные функции, ослабляются реакции фотосинтеза. Верхушечные листья постепенно бледнеют и усыхают.
Верхушечные листья постепенно бледнеют и усыхают.
Микроэлементы
Основными микроэлементами являются: железо, марганец, бор, натрий, цинк, медь, молибден, хлор, никель, кремний. Их роль в жизни растений нельзя недооценивать. Недостаток микроэлементов хоть и не приводит к гибели растений, но сказывается на скорости протекания различных процессов. Это влияет на качество бутонов, плодов и урожаях в целом.
Кальций
Регулирует усвоение белков и углеводов, влияет на продуцирование хлоропластов и усвоению азота. Он играет важную роль в построении сильных клеточных оболочек. Наибольшее содержание кальция наблюдается в зрелых частях растений. Старые листья состоят из кальция на 1 %. Кальций активирует работу многих энзимов, в том числе амилазы, фосфорилазы, дегидрогеназы и др. Он регулирует работу сигнальных систем растений, отвечая за нормальные реакции на воздействия гормонами и внешними раздражителями.
При нехватке этого химического элемента происходит ослизнение клеток растений. Особенно это проявляется на корнях. Нехватка кальцием приводит к нарушению транспортной функции мембран клеток, повреждению хромосом, нарушению цикла деления клеток. Перенасыщение кальцием провоцирует хлороз. На листьях появляются бледные пятна с признаками некроза. В некоторых случаях можно наблюдать круги, заполненные водой. Отдельные растения реагируют на переизбыток данного элемента ускоренным ростом, но появившиеся побеги быстро отмирают. Признаки отравления кальцием схожи с переизбытком железа и магния.
Особенно это проявляется на корнях. Нехватка кальцием приводит к нарушению транспортной функции мембран клеток, повреждению хромосом, нарушению цикла деления клеток. Перенасыщение кальцием провоцирует хлороз. На листьях появляются бледные пятна с признаками некроза. В некоторых случаях можно наблюдать круги, заполненные водой. Отдельные растения реагируют на переизбыток данного элемента ускоренным ростом, но появившиеся побеги быстро отмирают. Признаки отравления кальцием схожи с переизбытком железа и магния.
Марганец
Активизирует работу ферментов, участвует в синтезировании протеинов, углеводов, витаминов. Марганец также принимает участие в фотосинтезе, дыхании, углеводно-белковом обмене. Недостаток марганца приводит к высветлению окраски листьев, появлению отмерших участков. Растения заболеванию хлорозом, у них отмечается недоразвитие корневой системы. В серьезных случаях начинают засыхать и опадать листья, отмирать верхушки веток.
Цинк
Регулирует окислительно-восстановительные процессы.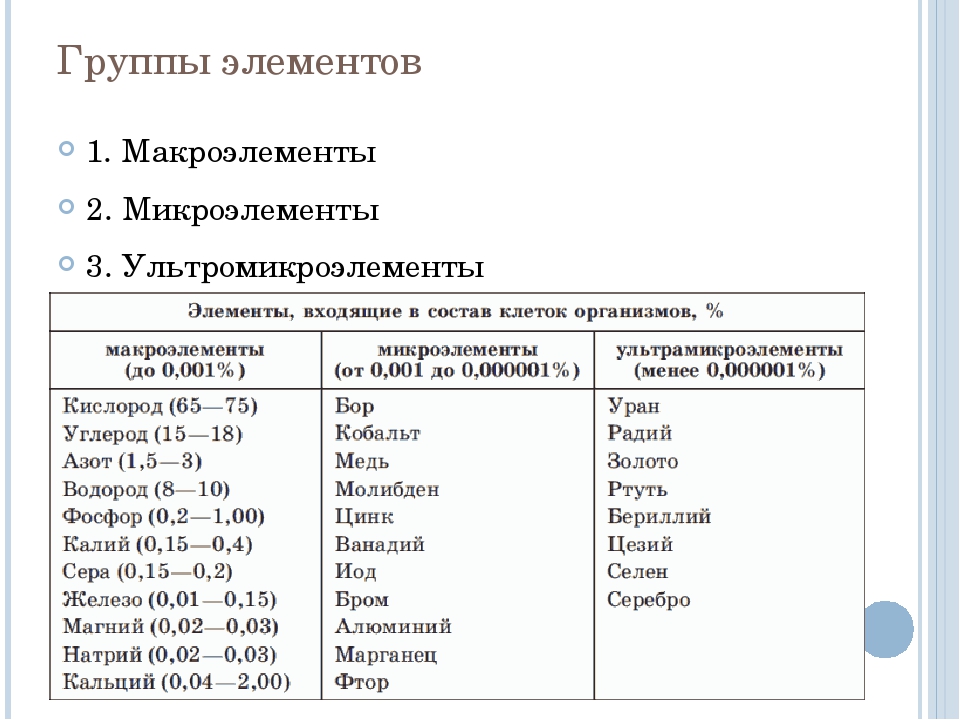 Является компонентом некоторых важных ферментов. Цинк повышает выработку сахарозы и крахмала, содержание в плодах углеводов и белков. Он участвует в реакции фотосинтеза и способствует выработке витаминов. При нехватке цинка растения хуже противостоят холоду и засухе, уменьшается содержание в них белка. Цинковое голодание также приводит к изменению окраски листьев (они желтеют или обретают белесый цвет), уменьшению образования почек, падению урожайности.
Является компонентом некоторых важных ферментов. Цинк повышает выработку сахарозы и крахмала, содержание в плодах углеводов и белков. Он участвует в реакции фотосинтеза и способствует выработке витаминов. При нехватке цинка растения хуже противостоят холоду и засухе, уменьшается содержание в них белка. Цинковое голодание также приводит к изменению окраски листьев (они желтеют или обретают белесый цвет), уменьшению образования почек, падению урожайности.
Молибден
На сегодняшний день именно этот микроэлемент называют одним из важнейших. Молибден регулирует азотный обмен, нейтрализует нитраты. Он также влияет на углеводородный и фосфорный обмен, производство витаминов и хлорофилла, а также на скорость протекания окислительно-восстановительных процессов. Молибден способствует обогащению растений витамином С, углеводами, каротином, белками.
Недостаточные концентрации молибдена негативно сказываются на обменных процессах, затормаживается редуцирование нитратов, образование белков и аминокислот. В связи с этим урожаи снижаются, их качество ухудшается.
В связи с этим урожаи снижаются, их качество ухудшается.
Медь
Является элементом медьсодержащих белков, энзимов, участвует в фотосинтезе, регулирует транспорт белков. Медь повышает содержание азота и фосфора в два раза, а также защищает хлорофилл от разрушения.
Дефицит меди приводит к скручиванию кончиков листьев и хлорозу. Снижается количество пыльцевых зерен, падает урожайность, у деревьев “повисает” крона.
Бор
Регулирует обмен протеинов и углеводов. Является важнейшим компонентом синтеза РНК и ДНК. Бор в союзе с марганцем являются катализаторами реакции фотосинтеза в растениях, которые испытали на себе заморозки. Бор требуется насаждениям на всех стадиях жизненного цикла.
От дефицита бора страдают больше всего молодые листья. Нехватка этого микроэлемента приводит к замедленному развитию пыльцы, внутреннему некрозу стеблей.
Избыток бора тоже нежелателен, так как приводит к ожогам нижних листьев.
Никель
Представляет собой составной компонент уреазы, с его участием протекают реакции разложения мочевины. В насаждениях, которые обеспечены никелем в достаточном количестве, содержание мочевины ниже. Также никель активирует некоторые ферменты, участвует в транспорте азота, стабилизирует структуру рибосом. При недостаточном поступлении никеля замедляется рост растений, снижается объем биомассы. А при перенасыщении никелем угнетаются реакции фотосинтеза, появляются признаки хлороза.
Хлор
Является основным элементов водно-солевого обмена растений. Участвует в поглощении кислорода корневой системой, реакциях фотосинтеза, энергетическом обмене. Хлор уменьшает последствия заболевания грибком, борется с излишним поглощением нитратов.
При недостатке хлора корни вырастают короткими, но при этом густо разветвленными, а листья увядают. Капуста, испытавшая дефицит хлора, получается неароматной.
При этом и переизбыток хлора вреден.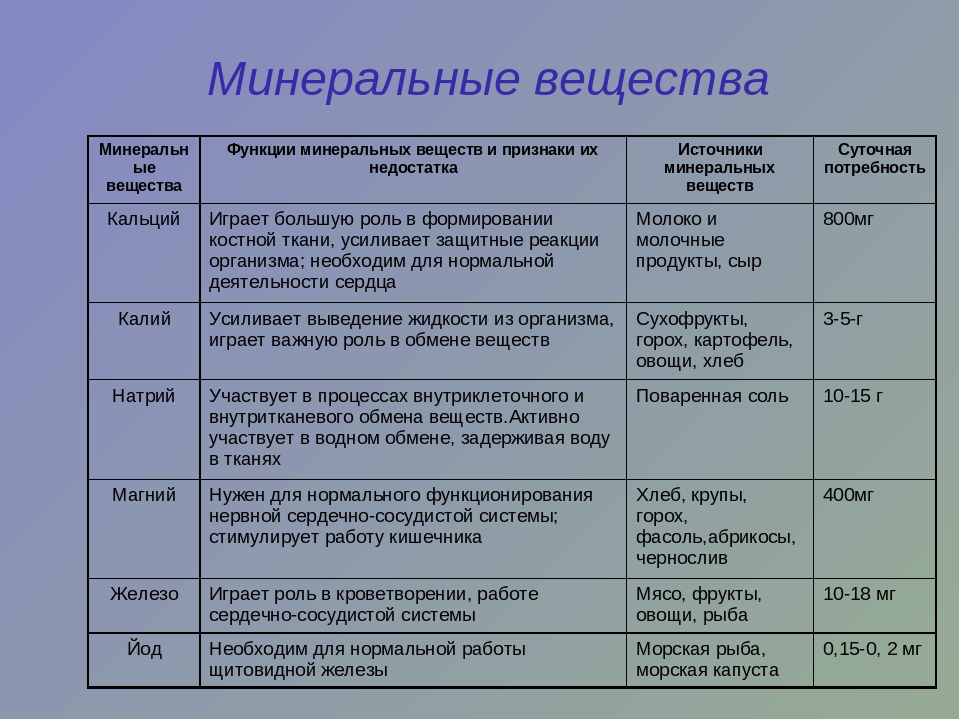 При нем листья становятся мельче и твердеют, на некоторых появляются пурпурные пятна. Стебель также грубеет. Чаще всего дефицит Cl проявляется наряду с недостатком N. Исправить ситуацию позволяет аммиачная селитра и каинит.
При нем листья становятся мельче и твердеют, на некоторых появляются пурпурные пятна. Стебель также грубеет. Чаще всего дефицит Cl проявляется наряду с недостатком N. Исправить ситуацию позволяет аммиачная селитра и каинит.
Кремний
Является своеобразным кирпичиком стенок клеток, а потому повышает выносливость насаждений перед заболеваниями, заморозками, загрязнениями, нехваткой воды. Микроэлемент влияет на обменные процессы с участие фосфора и азота, помогает снижать токсичность тяжелых металлов. Кремний стимулирует развитие корней, влияет на рост и развитие растений, способствует урожайности, повышает содержание сахара и витаминов в плодах. Визуально дефицит кремния не обнаружить, но его недостаток негативно скажется на сопротивляемости культур негативным факторам, развитости корневой системы, развитии цветов и плодов.
Питание для растений
Микро- и макроэлементы оказывают влияние друг на друга, в результате их биодоступность для флоры меняется.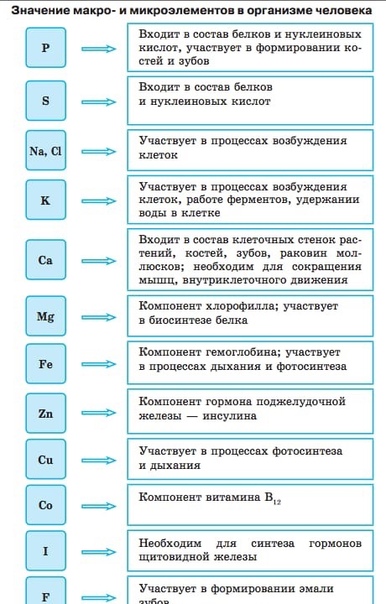 Переизбыток фосфора приводит к нехватке цинка и образованию фосфатов меди и железа – то есть недоступности этих металлов для растений. Переизбыток серы уменьшает усвояемость молибдена. Излишек марганца приводит к хлорозу, вызванного недостатком железа. Высокие концентрации меди приводят к нехватке железа. При дефиците B нарушается всасываемость кальция. И это только часть примеров!
Переизбыток фосфора приводит к нехватке цинка и образованию фосфатов меди и железа – то есть недоступности этих металлов для растений. Переизбыток серы уменьшает усвояемость молибдена. Излишек марганца приводит к хлорозу, вызванного недостатком железа. Высокие концентрации меди приводят к нехватке железа. При дефиците B нарушается всасываемость кальция. И это только часть примеров!
Вот почему так важно для восполнения дефицита макро- и микроэлементов, использовать сбалансированные комплексы удобрений. Для различных сред существуют свои составы. Нельзя применять удобрение для почвы в гидропонике, ведь изначальные условия будут неодинаковы.
Почва – своеобразный буфер. В ней питательные вещества могут находиться до тех пор, пока не понадобятся растению. Почва сама регулирует уровень pH, тогда как в гидропонных системах показатели полностью зависят от человека и тех препаратов, которыми он насыщает питательный раствор.
При традиционном выращивании нельзя точно знать, сколько тех или иных микроэлементов содержится в земле, тогда как в гидропонике показатели pH и ЕС питательного раствора можно определить без труда – с помощью рН-метра и ЕС-метра. Выращивание в гидропонике более эффективно. Вместе с тем любой сбой здесь имеет более серьезные последствия для насаждений. Вот почему нужно выбирать удобрения внимательно.
Выращивание в гидропонике более эффективно. Вместе с тем любой сбой здесь имеет более серьезные последствия для насаждений. Вот почему нужно выбирать удобрения внимательно.
Оптимальный комплекс макро- и микроэлементов, необходимых для питания растения, выращиваемого в земле, содержит комплект удобрений Bio-Grow + Bio-Bloom. Препарат ускоряет рост цветов и культур, увеличивает урожайность.
Для растений, выращиваемых методом гидропоники рекомендуем выбрать комплект удобрений Flora Duo Grow HW + Flora Duo Bloom производства Франция. Он имеет сбалансированный состав, который закрывает все потребности растений на протяжении всего жизненного цикла. Flora Duo Grow способствует ускоренному росту листьев и формированию сильных стеблей. Flora Duo Bloom содержит фосфор, который готовит насаждения к цветению и плодоношению.
5. Химический состав клетки. Биология. Общая биология. 10 класс. Базовый уровень
5. Химический состав клетки
Вспомните!
Что такое химический элемент?
Какие химические элементы преобладают в земной коре?
Что вам известно о роли таких химических элементов, как иод, кальций, железо, в жизнедеятельности организмов?
Одним из основных общих признаков живых организмов является единство их элементного химического состава. Независимо от того, к какому царству, типу или классу принадлежит то или иное живое существо, в состав его тела входят одни и те же так называемые универсальные химические элементы. Сходство в химическом составе разных клеток свидетельствует о единстве их происхождения.
Независимо от того, к какому царству, типу или классу принадлежит то или иное живое существо, в состав его тела входят одни и те же так называемые универсальные химические элементы. Сходство в химическом составе разных клеток свидетельствует о единстве их происхождения.
Рис. 8. Панцири одноклеточных диатомовых водорослей содержат большое количество кремния
В живой природе обнаружено около 90 химических элементов, т. е. большая часть всех известных на сегодняшний день. Никаких специальных элементов, характерных только для живых организмов, не существует, и это является одним из доказательств общности живой и неживой природы. Но количественное содержание тех или иных элементов в живых организмах и в окружающей их неживой среде существенно отличается. Например, кремния в почве около 33 %, а в наземных растениях лишь 0,15 %. Подобные различия указывают на способность живых организмов накапливать только те элементы, которые необходимы им для жизнедеятельности (рис. 8).
В зависимости от содержания все химические элементы, входящие в состав живой природы, разделяют на несколько групп.
Макроэлементы. I группа. Главными компонентами всех органических соединений, выполняющих биологические функции, являются кислород, углерод, водород и азот. Все углеводы и липиды содержат водород, углерод и кислород, а в состав белков и нуклеиновых кислот, кроме этих компонентов, входит азот. На долю этих четырёх элементов приходится 98 % от массы живых клеток.
II группа. К группе макроэлементов относятся также фосфор, сера, калий, магний, натрий, кальций, железо, хлор. Эти химические элементы являются обязательными компонентами всех живых организмов. Содержание каждого из них в клетке составляет от десятых до сотых долей процента от общей массы.
Натрий, калий и хлор обеспечивают возникновение и проведение электрических импульсов в нервной ткани. Поддержание нормального сердечного ритма зависит от концентрации в организме натрия, калия и кальция.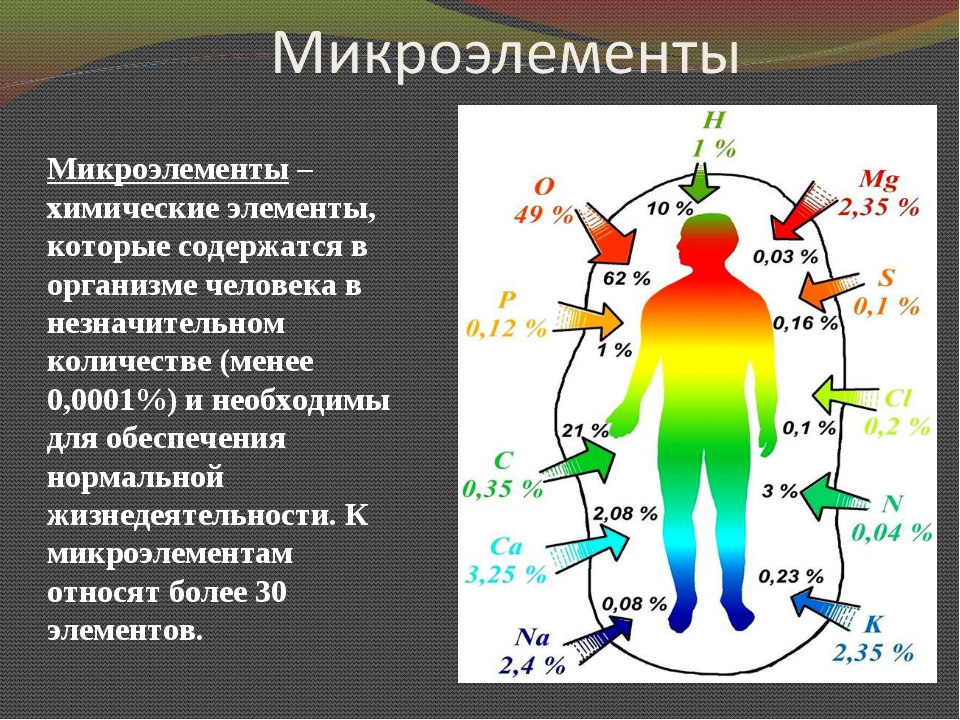 Железо участвует в биосинтезе хлорофилла, входит в состав гемоглобина (белка-переносчика кислорода в крови) и миоглобина (белка, содержащего запас кислорода в мышцах). Магний в клетках растений входит в состав хлорофилла, а в животном организме участвует в формировании ферментов, необходимых для нормального функционирования мышечной, нервной и костной тканей. В состав белков часто входит сера, а все нуклеиновые кислоты содержат фосфор. Фосфор также является компонентом всех мембранных структур.
Железо участвует в биосинтезе хлорофилла, входит в состав гемоглобина (белка-переносчика кислорода в крови) и миоглобина (белка, содержащего запас кислорода в мышцах). Магний в клетках растений входит в состав хлорофилла, а в животном организме участвует в формировании ферментов, необходимых для нормального функционирования мышечной, нервной и костной тканей. В состав белков часто входит сера, а все нуклеиновые кислоты содержат фосфор. Фосфор также является компонентом всех мембранных структур.
Среди обеих групп макроэлементов кислород, углерод, водород, азот, фосфор и сера объединяются в группу биоэлементов, или органогенов, на основании того, что они составляют основу большинства органических молекул (табл. 1).
Микроэлементы. Существует большая группа химических элементов, которые содержатся в организмах в очень низких концентрациях. Это алюминий, медь, марганец, цинк, молибден, кобальт, никель, иод, селен, бром, фтор, бор и многие другие. На долю каждого из них приходится не более тысячных долей процента, а общий вклад этих элементов в массу клетки – около 0,02 %. В растения и микроорганизмы микроэлементы поступают из почвы и воды, а в организм животных – с пищей, водой и воздухом. Роль и функции элементов этой группы в различных организмах весьма разнообразны. Как правило, микроэлементы входят в состав биологически активных соединений (ферментов, витаминов и гормонов), и их действие проявляется главным образом в том, как они влияют на обмен веществ.
На долю каждого из них приходится не более тысячных долей процента, а общий вклад этих элементов в массу клетки – около 0,02 %. В растения и микроорганизмы микроэлементы поступают из почвы и воды, а в организм животных – с пищей, водой и воздухом. Роль и функции элементов этой группы в различных организмах весьма разнообразны. Как правило, микроэлементы входят в состав биологически активных соединений (ферментов, витаминов и гормонов), и их действие проявляется главным образом в том, как они влияют на обмен веществ.
Таблица 1. Содержание биоэлементов в клетке
Кобальт входит в состав витамина В12 и принимает участие в синтезе гемоглобина, его недостаток приводит к анемии. Молибден в составе ферментов участвует в фиксации азота у бактерий и обеспечивает работу устьичного аппарата у растений. Медь является компонентом фермента, участвующего в синтезе меланина (пигмента кожи), влияет на рост и размножение растений, на процессы кроветворения у животных организмов. Иод у всех позвоночных животных входит в состав гормона щитовидной железы – тироксина. Бор влияет на ростовые процессы у растений, его недостаток приводит к отмиранию верхушечных почек, цветков и завязей. Цинк действует на рост животных и растений, а также входит в состав гормона поджелудочной железы – инсулина. Нехватка селена приводит к возникновению у человека и животных раковых заболеваний. Каждый элемент играет свою определённую, очень важную роль в обеспечении жизнедеятельности организма.
Иод у всех позвоночных животных входит в состав гормона щитовидной железы – тироксина. Бор влияет на ростовые процессы у растений, его недостаток приводит к отмиранию верхушечных почек, цветков и завязей. Цинк действует на рост животных и растений, а также входит в состав гормона поджелудочной железы – инсулина. Нехватка селена приводит к возникновению у человека и животных раковых заболеваний. Каждый элемент играет свою определённую, очень важную роль в обеспечении жизнедеятельности организма.
Как правило, биологический эффект того или иного микроэлемента зависит от присутствия в организме других элементов, т. е. каждый живой организм – это уникальная сбалансированная система, нормальная работа которой зависит, в том числе, и от правильного соотношения её компонентов на любом уровне организации. Так, например, марганец улучшает усвоение организмом меди, а фтор влияет на метаболизм стронция.
Обнаружено, что некоторые организмы интенсивно накапливают определённые элементы. Например, многие морские водоросли накапливают иод, хвощи – кремний, лютики – литий, а моллюски отличаются повышенным содержанием меди.
Например, многие морские водоросли накапливают иод, хвощи – кремний, лютики – литий, а моллюски отличаются повышенным содержанием меди.
Микроэлементы широко используют в современном сельском хозяйстве в виде микроудобрений для повышения урожайности культур и в качестве добавок к кормам для увеличения продуктивности животных. Применяют микроэлементы и в медицине.
Ультрамикроэлементы. Существует группа химических элементов, которые содержатся в организмах в следовых, т. е. ничтожно малых, концентрациях. К ним относят золото, бериллий, серебро и другие элементы. Физиологическая роль этих компонентов в живых организмах пока окончательно не установлена.
Роль внешних факторов в формировании химического состава живой природы. Содержание тех или иных элементов в организме определяется не только особенностями данного организма, но также составом среды, в которой он обитает, и той пищей, которую он использует. Геологическая история нашей планеты, особенности почвообразовательных процессов привели к тому, что на поверхности Земли сформировались области, которые отличаются друг от друга по содержанию химических элементов. Резкий недостаток или, наоборот, избыток какого-либо химического элемента вызывает в пределах таких зон возникновение биогеохимических эндемий – заболеваний растений, животных и человека.
Геологическая история нашей планеты, особенности почвообразовательных процессов привели к тому, что на поверхности Земли сформировались области, которые отличаются друг от друга по содержанию химических элементов. Резкий недостаток или, наоборот, избыток какого-либо химического элемента вызывает в пределах таких зон возникновение биогеохимических эндемий – заболеваний растений, животных и человека.
Во многих районах нашей страны – на Урале и Алтае, в Приморье и в Ростовской области количество иода в почве и в воде значительно снижено.
Если человек не получает с пищей нужного количества иода, у него снижается синтез тироксина. Щитовидная железа, пытаясь компенсировать нехватку гормона, разрастается, что приводит к образованию так называемого эндемического зоба. Особенно тяжёлые последствия от недостатка иода возникают у детей. Сниженное количество тироксина приводит к резкому отставанию в умственном и физическом развитии.
Чтобы предотвратить заболевания щитовидной железы, врачи рекомендуют подсаливать пищу специальной солью, обогащённой иодидом калия, употреблять рыбные блюда и морскую капусту.
Почти 2 тыс. лет назад правитель одной из северо-восточных провинций Китая издал указ, в котором обязал всех своих подданных съедать по 2 кг морской капусты в год. С тех пор жители послушно соблюдают древний указ, и, несмотря на то, что в этом районе существует явный недостаток иода, население не страдает заболеваниями щитовидной железы.
Вопросы для повторения и задания
1. В чём заключается сходство биологических систем и объектов неживой природы?
2. Перечислите биоэлементы и объясните, каково их значение в образовании живой материи.
3. Что такое микроэлементы? Приведите примеры и охарактеризуйте биологическое значение этих элементов.
4. Как отразится на жизнедеятельности клетки и организма недостаток какого-либо микроэлемента? Приведите примеры таких явлений.
5. Расскажите об ультрамикроэлементах. Каково их содержание в организме? Что известно об их роли в живых организмах?
6. Приведите примеры известных вам биохимических эндемий. Объясните причины их происхождения.
Приведите примеры известных вам биохимических эндемий. Объясните причины их происхождения.
7. Составьте схему, иллюстрирующую элементный химический состав живых организмов.
Подумайте! Выполните!
1. По какому принципу все химические элементы, входящие в состав живой природы, разделяют на макроэлементы, микроэлементы и ультрамикроэлементы? Предложите свою, альтернативную, классификацию химических элементов, основанную на другом принципе.
2. Иногда в учебниках и пособиях вместо словосочетания «элементный химический состав» можно встретить выражение «элементарный химический состав». Объясните, в чём некорректность такой формулировки.
3. Выясните, существуют ли какие-либо особенности химического состава воды в местности, где вы живёте (например, избыток железа или нехватка фтора и т. д.). Используя дополнительную литературу и ресурсы Интернета, определите, какое влияние это может оказать на организм человека.
Работа с компьютером
Обратитесь к электронному приложению. Изучите материал и выполните задания.
Повторите и вспомните!
Растения
Удобрения. Азот необходим растениям для нормального формирования вегетативных органов. При дополнительном внесении в почву азотных и азотистых удобрений усиливается рост наземных побегов. Фосфор влияет на развитие и созревание плодов. Калий способствует оттоку органических веществ от листьев к корням, влияет на подготовку растения к зиме.
Все элементы в составе минеральных солей растения получают из почвы. Для того чтобы были высокие урожаи, необходимо поддерживать плодородие почвы, вносить удобрения. В современном сельском хозяйстве используют органические и минеральные удобрения, благодаря которым культурные растения получают необходимые элементы питания.
Органические удобрения (навоз, торф, перегной, птичий помёт и др.) содержат все необходимые растению питательные вещества. При внесении органических удобрений в почву попадают микроорганизмы, которые минерализуют органические остатки и тем самым повышают плодородие почвы. Навоз необходимо вносить задолго до посева семян, при осенней обработке почвы.
При внесении органических удобрений в почву попадают микроорганизмы, которые минерализуют органические остатки и тем самым повышают плодородие почвы. Навоз необходимо вносить задолго до посева семян, при осенней обработке почвы.
Минеральные удобрения обычно содержат те элементы, которых не хватает в почве: азот (натриевая и калиевая селитры, хлористый аммоний, мочевина и др.), калий (хлористый калий, сульфат калия), фосфор (суперфосфаты, фосфоритная мука и пр.). Удобрения, содержащие азот, обычно вносят весной или в начале лета, так как они быстро вымываются из почвы. Калийные и фосфорные удобрения сохраняются дольше, поэтому их вносят осенью. Излишек удобрений столь же вреден для растений, как и их недостаток.
Данный текст является ознакомительным фрагментом.
Продолжение на ЛитРеснормы физиологических потребностей организма в минеральных веществах
Способы применения микроудобрений и удобрений, содержащих микроэлементы
Микроудобрения применяют для внесения в почву, некорневых подкормок и предпосадочной обработки семян. Дозы микроудобрений малы. Это требует высокой точности дозирования и равномерности внесения.
Дозы микроудобрений малы. Это требует высокой точности дозирования и равномерности внесения.
Внесение в почву
- образование трудно растворимых форм микроэлементов,
- вымывание микроэлементов за пределы корнеобитаемого слоя.
Не рекомендуется вносить в почву дорогостоящие виды микроудобрений, особенно осенью. В данном случае лучше использовать различные макроудобрения, модифицированные микроэлементами, труднодоступные промышленные отходы и удобрения пролонгированного действия.
Итак, краткая сводка
Железо
Самое главное, зачем нам нужно железо – оно образует гемоглобин — переносчик кислорода ко всем тканям. Железо может откладываться «про запас» в печени и почках – это его депо.
Однако, если с пищей его поступает мало, депо пустеет, и развиваются симптомы недостатка: анемия (особенно у вегетарианцев часто бывает), бледность и сухость кожи, слабость, плохое зрение, плохое пищеварение, онемение пальцев.
Избыток: если железа накапливается слишком много, возникают запоры, сахарный диабет, артрит и даже цирроз печени.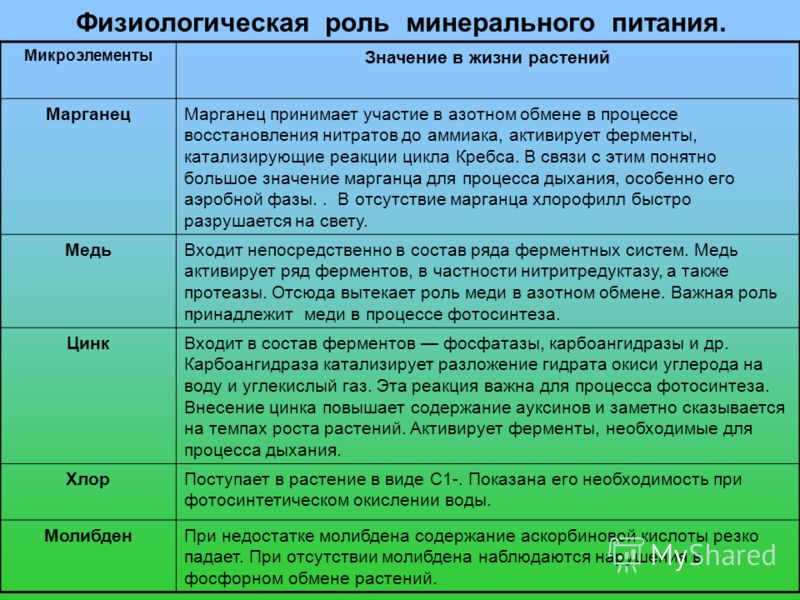
Медь
Медь необходима для усвоения железа, тоже участвует в кроветворении, образует многие ферменты, например, коллаген (отвечает за эластичность кожи), меланин (отвечает за окраску). Плюс у меди хорошо развиты бактерицидные свойства.
Как проявляется недостаток: низкий гемоглобин, анемия, пищеварительные расстройства, хрупкие кости, частые инфекции, выпадение волос, ранняя седина, блёклый цвет глаз, очень заметные, вздутые вены. Но недостаток бывает редко, потому что меди обычно достаточно в воде.
Избыток довольно токсичен, у воды появляется явный металлический привкус, организм реагирует поносом, тошнотой, рвотой, в некоторых случаях даже эпилепсией и болезнями сердца.
Йод
Главный помощник щитовидной железы — контролирует её нормальную работу, отвечает за производство гормонов, которые регулируют обмен веществ, рост и развитие детей, нормальное усвоение пищи, необходим для крепких ногтей. Поэтому самый простой способ постоянно поддерживать щитовидку – покупать йодированную соль.
Если вспомнить основы ОБЖ, йод принимают при угрозе радиоактивного излучения, чтобы избежать лучевой болезни.
Признаки недостатка: плохая память, постоянный голод, лишний вес, дети отстают в росте и умственном развитии, у женщин не получается забеременеть или выносить ребёнка. Развивается эндемический зоб – щитовидная железа увеличивается.
Избыток йода подавляет синтез гормонов, развивается гипотиреоз.
Цинк
Образует многие ферменты, но особенно важен для правильного полового развития мальчиков, обеспечивает нормальную работу центральной нервной системы.
При дефиците цинка мальчики отстают в росте и развитии (особенно половом), у мужчин снижается качество и объем спермы. У женщин недостаток может проявиться осложненными родами, болезнями ЦНС. Люди быстро устают, часто болеют, склонны к аллергии.
При избытке развиваются гастриты, тошнота, рвота, частые инфекции, сухой кашель, постоянная жажда и приторно-сладкий привкус во рту.
Кобальт
Он участвует в кроветворении, синтезе инсулина и витамина В12. И помогает усваиваться кальцию и фосфору.
И помогает усваиваться кальцию и фосфору.
Поэтому при недостатке развивается анемия, люди быстро устают, повышается возбудимость.
Избытка практически не бывает.
Марганец
Он участвует в синтезе интерферона и гликопротеина, поддерживает уровень сахара в крови, помогает усваиваться витаминам С, Е и группы В, входит в состав ферментов-антиоксидантов, поддерживает сосуды и клетки головного мозга, повышает потенцию.
Недостатка марганца практически не бывает, как и избытка. Крайне редко из-за его дефицита могут размягчаться кости и суставы, повышается раздражительность.
Хром
Тоже участвует в производстве инсулина, регулирует уровень сахара и холестерина в крови, защищает сердце и сосуды, потому что поддерживает в норме обмен жиров и углеводов.
Дефицит хрома отражается на красоте волос, ногтей, зубов, костной системы, могут быть скачки сахара, быстрое образование бляшек на стенках сосудов.
Избытка не бывает, потому что хром медленно усваивается и быстро выводится.
Селен
Селен входит в состав антиоксидантных ферментов и даже в сперму
Нейтрализует и выводит соли тяжелых металлов, для курильщиков это очень важно. Помогает усваиваться витамину Е, защищает его от разрушения
При недостатке слабеет иммунитет, выпадают волосы, кожа становится суше, снижается качество спермы.
Избытка практически не бывает, только если злоупотреблять минеральными добавками.
О том, в каких продуктах питания какой микроэлемент содержится, подробно покажет таблица.
Цинк
Это полезное вещество регулирует большое количество процессов в организме:
- Метаболизм.
- Работа репродуктивной системы.
- Формирование кровяных клеток.
Цинк можно найти в кунжуте или зародышах пшеницы.
Вы когда-нибудь замечали белые пятна на ногтях? Это все из-за недостатка цинка в организме. Помимо этого, возможно быстрое утомление, инфекционные патологии и развитие аллергии различного характера.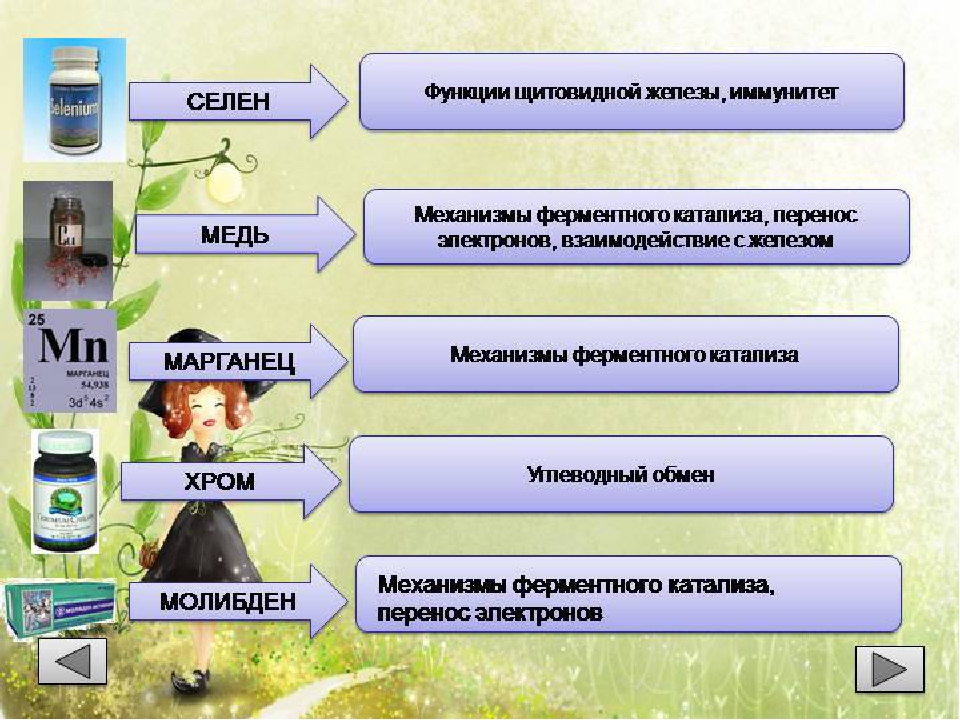
Подводя итог, отметим, что микроэлементы занимают важное место в организме человека и способствуют нормальной работе большинства жизненно важных систем организма. https://www.youtube.com/embed/ZM223bqedbc
Смотрели:
44
Последствия дефицита и передозировки
Если микроэлементы не будут постоянно поступать в ткани, это отрицательно скажется на работе внутренних органов. Пониженный уровень микровеществ может быть вызван сильной потерей крови, ограниченным питанием в результате жестких диет, плохой экологии. Дефицит жизненно важных веществ приводит к патологиям и серьезным проблемам с самочувствием.
Патологии, возникающие при недостатке микроэлементов
| Название | Химический знак | Признаки недостаточности |
| Марганец | Mn | нарушение костеобразования, стерильность |
| Цинк | Zn | выпадение волос и нарушение их роста |
| Медь | Cu | неправильный обмен веществ, талассемия |
| Кобальт | Co | снижение веса, анемия |
| Йод | I | эндемический зоб |
Микроэлементозы – заболевания, указывающие на дефицит элементов. Своевременная реакция на сигналы организма помогает избавиться от дальнейших проблем. Поэтому внимательно присматривайтесь даже к незначительным изменениям.
Своевременная реакция на сигналы организма помогает избавиться от дальнейших проблем. Поэтому внимательно присматривайтесь даже к незначительным изменениям.
Видео
Среди симптомов дефицита микроэлементов зачастую:
- медленный рост волос;
- слабость в мышцах;
- ломкость и слоение ногтевой пластины;
- разрушение зубной эмали;
- ухудшение памяти;
- сбои работы ЖКТ;
- изменения сердечного ритма.
О наличии дефицита также свидетельствует неконтролируемая агрессия, злость, депрессия, усталость и сонливость. Чтобы понять, каких микроэлементов не хватает, нужно сдать анализы и пройти лабораторные обследования. Специалисты по состоянию волос, ногтей и крови пациента могут определить гинекологические, сердечно-сосудистые, терапевтические и урологические проблемы.
Специалисты по состоянию волос, ногтей и крови пациента могут определить гинекологические, сердечно-сосудистые, терапевтические и урологические проблемы.
По внешнему виду и работе органов можно самостоятельно определить, какого микроэлемента не хватает в организме. При избыточном весе следует увеличить количество марганца и хрома. При проблемах с пищеварением увеличьте дозу хрома. Цинк также необходим для профилактики дисбактериоза, пищевой аллергии, дисфункции предстательной железы. О дефиците кремния и селена свидетельствуют ломкие ногти. Как мы выяснили, микроэлементы необходимые человеку для нормальной жизнедеятельности и правильного функционирования внутренних органов. Их невозможно заменить или выработать в организме, поэтому только от человека зависит поддержание оптимальных процессов метаболизма, развитие и рост ребенка, иммунитет. Чтобы помочь синтезу микроэлементов, следует правильно питаться и контролировать количество ежедневного поступления веществ.
Взаимосвязь строения и функций неорганических и органических веществ
Выполняемые неорганическими и органическими веществами функции тесно связаны с их строением. Так, покрывающая клетку мембрана (оболочка) содержит в своем составе углеводы, белки и липиды. Находящиеся на поверхности клеточной оболочки белки-рецепторы воспринимают сигналы из окружающего пространства, выполняя тем самым рецепторную функцию.
Так, покрывающая клетку мембрана (оболочка) содержит в своем составе углеводы, белки и липиды. Находящиеся на поверхности клеточной оболочки белки-рецепторы воспринимают сигналы из окружающего пространства, выполняя тем самым рецепторную функцию.
Содержание липидов (жиров) внутри мембран определяет проницаемость оболочки для одних соединений и непроницаемость для других. Углеводы ответственны за синтез молекул АТФ, запасающих энергию. Аналогично связано строение других компонентов клетки с их составом.
Польза для человека
Микроэлементы в организме человека отвечают за правильные обменные процессы, синтезирование гормонов, ферментов и полезных витаминов. Если соблюдать норму каждого вещества в организме, укрепляемся иммунитет, улучшается образование крови, кислородный обмен в тканях и развитие костной ткани. Работоспособность половой системы также зависит от кислотно-щелочного баланса, который обеспечивают микровещества.
Видео
МАКРО и МИКРОЭЛЕМЕНТЫ.» src=»https://www.youtube.com/embed/uDXq7dsPKbU?feature=oembed&wmode=opaque» frameborder=»0″ allow=»accelerometer; autoplay; clipboard-write; encrypted-media; gyroscope; picture-in-picture» allowfullscreen=»»/>
После тщательного анализа строения клеток, ученые пришли к выводу, что жидкость, наполняющая их, по формуле схожа с морской водой, которая была в доисторическую эпоху. Состав достигается за счет оптимальной комбинации важных веществ. Если для жизнедеятельности не хватает одного из компонентов, он начинает высасывать их из собственных тканей с накопившимися нутриентами
Функции элементов и их важность для жизнедеятельности человека, указаны в таблице, приведенной ниже
Содержание микроэлементов в продуктах питания
| Название | Источники | Польза для человека | Последствия недостатка | Суточная норма |
| Медь | орехи, морепродукты | формирование красных кровяных частиц, сохранение упругости кожных покровов, усвоение железа | психические нарушения, пигментация дермы, анемия, патологическая низкая температура | детям до 2 мг, взрослым 3 мг, беременным и кормящим 4 – 5 мг |
| Железо | персики, черника, абрикосы, бобы, злаковые | поддержание здоровья нервной системы, улучшение кровообращения | малокровие | от 10 до 30 мг |
| Цинк | бананы, орехи, гречка, теквенные семена, злаки, бобы | производство инсулина, укрепление иммунитета участие в синтезе гормонов | пониженный иммунитет, потеря волос, депрессия | 10 – 25 мг |
| Марганец | бобы, злаки, орехи | обмен жирных кислот, регуляция уровня холестерина | повышенных холестерин, атеросклероз | 5 – 10 мг |
| Кобальт | земляника, клубника, свекла, бобовые | активация производства инсулина, формирование белков | нарушения обмена веществ | 40 – 70 мкг |
| Йод | морская капуста | поддержка функционирования нервных клеток и щитовидной железы, защита от микробов | медленное умственное детское развитие, зоб | 2 – 4 мкг/кг веса |
| Фтор | вода, вегетарианская пища | укрепление ногтей, зубов, костей, поддержка здоровья эмали | заболевания зубов и десен | 0,5 – 4 мг |
| Селен | виноград, грибы, морепродукты | предотвращение развития раковых клеток, антиоксидант, укрепление иммунитета, задержка старения | частые инфекционные болезни, ослабление иммунной системы, аритмия, одышка | 5 – 10 мг |
| Хром | цельные зерна, грибы | способствует переработке углеводов, производство инсулина | увеличение уровня сахара в крови, диабет, нарушение усвоения глюкозы | 100 – 200 мкг |
| Бром | водоросли, злаковые, бобовые, орехи, морская рыба | снятие судорог, укрепление при сердечно-сосудистых заболеваниях, укрепление ЖКТ, успокоение нервной системы | снижение уровня гемоглобина, замедление роста у детей, выкидыш на первом этапе беременности, бессонница | 0,5 – 2 мг |
| Молибден | крыжовник, черная смородина, шпинат, любой сорт капусты | расщепление липидов, активация обмена веществ | нарушение метаболизма, проблемы в работе пищеварительной системы | до 10 лет 20 – 150 мкг, взрослым 75 – 300 мкг |
Отказ от одного из видов продуктов приводит к изменению функциональности организма, поэтому важно придерживаться принципов правильного питания и тщательно продумывать свое меню. Уже через неделю изменения пищевых привычек вы увидите положительные изменения: ногти и волосы станут крепче, улучшится обмен веществ и работа внутренних органов
Уже через неделю изменения пищевых привычек вы увидите положительные изменения: ногти и волосы станут крепче, улучшится обмен веществ и работа внутренних органов
Микроэлементы самостоятельно концентрируются в разных органах. Кадмий сосредоточен в почках, а цинк в поджелудочной железе. Избирательная концентрация способствует нормальному функционированию и росту организма.
Какие бывают микроэлементы, и что происходит, если их не принимать?
Важнейшими микроэлементами, влияющими на процессы жизнедеятельности, являются эссенциальные нутриенты (незаменимые факторы питания). К микроэлементам относятся:
- железо;
- цинк;
- селен;
- хром;
- ванадий;
- молибден;
- йод;
- марганец;
- кобальт;
- хром.
Содержание некоторых из них настолько мало, что может быть измерено лишь специальными средствами для анализа. Но при полном отсутствии или недостаточном поступлении микроэлементов в организм прекращается рост, начинаются процессы деградации: нарушаются процессы обмена веществ, алгоритмы деления клеток, передачи наследственной информации. Комплекс заболеваний, вызванных недостатком микроэлементов, называется микроэлементозами.
Комплекс заболеваний, вызванных недостатком микроэлементов, называется микроэлементозами.
Причины микроэлементоза могут быть различны. Так, постоянный приток радиоактивных изотопов и фоновое излучение всегда закачиваются дисбалансом микроэлементов в теле человека. К числу вторичных факторов появления данного недуга следует отнести скудную пищу, отсутствие свежего воздуха, естественного освещения, некачественную питьевую воду, малоподвижный образ жизни.
Весомым фактором, приводящим к потере микроэлементов, считается регулярное употребление алкоголя, курение, употребление наркотических веществ. Чаще всего нездоровый образ жизни провоцирует дефицит кальция, цинка, селена, йода, магния. Чтобы восполнить нехватку этих веществ, организм действует по алгоритму, который биологи назвали механизмом замещения.
Полный список и основные характеристики свойств
Полный список и основные характеристики свойств макроэлементов представлен в таблице ниже.
Название макронутриента | Буквенное обозначение (латиница) | Свойства и характеристики |
|---|---|---|
Калий | K | Твердое вещество. |
Кальций | Ca | Твердое вещество. Легко вступает в химические реакции, поэтому найти его в природе в чистом виде без примесей невозможно. Является одним из наиболее распространенных химических элементов и обнаруживается в земной коре. В организме человека на долю вещества приходится около двух процентов от общего числа минералов. |
Магний | Mg | Твердое вещество. Металл, легко поддающийся нагреванию. В естественном виде кусочки вещества имеют серебристый оттенок. В природе находится преимущественно в виде солей. В человеческий организм поступает в растворах. |
Кислород | O | Газ. Не имеет цвета и запаха. Легко воспламеняется и отдает энергию. Является составной частью воды – основного источника жизни человека, животных и растений. |
Углерод | C | Вещество не стойкое и в природе существует в нескольких формах. Ученые выделяют углерод аморфный и кристаллический. Наиболее известные вещества, в составе которых находится углерод, – это алмаз и графит. В соединении с кислородом образует углекислый газ – продукт, образующийся в процессе жизнедеятельности клеток теплокровных организмов. Круговорот веществ в природе устроен так, что растения «забирают» и утилизируют углерод. |
Водород | H | Газ. Как и кислород, не имеет запаха. Вещество прозрачное. Присутствует в воде и воздухе, кроме того, ученые определили то, что именно водород является основным материалом во Вселенной. |
Азот | N | Газообразное вещество, но только при нормальных условиях. Азот является составной частью аммиака, а в жидком состоянии имеет способности замораживать клетки. |
Натрий | Na | Твердое вещество. Данное вещество очень активно, поэтому легко вступает в реакции. Наиболее известный всем источник натрия – каменная соль. В природе также встречается в составе полевых шпатов. |
Сера | S | Порошкообразное вещество. Минерал имеет неприятный запах, но последний выделяется только при проведении реакций. По внешнему виду сера напоминает пчелиный воск. Макроэлемент поступает в организм в виде солей и их производных – кислот. |
Фосфор | P | Твердое вещество. Широко распространено в природе, так как минерал проявляет высокую химическую активность и легко соединяется с прочими веществами. В организм человека поступает в ионной форме. |
Хлор | Cl | Газ. При нормальных условиях вещество ядовито, так как действует паралитически на клетки живых организмов. |
Многие характеристики макроэлементов по сей день остаются неизученными. Новые данные исследователи получают каждый день, благодаря чему удается выяснить работу веществ в клетках живых организмов более детально.
Роль калия в организме и суточная потребность в этом макроэлементе
Суточная потребность в калии составляет 2-4 г. Для чего нужен этот макроэлемент в организме? Калий регулирует водно-солевой и внутриклеточный обмен, кислотно-шелочное равновесие, нормализует работу сердца. Также этот макроэлемент для человека необходим потому, что он участвует в передаче нервных импульсов мышцам.
Уменьшение содержания калия в организме происходит при применении мочегонных препаратов, при частых рвотах, поносах, при гиперфункции коры надпочечников, обильном потоотделении.
При избытке калия в организме наблюдаются физическое и умственное возбуждение, парестезия конечностей, бледность кожи, повышение выведения натрия с мочой, изменения на электрокардиограмме.
Содержание калия в мг на 100 г съедобной части продуктов:
- Очень большое (более 500): урюк, фасоль, морская капуста, чернослив, изюм, горох, картофель.
- Большое (251-400): говядина, свинина, треска, хек, скумбрия, кальмары (филе), крупа овсяная, зеленый горошек, помидоры, свекла, редис, лук зеленый, черешня, смородина черная и красная, виноград, абрикосы, персики.
- Умеренное (150-250): мясо куры, свинина жирная, судак, пшено, крупа гречневая, хлеб из муки 2-го сорта, морковь, капуста, кабачки, тыква, клубника, груши, сливы, апельсины.
- Малое (менее 150): молоко, творог, сметана, сыр, рис, огурцы, арбуз, брусника, клюква.
Роль микроэлементов
Несмотря на тот факт, что микроэлементы содержатся в клетках человека в незначительном количестве, их роль не менее важна.
Видео
com/embed/LO5AGAE3Ed8?feature=oembed&wmode=opaque» frameborder=»0″ allow=»accelerometer; autoplay; clipboard-write; encrypted-media; gyroscope; picture-in-picture» allowfullscreen=»»/>
Представляются следующие факторы:
- Йод – основа для нормального функционирования щитовидной железы. При его дефиците у человека развиваются проблемы в сфере нервной системы, а также формируется гипотиреоз – заболевание, влекущее гормональный сбой, набор лишнего веса и прочие патологии.
- Кремний – также участвует в формировании костной и мышечной ткани, является одним из механизмов кроветворения. Если употреблять в пищу недостаточное количество продуктов, содержащих кремний, можно столкнуться с повышенной ломкостью костей, развитием заболеваний кишечника и желудка.
- Цинк – помогает в заживлении ран, поэтому его используют в производстве большинства мазей соответствующего назначения.
- Фтор – участвует в формировании зубной эмали, а также костной ткани.
 Если не хватает в организме фтора, человек сталкивается с элементарным развитием кариеса зубов.
Если не хватает в организме фтора, человек сталкивается с элементарным развитием кариеса зубов. - Селен – здесь выделяют участие в укреплении иммунной системы, а также в слаженной работе щитовидной железы. Этот микроэлемент при своем недостатке может повлечь развитие анемии.
- Медь – в организме за счет меди происходит перемещение электронов, что запускает процесс ферментного катализа. Если в клетках человека не хватает представленного микроэлемента, развивается анемия.
- Хром – это основной элемент в обмене углеводов, в результате дефицита которого происходят нарушения уровня сахара в крови человека. Зачастую именно нехватка хрома становится причиной развития у людей сахарного диабета.
- Молибден – этот ультрамикроэлемент помогает в переносе электронов. Его отсутствие способствует развитию кариеса на зубной эмали, а также провоцирует нарушения в работе нервной системы.
- Магний – необходим в ферментном катализе.
Говоря об ультрамикроэлементах, можно выделить дополнительные:
- рубидий – в клетках человека может стать отличным заменителем калия.
 В результате этот элемент препятствует развитию аллергии, воспалению и прочим патологическим процессам;
В результате этот элемент препятствует развитию аллергии, воспалению и прочим патологическим процессам; - ртуть – даже она в незначительном количестве содержится в клетках человека. Здесь выделяют пользу в работе мозга – заметно улучшается интеллект, пробуждается сознание, быстрее заживляются раны;
- серебро – в клетках человека уничтожает большинство бактерий, которые провоцируют развитие опасных заболеваний вплоть до серьезного отравления;
- золото – уничтожает большое количество микробов, помогает в деятельности сосудов и сердца.
Роль макро- и микроэлементов в жизни человека неоценима, поскольку именно химические элементы задают ритм на работу всего организма. Чтобы восполнить пробелы, необходимо практиковать правильное питание и разнообразить рацион. Это поможет сбалансировать химические элементы в своем организме, что положительно скажется на всей работе и жизнедеятельности человека.
Каково значение макроэлемента кальций, и в какой пище он содержится
Суточная потребность в кальции — 0,8 г.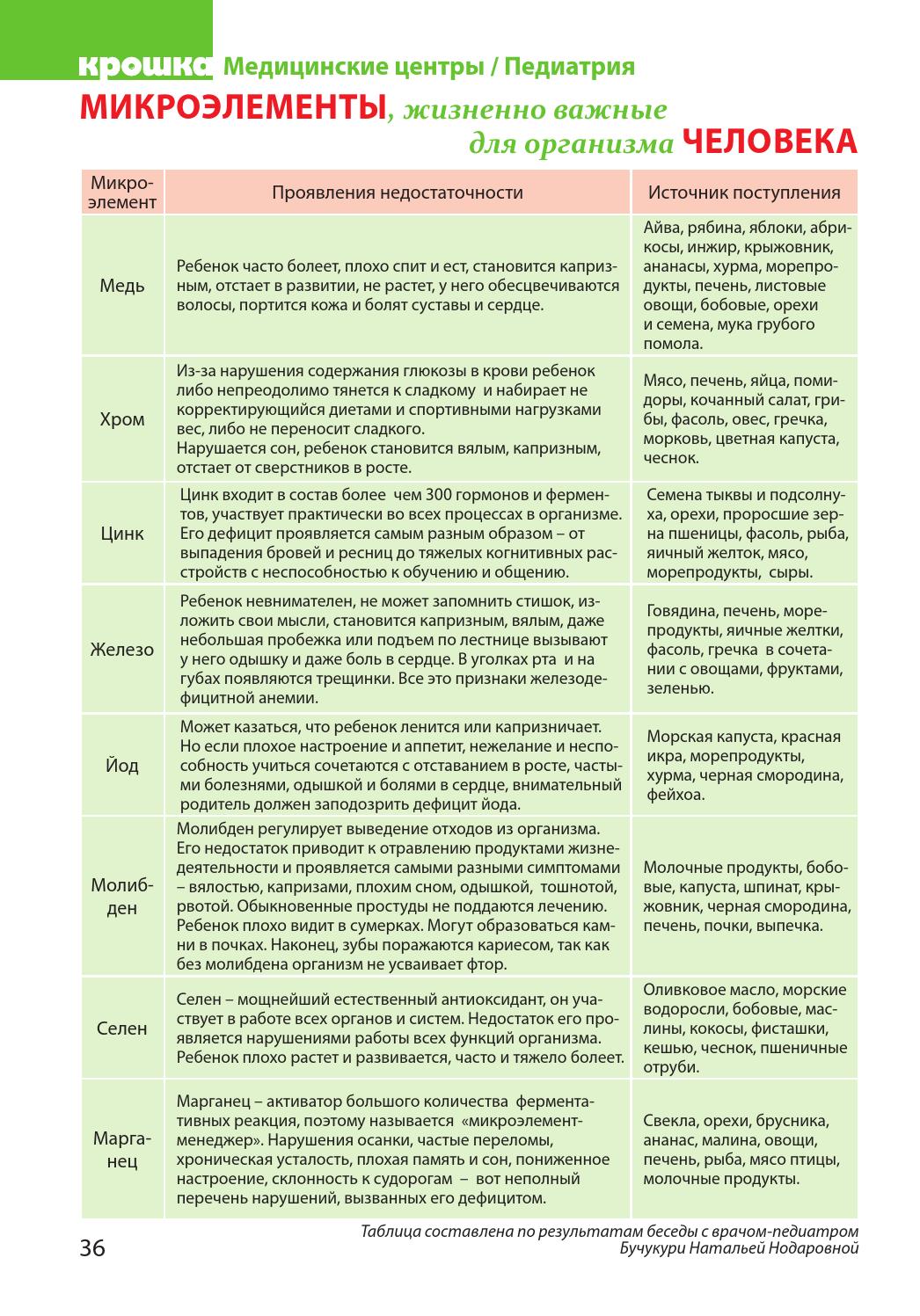 Основная роль кальция в организме – формирование костной ткани. Также этот микроэлемент участвует в процессах возбудимости нервной ткани, сократимости мышц и свертываемости крови, уменьшает проницаемость сосудов, обладает противовоспалительным действием и уменьшает проявления аллергии.
Основная роль кальция в организме – формирование костной ткани. Также этот микроэлемент участвует в процессах возбудимости нервной ткани, сократимости мышц и свертываемости крови, уменьшает проницаемость сосудов, обладает противовоспалительным действием и уменьшает проявления аллергии.
При избытке в пище фосфора, в частности в виде зерновых и бобовых продуктов, в кишечнике образуются нерастворимые соединения кальция, которые выводятся с калом; возможно выведение кальция из костей.
Сочетание продуктов часто улучшает соотношение кальция и фосфора, например каши на молоке, хлеб с сыром, овощные гарниры к мясным и рыбным блюдам. Усвоение макроэлемента кальций из пищи ухудшается при недостатке или избытке в рационе белков.
Избыток жиров, особенно бараньего, говяжьего сала, превращает кальций в невсасывающиеся кальциевые мыла. Ухудшает всасывание кальция щавелевая кислота, которой богаты шпинат, щавель, ревень, свекла, шоколад. При дефиците витамина D всасывание кальция резко нарушается и начинает использоваться кальций костей.
Содержание кальция увеличивают в рационе до 1,5-2 г при аллергических и воспалительных заболеваниях, при переломах костей, туберкулезе, заболеваниях, ведущих к нарушению всасывания кальция (хронические энтериты и панкреатиты, плохое желчеотделение при болезнях желчных путей).
Содержание макроэлемента кальций в продуктах (в мг на 100 г съедобной части):
- Очень большое (более 100): сыр голландский, сыр плавленый, молоко, кефир, творог, фасоль, петрушка, лук зеленый.
- Большое (51-100): сметана, яйца, гречневая и овсяная крупы, горох, морковь, ставрида, сельдь, икра.
- Умеренное (25-50): масло сливочное, скумбрия, окунь, судак, треска, пшено, крупа перловая, хлеб из муки 2-го сорта, капуста, горошек зеленый, редис, свекла, абрикосы, вишня, сливы, виноград, апельсины, клубника.
- Малое (менее 25) содержание макроэлемента кальций в продуктах питания: мясо, картофель, огурцы, помидоры, арбуз, яблоки, груши.
Роль в человеческом организме
Роль макроэлементов в человеческом организме сводится к обеспечению главных процессов жизнедеятельности:
- дыхания;
- кроветворения;
- поддержания целостности покровов и костных тканей.

Более подробно роль всех макроэлементов в организмах теплокровных животных и людей описана в таблице:
Название макронутриента | Характеристики и основная работа в организме человека |
|---|---|
Калий | Обнаруживается в клетках крови и головного мозга. Участвует в работе ЦНС, поддерживает кислотно-щелочной баланс организма, важен и необходим в образовании электролитов. |
Кальций | Наибольшее количество его содержится в костной ткани. Именно кальций отвечает за крепость костей и правильную работу опорно-двигательного аппарата. |
Магний | Обнаруживается в нервных клетках. Именно магний позволяет оптимизировать проводимость и отвечает за правильную передачу сигналов из головного мозга к прочим системам и органам. |
Кислород | Необходим для дыхания клеток и поддержания водного баланса в организме. |
Углерод | Является побочным продуктом, образуемым в процессе дыхания. Вступает в сложные реакции с другими неорганическими веществами и участвует в делении клеток. |
Водород | В организм человека попадает с водой и из воздуха. Сам по себе не имеет ценности для клеток, но благодаря тому, что вещество вступает в реакции с прочими жизненно необходимыми веществами, образуются сложные органические соединения, такие как белки, жиры и углеводы. Кроме того, вещество участвует в образовании рибонуклеиновых и дезоксирибонуклеиновых кислот, являющихся источниками генной информации. |
Азот | Содержится во всех без исключения гормонах, а также обнаруживается в белках и аминокислотах. Сам по себе азот не имеет биологической ценности, но благодаря способности быстро образовывать крепкие связи выполняет множество защитных функций. |
Натрий | Вещество является составной частью электролита – основного раствора в клетках. Соли натрия удерживают воду, чем защищают клетки от обезвоживания. Также вещество в виде макроэлемента помогает правильно передавать сигналы от головного мозга к мышцам. |
Сера | Обнаружена в двух разных аминокислотах, способных создать протеины – основу жизнедеятельности организма. |
Фосфор | В большей мере вещество сконцентрировано в костной ткани. Вступает в стойкие взаимосвязи с кальцием и способствует поддержанию скелета в «рабочем» состоянии. |
Хлор | В большом количестве хлор содержится в соляной кислоте. Благодаря этой жидкости, находящейся в желудке, человек и теплокровные животные имеют возможность переваривать пищу любого происхождения. |
Все вышеописанные вещества в определенном количестве присутствуют в тканях. В случае, когда уменьшается поступление их извне, организм высвобождает макроэлементы, нарушая работу слаженной системы. В том случае, когда возникает избыточное поступление веществ, все сверхнормативное количество накапливается клетками. Это тоже плохо, а для полноценной и правильной работы организма необходимо поддерживать сбалансированное количество макроэлементов.
Суточная норма
Суточная норма потребления макроэлементов в организме человека должна быть такой, чтобы ею можно было восполнить израсходованные вещества в полном объеме. Значение показателей зависит от:
- возраста;
- роста;
- массы тела;
- образа жизни человека;
- физической активности;
- рода занятий.
На количество необходимых макроэлементов оказывают влияние также хронические заболевания, к которым относят не только сахарный диабет, сердечную и почечную недостаточности, гормональный дисбаланс, но и вредные привычки, по определению отнесенные к болезням – алкоголизм и табакокурение.
С примерной суточной потребностью в макроэлементах можно ознакомиться в таблице ниже. Все данные приведены на основе исследований отечественных ученых нынешнего времени. Представления ученых стран Европы, США и прочих могут отличаться от приведенных значений.
В отдельной графе указано усредненное количество основных веществ, находящихся в организме человека «в запасе».
Название макронутриента | Количество в организме взрослого человека средних параметров | Дети от рождения до 14 лет | Подростки в период полового созревания | Взрослые независимо от пола |
|---|---|---|---|---|
Калий | 120 г | 400 мг | 1500 мг | 2,5 г |
Кальций | 1000 г | 400 мг | 1200 мг | 1000 мг |
Магний | 25 г | 80 мг | 250 мг | 400 мг |
Кислород | Нет информации. | Не нормируется. | Не нормируется. | Не нормируется. |
Углерод | Нет информации. | Не нормируется. | Не нормируется. | Не нормируется. |
Водород | Нет информации. | Не нормируется. | Не нормируется. | Не нормируется. |
Азот | 60 г (в белке) | 10 г | 15 г | 20 г |
Натрий | 200 г | 280 мг | 1,3 г | 1,3 г |
Сера | 140 г | 4 г | 4 г | 5 г |
Фосфор | 700 г | 300 мг | 500 мг | 1200 мг |
Хлор | 60 г | 300 мг | 1900 мг | 2300 мг |
В некоторых макроэлементах, таких как кальций и фосфор, нуждаются женщины. Это связано с репродуктивной функцией, беременностью и лактацией, а также некоторыми возрастными особенностями функционирования организма в климактерический и постклимактерический периоды. В дополнительных источниках кальция нуждаются люди, страдающие заболеваниями, связанными с невозможностью восприятия и правильного распределения полученного макроэлемента.
Это связано с репродуктивной функцией, беременностью и лактацией, а также некоторыми возрастными особенностями функционирования организма в климактерический и постклимактерический периоды. В дополнительных источниках кальция нуждаются люди, страдающие заболеваниями, связанными с невозможностью восприятия и правильного распределения полученного макроэлемента.
В отличие от микроэлементов, нарушение в усваиваемости и насыщаемости организма макроэлементами можно выявить и по анализу мочи. Потеря кальция костной тканью или излишнее насыщение клеток солями, содержащими фосфор, легко определяется в обычной лаборатории, которая есть почти при всех поликлиниках и больницах.
7.4: Микроэлементы в биологических системах
- Последнее обновление
- Сохранить как PDF
- MACROMOMERSALS
- Групповые реакции передачи
- Реакции биологического окисления
- Структурные компоненты
- Пример 9
- Сводка
- Ключ на вынос
- Концептуальные проблемы
Текстовая карта Libretexts по общей химии, организованная вокруг учебника
Химия: принципы, закономерности и приложения
Брюса А. Аверилл
Аверилл
I II III И.В. V В.И. VII VIII IX X XI XII XIII XIV Х V Х В.И. Х VII Х VIII Х IX Х Х Х XI Х XII Х XII Я Х XIV ● Домашнее задание
Цели обучения
- Описать некоторые роли микроэлементов в биологических системах.
Из более чем 100 известных элементов примерно 28 являются незаменимыми для роста по крайней мере одного биологического вида, и только 19 необходимы человеку.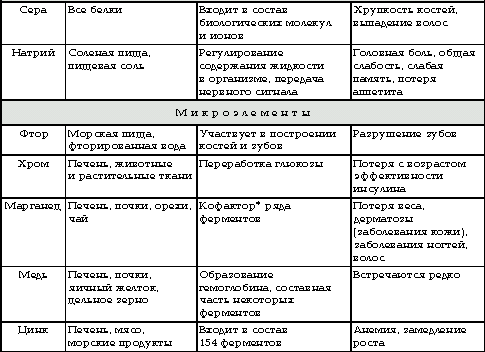 Что делает некоторые элементы необходимыми для организма, а остальные несущественными? Есть как минимум две причины:
Что делает некоторые элементы необходимыми для организма, а остальные несущественными? Есть как минимум две причины:
- Элемент должен иметь какое-то уникальное химическое свойство, которое организм может использовать в своих интересах и без которого он не может выжить.
- В окружающей среде должно быть достаточное количество элемента в легкодоступной форме.
Как видно из таблицы 7.6, многие из элементов, которыми богата земная кора, тем не менее не находятся в легкодоступной форме (например, в виде ионов, растворенных в морской воде). Вместо этого они имеют тенденцию образовывать нерастворимые оксиды, гидроксиды или карбонатные соли. Хотя кремний является вторым наиболее распространенным элементом в земной коре, SiO 2 и многие силикатные минералы нерастворимы, поэтому они с трудом усваиваются живыми тканями. Это также относится к железу и алюминию, которые образуют нерастворимые гидроксиды.Поэтому многие организмы разработали сложные стратегии получения железа из окружающей среды. Напротив, молибден и йод, хотя и не особенно распространены, хорошо растворимы — молибден в виде молибдата (MoO 4 2–) и йод в виде йодида (I –) и йодата (IO 3 ––) — и поэтому в морской воде их больше, чем железа. Неудивительно, что и молибден, и йод используются многими организмами.
Напротив, молибден и йод, хотя и не особенно распространены, хорошо растворимы — молибден в виде молибдата (MoO 4 2–) и йод в виде йодида (I –) и йодата (IO 3 ––) — и поэтому в морской воде их больше, чем железа. Неудивительно, что и молибден, и йод используются многими организмами.
Таблица 7.6 Относительное содержание некоторых эфирных элементов в земной коре и океанах
| Элемент* | Корка (частей на миллион; в среднем) | Морская вода (мг/л = частей на миллион) |
|---|---|---|
| *Известно, что элементы, выделенные жирным шрифтом, необходимы человеку. | ||
| О | «> 461 000 | 857 000 |
| Си | 282 000 | 2,2 |
| Ал | 82 300 | 0,002 |
| Фе | «> 56 300 | 0,002 |
| Ка | 41 500 | 412 |
| Нет данных | 23 600 | 10 800 |
| мг | «> 23 300 | 1290 |
| К | 20 900 | 399 |
| Н | 1400 | 108 000 |
| П | «> 1050 | 0.06 |
| Мн | 950 | 0,0002 |
| Ф | 585 | 1,3 |
| С | «> 350 | 905 |
| С | 200 | 28 |
| Класс | 145 | 19 400 |
| В | «> 120 | 0.0025 |
| Кр | 102 | 0,0003 |
| Никель | 84 | 0,00056 |
| Цинк | «> 70 | 0,0049 |
| Медь | 60 | 0,00025 |
| Ко | 25 | 0.00002 |
| Ли | «> 20 | 0,18 |
| Н | 19 | 0,5 |
| Бр | 2,4 | 67,3 |
| Пн | «> 1,2 | 0,01 |
| я | 0.45 | 0,06 |
| Се | 0,05 | 0,0002 |
Источник: Данные CRC Handbook of Chemistry and Physics (2004).
К счастью, многие элементы, необходимые для жизни, необходимы лишь в небольших количествах. (В таблице 1.6 перечислены микроэлементы в организме человека.) Тем не менее, элементы, присутствующие в следовых количествах, могут оказывать большое влияние на здоровье организма.Такие элементы функционируют как часть механизма амплификации, в котором молекула, содержащая микроэлемент, является существенной частью более крупной молекулы, которая, в свою очередь, регулирует концентрацию других молекул и так далее. Механизм амплификации позволяет небольшим изменениям концентрации микроэлемента оказывать большое биохимическое воздействие.
(В таблице 1.6 перечислены микроэлементы в организме человека.) Тем не менее, элементы, присутствующие в следовых количествах, могут оказывать большое влияние на здоровье организма.Такие элементы функционируют как часть механизма амплификации, в котором молекула, содержащая микроэлемент, является существенной частью более крупной молекулы, которая, в свою очередь, регулирует концентрацию других молекул и так далее. Механизм амплификации позволяет небольшим изменениям концентрации микроэлемента оказывать большое биохимическое воздействие.
Эссенциальные микроэлементы у млекопитающих могут играть четыре основные роли: (1) они могут вести себя как макроминералы, (2) они могут участвовать в катализе реакций группового переноса, (3) они могут участвовать в окислительно-восстановительных реакциях или ( 4) они могут служить структурными элементами.
Макроминералы
Макроминералы — Na, Mg, K, Ca, Cl и P — содержатся в больших количествах в биологических тканях и присутствуют в виде неорганических соединений, растворенных или осажденных.
 Все образуют одноатомные ионы (Na + , Mg 2+ , K + , Ca 2+ , Cl — ), за исключением фосфора, который находится в виде иона фосфата (PO 4 9 − ). Напомним, что соли кальция используются многими организмами в качестве структурных материалов, например, в костях [гидроксиапатит, Ca 5 (PO 4 ) 3 OH]; соли кальция есть также в морских раковинах и яичной скорлупе (CaCO 3 ), а в растениях они служат хранилищем для Ca 2+ (оксалат кальция).
Все образуют одноатомные ионы (Na + , Mg 2+ , K + , Ca 2+ , Cl — ), за исключением фосфора, который находится в виде иона фосфата (PO 4 9 − ). Напомним, что соли кальция используются многими организмами в качестве структурных материалов, например, в костях [гидроксиапатит, Ca 5 (PO 4 ) 3 OH]; соли кальция есть также в морских раковинах и яичной скорлупе (CaCO 3 ), а в растениях они служат хранилищем для Ca 2+ (оксалат кальция).Жидкости организма всех многоклеточных организмов содержат относительно высокие концентрации этих ионов. Некоторые ионы (Na + , Ca 2+ и Cl — ) локализованы в основном во внеклеточных жидкостях, таких как плазма крови, тогда как K + , Mg 2+ и фосфат локализованы преимущественно в в внутриклеточных жидкостях. Для избирательного транспорта этих ионов через клеточные мембраны требуется значительное количество энергии.
 Селективность этих ионных насосов основана на различиях в ионном радиусе (раздел 7.2) и ионный заряд.
Селективность этих ионных насосов основана на различиях в ионном радиусе (раздел 7.2) и ионный заряд.Поддержание оптимального уровня макроминералов важно, поскольку временные изменения их концентрации в клетке влияют на биологические функции. Например, для передачи нервного импульса требуется внезапное обратимое увеличение количества Na + , поступающего в нервную клетку. Точно так же, когда гормоны связываются с клеткой, они могут вызвать проникновение ионов Ca 2+ в эту клетку. В сложной серии реакций ионы Ca 2+ запускают такие события, как сокращение мышц, высвобождение нейротрансмиттеров или секрецию гормонов.Когда люди, которые интенсивно тренируются в течение длительного периода времени, чрезмерно пьют воду, низкий уровень соли в крови может привести к состоянию, известному как гипонатриемия , которое вызывает тошноту, усталость, слабость, судороги и даже смерть. По этой причине спортсменам следует пить спортивный напиток, содержащий соли, а не только воду.
Реакции группового переноса
Следовые ионы металлов также играют решающую роль во многих биологических реакциях переноса групп.В этих реакциях узнаваемая функциональная группа, такая как фосфорильная единица (-PO 3 — ), переносится с одной молекулы на другую. В этом примере
Уравнение 7.18
ROPO2-3+h3O→ROH+HOPO2-3
ед. переводится из алкоксида (RO − ) в гидроксид (OH − ). Чтобы нейтрализовать отрицательный заряд молекулы, которая подвергается реакции, многие биологические реакции этого типа требуют присутствия ионов металлов, таких как Zn 2+ , Mn 2+ , Ca 2+ или Mg 2+ и иногда Ni 2+ или Fe 3+ .Эффективность иона металла во многом зависит от его заряда и радиуса.
Цинк является важным компонентом ферментов, катализирующих гидролиз белков, присоединение воды к CO 2 с образованием HCO 3 − и H + , а также большинство реакций, связанных с ДНК (дезоксирибонуклеиновая кислота). ) и синтез, репарация и репликация РНК (рибонуклеиновой кислоты). Следовательно, дефицит цинка имеет серьезные побочные эффекты, включая аномальный рост и половое развитие, а также потерю вкусовых ощущений.
Биологические реакции окисления-восстановления
Третьей важной ролью микроэлементов является перенос электронов в биологических окислительно-восстановительных реакциях. Железо и медь, например, содержатся в белках и ферментах, участвующих в транспорте O 2 , восстановлении O 2 , окислении органических молекул и превращении атмосферного N 2 в NH 3 . Эти металлы обычно переносят один электрон на ион металла, чередуя состояния окисления, такие как 3+/2+ (Fe) или 2+/1+ (Cu).
Поскольку большинство переходных металлов имеют несколько степеней окисления, разделенных только одним электроном, они идеально подходят для одновременного переноса нескольких электронов. Примеры включают молибден (+6/+5/+4), который широко используется в реакциях двухэлектронного окисления-восстановления, и кобальт (+3/+2/+1), который содержится в витамине B 12 . Напротив, многие из р -блочных элементов хорошо подходят для переноса двух электронов сразу. Например, селен (+4/+2) содержится в ферменте, катализирующем окисление глутатиона (GSH) до его дисульфидной формы (GSSG):
\[2 GSH + H_ 2 O_ 2 \rightarrow 2 H_ 2 O + GSSG\]
Структурные компоненты
Микроэлементы также действуют как важные структурные компоненты биологических тканей или молекул.Во многих системах, где микроэлементы не изменяют степени окисления или иным образом непосредственно не участвуют в биохимических реакциях, часто предполагается, хотя часто и без прямых доказательств, что элемент стабилизирует определенную трехмерную структуру биомолекулы, в которой он находится. Одним из примеров является сахаросвязывающий белок, содержащий Mn 2+ и Ca 2+ , который является частью системы биологической защиты некоторых растений. Другие примеры включают ферменты, которым требуется Zn 2+ в одном месте для проявления активности в другом месте молекулы.Некоторые неметаллические элементы, такие как F — , также играют структурную роль. Фтор, например, вытесняет ион гидроксида из гидроксиапатита в костях и зубах с образованием фторапатита [Ca 5 (PO 4 ) 3 F]. Фторапатит менее растворим в кислоте и обеспечивает повышенную устойчивость к кариесу.
Фторапатит (\(Ca_5(PO_4)_3F\)) менее растворим, чем гидроксиапатит (\(Ca_5(PO_4)_3(OH)\))
Другим примером неметалла, который играет структурную роль, является йод, который в организме человека содержится только в одной молекуле, гормоне щитовидной железы тироксине .Когда рацион человека не содержит достаточного количества йода, щитовидная железа на шее сильно увеличивается, что приводит к состоянию, называемому зобом . Поскольку йод содержится в основном в морской рыбе и водорослях, у многих первых поселенцев Среднего Запада Америки развился зоб из-за отсутствия в их рационе морепродуктов. Сегодня большая часть поваренной соли содержит небольшое количество йода [фактически йодида калия (KI)], чтобы предотвратить эту проблему.
Больной зобом. В США «йодированная соль» предотвращает возникновение зоба.
Пример 9
Есть некоторые свидетельства того, что олово является важным элементом для млекопитающих. Основываясь исключительно на том, что вы знаете о химическом составе олова и его положении в периодической таблице, предскажите вероятную биологическую функцию олова.
Дано: элемент и данные таблицы 1.6
Запрашиваемый: вероятная биологическая функция
Стратегия:
Из положения олова в периодической таблице, его общих степеней окисления и данных таблицы 1.6, предсказать вероятную биологическую функцию элемента.
Решение:
Из его положения в нижней части группы 14 мы знаем, что олово — это металлический элемент, наиболее распространенными степенями окисления которого являются +4 и +2. Учитывая низкий уровень олова у млекопитающих (140 мг/70 кг человека), маловероятно, что олово будет функционировать как макроминерал. Хотя нельзя исключать его роль в катализе реакций переноса группы или в качестве важного структурного компонента, наиболее вероятная роль олова будет заключаться в катализе реакций окисления-восстановления, которые включают перенос двух электронов.Это позволило бы использовать способность олова иметь две степени окисления, разделенные двумя электронами.
Упражнение
Основываясь исключительно на том, что вы знаете о химическом составе ванадия и его положении в периодической таблице, предскажите вероятную биологическую функцию ванадия.
Ответ: Ванадий, вероятно, катализирует реакции окисления-восстановления, поскольку он является переходным металлом первого ряда и, вероятно, имеет несколько степеней окисления.
Резюме
Многие элементы периодической таблицы являются незаменимыми микроэлементами , которые необходимы для роста большинства организмов.Хотя они присутствуют только в небольших количествах, они имеют важные биологические эффекты из-за их участия в механизме амплификации . Макроминералы присутствуют в больших количествах и играют структурную роль или действуют как электролиты, распределение которых в клетках строго контролируется. Эти ионы избирательно транспортируются через клеточные мембраны с помощью ионных насосов . Другие микроэлементы катализируют реакции группового переноса или биологические окислительно-восстановительные реакции, в то время как другие являются важными структурными компонентами биологических молекул.
Ключ на вынос
- Основные микроэлементы у млекопитающих играют четыре основные роли: в качестве макроминералов, в качестве катализаторов в реакциях группового переноса или окислительно-восстановительных реакциях или в качестве структурных компонентов.
Концептуальные проблемы
Приведите хотя бы один критерий незаменимых элементов, участвующих в биологических окислительно-восстановительных реакциях. Какая область периодической таблицы содержит элементы, которые очень хорошо подходят для этой роли? Объясните свои рассуждения.
Какова общая биологическая роль микроэлементов, не имеющих двух или более доступных степеней окисления?
Микроэлементы – обзор
Микроэлементы
Микроэлементы, также известные как микроминералы, представляют собой вещества, составляющие менее 0,01% массы тела. В грудном молоке к ним относятся железо, цинк, медь, марганец, селен, йод, фтор, молибден, кобальт, хром и никель.
Железо является важным компонентом гема в гемоглобине, миоглобине, цитохромах и других белках; следовательно, он играет роль в транспортировке, хранении и использовании кислорода. Железодефицитной анемией страдает около 30% населения мира, включая западные и слаборазвитые страны. Средняя концентрация железа в грудном молоке составляет 0,3 мг/л. Содержание железа в грудном молоке снижается в течение периода лактации; уровень железа в молозиве составляет около 1 мг/л, а в зрелом молоке снижается до 0,3–0,6 мг/л.Потребление железа с пищей не связано с концентрацией железа в грудном молоке, а добавление железа в количестве до 30 мг/день не влияет на концентрацию железа в молоке. Железо грудного молока связано с тремя основными компонентами: лактоферрином, низкомолекулярным соединением, и компонентом мембраны шариков молочного жира. Лактоферрин является основным железосвязывающим белком в грудном молоке, обладающим высоким сродством к ионам трехвалентного железа, которые связывают два участка вместе с ионами бикарбоната или карбоната.Концентрация лактоферрина в грудном молоке намного выше, чем концентрация железа, поэтому, хотя одна треть железа связана с лактоферрином, только 3-5% лактоферрина насыщено железом. Однако железо, высвобождаемое из других компонентов во время пищеварения, может связываться с лактоферрином, особенно при наличии бикарбоната из жидкости поджелудочной железы. Цитрат в низкомолекулярной фракции и ксантиноксидаза в мембране жировых шариков могут быть среди этих других железосвязывающих компонентов. Очень мало железа в грудном молоке связано с казеином (Lonnerdal, 1989).
Цинк необходим для правильного роста и развития, полового созревания, заживления ран и может играть роль в функционировании иммунной системы и других физиологических процессах. Цинк помогает нескольким гормонам, участвующим в репродукции, необходим для синтеза ДНК, РНК и белков, а также является кофактором многих ферментов, участвующих в большинстве основных метаболических процессов (Flynn, 1992). О дефиците цинка у человека впервые сообщили в 1960-х годах на Ближнем Востоке, что привело к карликовости, нарушению полового развития и анемии.Трудно обнаружить умеренный дефицит цинка, хотя было показано, что он встречается в западных странах, особенно у младенцев и детей, и приводит к субоптимальному росту, плохому аппетиту, нарушению остроты вкуса и низкому уровню цинка в волосах. Средняя концентрация цинка в зрелом грудном молоке в течение первых шести месяцев лактации составляет около 2 мг/л, хотя сообщалось о больших колебаниях уровня цинка в пределах 0,65–5,3 мг/л. Потребление цинка с пищей не коррелирует с содержанием цинка в грудном молоке, а добавление цинка в диету с достаточным содержанием цинка не оказывает существенного влияния на концентрацию цинка в грудном молоке.Цинк в грудном молоке содержится в трех основных компонентах: сывороточном альбумине и цитрате в сыворотке и в щелочной фосфатазе в мембране жировых шариков.
Медь необходима для утилизации железа и является кофактором ферментов, участвующих в метаболизме глюкозы, а также в синтезе гемоглобина, фосфолипидов и соединительной ткани. Дефицит меди встречается редко, за исключением случаев тяжелого недоедания. Зрелое грудное молоко содержит медь в концентрации 0,3 мг/л. Концентрация меди снижается по мере увеличения лактации, начиная с 0.6 мг/л в первую и вторую недели лактации, до 0,36 мг/л к 6–8 неделям и 0,21–0,25 мг/л к 20 неделям лактации. Не существует существенной корреляции между концентрацией меди в молоке и потреблением меди с пищей. Медь в грудном молоке связана с сывороточным альбумином и цитратом. Медь также была обнаружена в мембране жировых шариков, однако лиганд до сих пор не идентифицирован.
Марганец является кофактором гликозилтрансфераз, играющих роль в синтезе мукополисахаридов, а также неспецифическим кофактором многих других ферментов.Были идентифицированы два металлофермента марганца: митохондриальная супероксиддисмутаза и пируваткарбоксилаза (Hurley & Keen, 1987). Поскольку марганец широко распространен в пищевых продуктах, о дефиците марганца у людей не известно (Flynn, 1992). В зрелом человеческом молоке средняя концентрация марганца составляет примерно 10 мкг/л, и известно, что содержание марганца снижается с увеличением продолжительности лактации. О случаях дефицита марганца у младенцев не сообщалось, поэтому дети, находящиеся на полном грудном вскармливании, получают достаточное количество марганца (Lonnerdal et al., 1983). Марганец в грудном молоке в основном связан с лактоферрином, однако он существует в такой низкой концентрации, что примерно в 2000 раз больше железа связано с лактоферрином, чем марганца. Поэтому очень малая часть металлсвязывающей способности лактоферрина занята марганцем (Lonnerdal, 1989).
Селен является важным компонентом фермента глутатионпероксидазы. Глутатионпероксидаза присутствует во многих тканях, где она работает с витамином Е, каталазой и супероксиддисмутазой в качестве антиоксиданта, защищая клетки от окислительного повреждения.Концентрация селена в молоке женщин США составляет примерно 16 мкг/л. Концентрация селена выше в молозиве – 41 мкг/л, чем в зрелом молоке – 16 мкг/л. Наблюдалась корреляция между содержанием селена в грудном молоке и концентрацией селена в плазме матери, а также активностью глутатионпероксидазы в плазме, что свидетельствует о том, что на содержание селена в молоке влияет статус селена у матери (Levander et al., 1987). Среднее содержание селена в молоке североамериканских женщин считается более чем достаточным для грудных детей.
Йод необходим для гормонов щитовидной железы, тироксина и трийодтиронина, которые играют важную роль в регуляции основного энергетического обмена и репродукции. Дефицит йода вызывает увеличение щитовидной железы и образование зоба, в то время как избыток йода в рационе снижает поглощение йода щитовидной железой, что дает признаки дефицита щитовидной железы. В Соединенных Штатах средняя концентрация йода в грудном молоке составляет 142 мкг/л (диапазон: 21–281 мкг/л). Наблюдалась корреляция между концентрацией йода в молоке и потреблением йода с пищей, поэтому использование йодированной соли может увеличить содержание йода в молоке (ААР, 1981).Североамериканские женщины потребляют повышенное количество йода, поэтому количество йода в их молоке является адекватным.
Молибден является важным компонентом нескольких ферментов, включая альдегидоксидазу, ксантиноксидазу и сульфитоксидазу, где он присутствует в простетической группе молибдоптерина. Еще предстоит определить, связана ли потребность человека именно в молибдене или же в молибдоптерине или его предшественнике. Диетического дефицита у людей не наблюдалось, за исключением пациентов, длительно находящихся на полном парентеральном питании.Содержание молибдена в грудном молоке сильно коррелирует со стадией лактации, снижаясь с 15 мкг/л в 1-й день до 4,5 мкг/л к 14-му дню и, наконец, до концентрации примерно 2 мкг/л к одному месяцу и позже.
Хром считается важным для здоровья человека, и самым ранним признаком дефицита является нарушение толерантности к глюкозе. Дефицит хрома наблюдался исключительно у больных, длительно получающих полное парентеральное питание. Эти пациенты реагируют на внутривенное введение трехвалентного хрома улучшением непереносимости глюкозы.Среднее содержание хрома в зрелом грудном молоке составляет 0,27 мкг/л.
Единственная функция кобальта, выявленная у человека, – это его присутствие в качестве основного компонента витамина B 12 . Витамин B 12 синтезируется из бактерий. Таким образом, неорганический кобальт необходим для всех животных, которые полностью полагаются на свою бактериальную флору в качестве источника витамина B 12 . Зрелое грудное молоко содержит кобальт в концентрации приблизительно 0,1 мкг/л. Пищевые добавки кобальта повышают уровень витамина B 12 в грудном молоке только в том случае, если в материнском рационе недостаточно кобальта.
Фтор считается полезным, а не необходимым элементом для здоровья человека, поскольку он защищает от кариеса и накапливается в костях и зубах. Однако чрезмерное потребление фтора приводит к флюорозу, который вызывает пятнистость зубов, а также влияет на здоровье костей и функцию почек. В зрелом грудном молоке среднее содержание фтора составляет около 16 мкг/л. Младенцы, находящиеся на грудном вскармливании или потребляющие концентрированные или сухие смеси, приготовленные с нефторированной водой, потребляют мало фтора и должны получать добавки фтора (NRC, 1989).
Существуют убедительные доказательства необходимости никеля, кремния, мышьяка и бора для животных, и наиболее вероятно, что эти микроэлементы необходимы и человеку. Однако питательные функции этих элементов еще предстоит определить (NRC, 1989). Никель содержится в зрелом человеческом молоке на уровне 1,2 мкг/л, кремний – 700 мкг/л, мышьяк – 0,2 – 0,6 мкг/л (Renner, 1983).
Биология микроэлементов: база знаний и ее применение для питания людей и населения | Журнал питания
Аннотация
Впечатляющие успехи достигнуты в понимании метаболизма и функции микроэлементов.Это подчеркивается многочисленными вкладами в эти разбирательства. Однако не столь впечатляющими являются: i ) трудно оценить точное распознавание легкого дефицита микроэлементов и как установить их функциональные последствия, возможно смешанные с одновременным дефицитом микроэлементов, ii ) подходы к количественному определению потребности в микроэлементах остаются неудовлетворительными и архаичными во многих отношениях, iii ) наше понимание степени биологической основы различий в потребностях между внешне похожими людьми плохо, и iv ) многое еще предстоит узнать о количественная степень, в которой генетические, эпигенетические и диетические факторы взаимодействуют для определения пищевого фенотипа.Представлены некоторые идеи относительно того, как мы могли бы использовать в контексте реконструктивного подхода захватывающие новые знания и связанные с ними методы, появившиеся в эпоху постгенома, и разработать новые парадигмы для оценки потребностей и состояния микроэлементов, а также для установления эффективного потребления питательных веществ в условиях разные условия сложных генотип-средовых взаимодействий. Метаболиты являются функциональными клеточными образованиями, и я также призываю к активному применению метаболомики и метаболического профилирования, тесно связанных с геномикой, протеомикой, кинетикой микроэлементов и системным анализом, в качестве компонентов новой интегративной парадигмы.Нам нужно понять систему и ее стратегию, а не только молекулярные детали ее составных частей и отдельных элементов управления. Для достижения этой цели потребуются междисциплинарные исследования и обучение. Все это связано с нашей общей целью содействовать повышению роли микроэлементов для благополучия человека посредством расширения биологических знаний и их эффективного применения.
Для меня большая честь, что меня попросили помочь завершить то, что было для меня действительно захватывающим и информативным TEMA 11.Было предложено, чтобы я попытался связать, в том числе определить некоторые из сильных и возможных слабых сторон современного направления исследований, расширяющиеся знания по базовой биологии микроэлементов с заботой о микроэлементах и питании людей и популяций в различных условиях. Это решительный вызов, и можно даже спросить, почему мне его предложили, потому что, за исключением относительно короткого перерыва в 1980-х годах (1–3), я, по сути, отказался от исследований, посвященных минеральному обмену и питанию, как только я защитил докторскую диссертацию.D тезис (4–6). Можно, однако, предположить, что одна из причин такого приглашения состоит в том, что даже тот, кто прежде всего интересовался метаболизмом аминокислот и белков, может обнаружить связь с микроэлементами еще в самом начале жизни; так, около 4 миллиардов лет назад, согласно одной общей теории, основанной на гидротермальном происхождении жизни на Земле, в железо-серном мире под давлением или в среде железа возник автотрофный метаболизм низкомолекулярных компонентов, включая аминокислоты и пептиды. -сульфидные и горячие магматические выбросы (7), для которых появляется все больше подтверждающих данных (8).Действительно, это напоминает интересные исследования Росса и Эйзенштейна (9) по митохондриальной аконитазе, которая имеет железо-серный кластер [4Fe-4S] и считается древним ферментом (10). Он катализирует превращение цитрата в изоцитрат, и они (9) показывают, что он является мишенью для регуляции белками, регулирующими железо; хороший пример связи между микроэлементом и метаболизмом макронутриентов, который меня больше всего интересовал. Другая причина может заключаться в том, что мы все легко подключаемся через небольшой мир научных сетей (11), которые связывают нас вместе в различных областях науки о питании.Наконец, и, возможно, это реально, сейчас для всех нас, заинтересованных в развитии науки о питании и ее применении, как никогда важно широко и активно взаимодействовать по мере того, как биологические знания, а также технологические и информационные базы, от которых зависят наши средства к существованию и понимание, продолжают существовать. расширяться и развиваться с невероятной скоростью.
Видение и некоторые проблемы
Таким образом, я попытаюсь создать картину некоторых предстоящих испытаний или своего рода видение.Это не предсказание, а то, каким может быть мир микроэлементов в организме человека и животных (ТЕМА), и отчасти я подойду к своей задаче с должным признанием многих захватывающих достижений, которые были представлены на ТЕМА 11. и как записано в этих разбирательствах. В частности, большое внимание уделялось деталям молекулярных механизмов, ответственных за поглощение, движение, гомеостаз и функцию микроэлементов. Однако гораздо меньше внимания, чем хотелось бы, уделялось более целостному представлению биологии микроэлементов или общесистемному пониманию микроэлементов в функциях и благополучии человека и животных (12).Позже я укажу на необходимость реконструкционистской деятельности, чтобы дополнить и использовать редукционистскую парадигму, которая оказалась столь успешной, с секвенированием самых маленьких геномов, содержащих ∼396 генов, кодирующих белок (13), в более крупные геномы, включая человека (14, 15) и двух подвидов риса (16, 17), являющихся яркими примерами. Действительно, как спросила редакция (18); «Что означает последовательность генома для меня, моих исследований и моей конституции?» и многие из присутствующих на этой встрече серьезно задумались над этим вопросом, сосредоточив свои исследования на последовательностях соответствующих генов и их функциях.В скобках также интересно, что генетики в настоящее время утверждают, что некодирующие продукты генома (например, некодирующие РНК) функционируют в сетях, регулирующих гены (19, 20), и будет интересно узнать, как микроэлементы могут функционировать через и/или взаимодействовать с «RNome» (21). Тем не менее, мы должны ценить и понимать, что интеграция «_omes и _omics», в конечном счете, является ключом к решению сложных проблем с микроэлементами/питанием. В Таблице 1 перечислены некоторые перспективные области применения новейших знаний о биологии микроэлементов и области дальнейших исследований.Это не исчерпывающий подробный список, а несколько общий список, который я разработал в связи с моими интересами в качестве диетолога-биохимика и который я могу использовать, чтобы изложить свою точку зрения.
ТАБЛИЦА 1Некоторые сложные области применения новейших знаний в области биологии микроэлементов и желаемые области исследований
| • Точное распознавание легкого дефицита микроэлементов и определение их функциональных последствий, возможно, смешанных с другими одновременными недостаточности микроэлементов, трудно оценить |
| • Подходы к количественному определению потребностей в микроэлементах остаются неудовлетворительными и архаичными |
| • Наше понимание биологической основы и степени вариации потребностей среди внешне похожих людей плохое |
| • Необходимо определить количественную степень взаимодействия генетических, эпигенетических и диетических факторов для определения нутритивного фенотипа |
| • Требуются биологические и социологические исследования о том, как наиболее эффективно улучшить потребление и баланс между микроэлементами и другими питательными веществами для оптимизации рациона питания и благополучия отдельных лиц и различных групп населения. |
| • Точное распознавание легкого дефицита микроэлементов и определение его функциональных последствий, возможно, смешанных с другими одновременными дефицитами микроэлементов, трудно оценить |
| • Подходы к количественному определению потребностей для микроэлементов остаются неудовлетворительными и архаичными |
| • Наше понимание биологической основы и степени вариации потребностей среди внешне похожих людей плохое |
| • Необходимо определить количественные степени, в которых генетические, эпигенетические и диетические факторы взаимодействуют, чтобы определить пищевой фенотип |
| • Требуются биологические и социальные исследования, чтобы выяснить, как наиболее эффективно улучшить потребление и баланс между микроэлементами и другими питательными веществами, оптимизировать рацион и улучшить самочувствие отдельных лиц и различных групп населения.группы. |
Некоторые сложные области применения новейших знаний в области биологии микроэлементов и желаемые области исследований
| • Точное распознавание легкого дефицита микроэлементов и определение его функциональных последствий, возможно |
| • Подходы к количественному определению потребности в микроэлементах остаются неудовлетворительными и устаревшими среди внешне похожих людей беден |
| • Необходимо определить количественные степени, в которых взаимодействуют генетические, эпигенетические и диетические факторы для определения пищевого фенотипа |
| эффективно улучшать потребление и баланс между микроэлементами и другими питательными веществами, оптимизировать рацион и самочувствие отдельных лиц и различных групп населения. |
| • Точное распознавание легкого дефицита микроэлементов и определение его функциональных последствий, возможно, смешанных с другими одновременными дефицитами микроэлементов, трудно оценить |
| • Подходы к количественному определению потребностей для микроэлементов остаются неудовлетворительными и архаичными |
| • Наше понимание биологической основы и степени вариации потребностей среди внешне похожих людей плохое |
| • Необходимо определить количественные степени, в которых генетические, эпигенетические и диетические факторы взаимодействуют, чтобы определить пищевой фенотип |
| • Требуются биологические и социальные исследования, чтобы выяснить, как наиболее эффективно улучшить потребление и баланс между микроэлементами и другими питательными веществами, оптимизировать рацион и улучшить самочувствие отдельных лиц и различных групп населения.группы. |
Дефицит микроэлементов.
Первая запись в Таблице 1 начинается с признания трудностей, с которыми все еще приходится сталкиваться при выявлении умеренного дефицита микроэлементов и их функциональных последствий, которые, возможно, дополнительно осложняются другими специфическими, но сопутствующими недостатками. В этом контексте уместно упомянуть два недавних наблюдения: i ) восстановление адекватного статуса цинка с помощью добавок цинка снижает показатели статуса железа при наличии низких запасов железа (22) и ii ) лечение железа дефицит у детей с зобом повышает эффективность йодированного масла в уменьшении зоба (23).Опять же, сообщение состоит в том, что взаимодействие микроэлементов наиболее важно для распознавания и что они также определяют фенотип. Более того, несмотря на то, что дефицит цинка легкой или средней степени тяжести связан с такими симптомами, как плохой аппетит, нарушение вкуса и обоняния, а также плохой рост, они неспецифичны, и, как утверждают Блэк и Мигель (24), «…сложно идентифицировать дефицит цинка с уверенностью. ” То же самое можно сказать и о большинстве, если не обо всех других микроэлементах. Действительно, в этом контексте трудно ответить на некоторые важные вопросы, в том числе: i ) Что такое (или становится) дефицит цинка или любого другого микроэлемента? ii ) Что функционально означает баланс цинка или других микроэлементов? iii ) Как макромолекулярное состояние клеток и органов связано с метаболическим потоком микроэлемента? iv ) Какие временные рамки задействованы? Очевидно, что дефицит цинка, меди или молибдена не обязательно возникает в течение дня недостаточного потребления или повышенных потерь.Это обманчиво сложные вопросы, требующие ответа, если необходимо оптимизировать рационы в отношении содержания и баланса микроэлементов.
Кроме того, с точки зрения дефицита мы должны спросить, например, какие из множества функций цинка (например, 25) и/или механизмы, которые объясняют незаменимость цинка в организме животных, более или менее уязвимы для изменение доступности этого элемента. i ) Существует ли начальное и четко выраженное ускорение одного или нескольких путей апоптоза (группы генетически закодированных программ гибели клеток) (26, 27) в клетках, таких как лимфоциты-предшественники, которые можно относительно легко получить для оценки? ii ) Является ли формирование и/или активность одного или нескольких белков цинковых пальцев (28) или более 700 генов (29), которые кодируют эти факторы транскрипции, затронутыми на ранних этапах развития истощения пулов цинка ; или iii ) репарация и репликация ДНК (30) изменены более непосредственно и глубоко, и может ли этот эффект быть обнаружен и локализован на уровне одной клетки с помощью новых и модифицированных анализов комет (31)?
Как уже упоминалось, задачи здесь еще более интересны и сложны, если должным образом учитывать взаимодействие между микроэлементами и другими питательными веществами.Чтобы еще больше подчеркнуть: a ) активность ДНК-связывающего домена рецептора ретиноевой кислоты (содержащего два цинковых пальца) снижается в прооксидантной среде с высвобождением цинка из мотива цинкового пальца (32). В частности, различается ли фенотип дефицита цинка при различной степени антиоксидантного статуса питательных веществ? b ) Существует цинковый «чувствительный» рецептор, участвующий во внутриклеточной мобилизации кальция и передаче сигналов (33, 34), а c ) мобилизация кальция индуцирует оксид азота, который высвобождает цинк из металлотионеина (35).Следовательно, ранний биохимический дефект при дефиците цинка может быть дефектом кальциевых каналов, как предполагает работа O’Dell и его коллег (36). Важным моментом, опять же, является то, что между микроэлементами, другими минералами и питательными веществами существует множество взаимосвязей и взаимодействий. Они имеют серьезные последствия для того, как мы могли бы расширить и улучшить подходы к оценке состояния питания и потребностей в микроэлементах, особенно у людей.
Требования к микроэлементам.
Вышеизложенное вкратце подводит нас теперь ко второй записи в списке в Таблице 1, а именно к определению потребности человека в микроэлементах на разных этапах жизни и в различных физиологических, диетических и экологических условиях. Думаю, можно согласиться с тем, что используемые на сегодняшний день подходы к определению потребности в микроэлементах (37), подобные указанным в табл. 2, далеки от идеальных, а в некоторых случаях совершенно неудовлетворительны. Помимо недостатка информации и трудностей в проведении исследований на людях, причина этой проблемы заключается в том, что не было согласованных крупных исследований, направленных на установление потребностей в питательных веществах у изначально здоровых людей.Недостаток ресурсов и минимальные обязательства по улучшению предварительных оценок потребностей способствуют сегодняшнему отсутствию надежной количественной информации о потребностях в питательных веществах, несмотря на ее критическую важность для планирования и оценки (38) рационов. Как сказал некоторое время назад Дэвид Бейкер (39 лет): «Ученые-диетологи часто избегают проектов, связанных с определением потребностей в питательных веществах. Эти исследования обычно считаются рутинными, легкими и лишенными творчества. Следовательно, экспертная оценка обычно приводит к «низким оценкам» за такие усилия, что приводит к трудностям в получении внешнего финансирования.«Хотя в этой точке зрения есть значительная доля правды, я считаю, что фундаментальные исследователи и те, кто занимается прикладными исследованиями в области микроэлементов, должны объединить и интегрировать некоторые из своих исследовательских интересов и усилий в вопросе определения требований к микроэлементам и улучшения оценки. нутритивного статуса в количественном и более точном прогностическом плане. Это приведет к значительным и значимым достижениям в области питания микроэлементами. Кроме того, тем из нас, кто интересуется этой областью, возможно, пора на некоторое время отступить и отказаться от немедленных попыток уточнить, например, текущие значения средних потребностей здоровых взрослых в меди и молибдене, которые составляют 700 и 34. мг/сут соответственно (37).Скорее, теперь может быть более продуктивным начать совместные исследования, предназначенные для получения более полной механистически основанной информации о реакции (характер экспрессии генов, активность метаболических путей, функции физиологических систем, например, связанные с иммунной и стрессоустойчивостью, микроэлементами). кинетика, например) к различным уровням потребления определенного микроэлемента в рамках данного генотипа/окружающей среды. Отсутствие надежных биологических данных о дозозависимой реакции характеризует большую часть базы знаний о потребностях человека в питательных веществах.Этого может быть чрезвычайно сложно достичь каким-либо всеобъемлющим образом, но я не вижу серьезной альтернативы или иного простого пути вперед. Кроме того, такие усилия позволили бы более четко сфокусировать и связать большую часть фундаментальной биологии с результатами более прикладных исследований, и это значительно расширило бы знания о пищевых аспектах микроэлементов в организме человека и животных. С этим новым знанием возникнет лучшее понимание механистической основы и степени вариации потребностей среди внешне похожих людей.Различия в абсорбции железа, на которые приходится большая часть различий в потребностях в железе у мужчин и женщин без менструаций, могут иметь генетическое происхождение и, возможно, быть связаны, по крайней мере частично, со специфическим геном, который кодирует цитохром В двенадцатиперстной кишки (40). , как я предполагал ранее (41). Суть в том, что сочетание генетических/клеточных исследований с исследованиями усвоения железа и его динамики в целом было бы ценным и захватывающим, а также проверило бы достоверность такой комплексной исследовательской структуры.
ТАБЛИЦА 2Некоторые подходы, используемые для оценки количественной потребности в микроэлементах 1
| Медь: СОД; плазма/тромбоциты Cu конц. |
| факториал: обязательная моча, фекалия, потери кожи и коэффициент поглощения Cu |
| цинковый: |
| Factorial Method (эндогенные потери по различным маршрутам; дробное поглощение Zn) |
| Утюг: |
| Факторный метод/базовые потери; увеличение массы гемоглобина; недепонирующие ткани/железо и менструальные потери вместе с биодоступностью железа |
| Медь: |
| Биохимические индикаторы: церулоплазмин; СОД; плазма/тромбоциты Cu конц. |
| факториал: обязательная моча, фекалия, потери кожи и коэффициент поглощения Cu |
| цинковый: |
| Factorial Method (эндогенные потери по различным маршрутам; дробное поглощение Zn) |
| Утюг: |
| Факторный метод/базовые потери; увеличение массы гемоглобина; Безопасные ткани / железо и менструальные потери, вместе с биодоступностью железа |
Некоторые подходы, используемые для оценки количественных требований для микроэлементов6 1
| Медь: |
| Биохимические показатели: церулоплазмин ; СОД; плазма/тромбоциты Cu конц. |
| факториал: обязательная моча, фекалия, потери кожи и коэффициент поглощения Cu |
| цинковый: |
| Factorial Method (эндогенные потери по различным маршрутам; дробное поглощение Zn) |
| Утюг: |
| Факторный метод/базовые потери; увеличение массы гемоглобина; недепонирующие ткани/железо и менструальные потери вместе с биодоступностью железа |
| Медь: |
| Биохимические индикаторы: церулоплазмин; СОД; плазма/тромбоциты Cu конц. |
| факториал: обязательная моча, фекалия, потери кожи и коэффициент поглощения Cu |
| цинковый: |
| Factorial Method (эндогенные потери по различным маршрутам; дробное поглощение Zn) |
| Утюг: |
| Факторный метод/базовые потери; увеличение массы гемоглобина; недепонирующие ткани/железо и менструальные потери вместе с биодоступностью железа |
На пути к большей интеграции и метаболомике биологии микроэлементов.
Для решения различных проблем, указанных выше, требуется, чтобы более серьезные исследовательские усилия были направлены на лучшее понимание связи между генотипом и фенотипом микроэлементов на уровне отдельных особей и популяций. Мало что известно о регуляции и функции большинства генов и/или о том, как они связаны с функцией и потребностью в микроэлементах. В этом контексте поучительна недавняя статья Стромана (42). Он указывает, используя аналогию Поланьи (43) с игрой в шахматы, что молекулярная биология сосредоточилась на деталях «ходов» (или управления), в значительной степени игнорируя стратегию или, в данном случае, динамические белковые сети, которые генерируют фенотип от генотипа.Важность понимания стратегии, с помощью которой клетка или организм реагируют на внешние сигналы, также подчеркивалась Voit (44). Строман (42) иллюстрирует свой аргумент, перечисляя различные биологические уровни, на которых происходит регуляция (Таблица 3), а в заголовке введения к серии статей, включающей статью Стромана (42), указано: «Дело не только в генах». Перефразируя Strohman (40), с этой точки зрения можно сделать вывод, что фенотипы болезней, связанных с питанием (микроэлементами), контролируются не только генами, но и законными самоорганизующимися сетями, которые демонстрируют общесистемную динамику.Они варьируются от метаболических до сигнальных путей, и при нарушении они изменяют выход вещества и энергии. Из этого следует, что необходимо изучать эти сети, включая метаболический контроль и метаболиты, если мы хотим получить новое представление о функции/статусе/заболевании людей, зависящих от следовых элементов. Фактически, в течение коротких периодов так называемого «пищевого» времени, таких как день или неделя, предположительно именно состояние этих метаболических и динамических сетей играет доминирующую роль в регуляции и функционировании клеток и органов; В этом контексте гены можно считать ответственными за более долгосрочные изменения фенотипа.
ТАБЛИЦА 3Уровни регуляции • локусы ограничений контроля • над геномом 1
| Уровни и переходы . | Динамическая система регулирования . |
|---|---|
| 1. От генома к транскриптому | Эпигенетическая регуляция экспрессии генов, включая пути, которые определяют уровни энергии (уровни окислительно-восстановительного потенциала) и подавляют транскрипцию ДНК при повышении уровня клеточного НАДН |
| 2.Транскриптом в протеом | Регуляторные ограничения, включая посттрансляционную модификацию белков |
| 3. Протеом в динамическую систему | Метаболические сети гликолиза и снижения митохондриального окисления являются динамическими системами, в настоящее время лучше всего изученными с точки зрения как механизма образования, так и принципов действия. Они демонстрируют контроль над всеми ферментами сети, а их фенотип включает клеточный окислительно-восстановительный потенциал |
| 4.Динамические системы для фенотипа | Контроль глобального фенотипа, такого как заболевание, может быть локализован в рамках одной регуляторной системы (метаболической, гормональной сигнализации и т. д.) или распределен по многим системам/уровням. |
| Уровни и переходы . | Динамическая система регулирования . |
|---|---|
| 1. От генома к транскриптому | Эпигенетическая регуляция экспрессии генов, включая пути, которые определяют уровни энергии (уровни окислительно-восстановительного потенциала) и подавляют транскрипцию ДНК при повышении уровня клеточного НАДН |
| 2.Транскриптом в протеом | Регуляторные ограничения, включая посттрансляционную модификацию белков |
| 3. Протеом в динамическую систему | Метаболические сети гликолиза и снижения митохондриального окисления являются динамическими системами, в настоящее время лучше всего изученными с точки зрения как механизма образования, так и принципов действия. Они демонстрируют контроль над всеми ферментами сети, а их фенотип включает клеточный окислительно-восстановительный потенциал |
| 4.Динамические системы для фенотипа | Контроль глобального фенотипа, такого как заболевание, может быть локализован в рамках одной регуляторной системы (метаболической, гормональной сигнализации и т. д.) или распределен по многим системам/уровням. |
Уровни регуляции • локусы контроля • над геномом 1
| Уровни и переходы . | Динамическая система регулирования . |
|---|---|
| 1.От генома к транскриптому | Эпигенетическая регуляция экспрессии генов, включая пути, определяющие уровни энергии (окислительно-восстановительные уровни) и подавляющие транскрипцию ДНК при повышении уровня клеточного NADH |
| 2. Транскриптом к протеому | белки |
| 3. Протеом в динамическую систему | Метаболические сети гликолиза и восстановления митохондриального окисления являются динамическими системами, которые в настоящее время лучше всего изучены с точки зрения как механизма образования, так и принципов действия.Они демонстрируют контроль над всеми ферментами сети, а их фенотип включает клеточный окислительно-восстановительный потенциал |
| 4. Динамические системы для фенотипа | и т. д.) или быть распределены по многим системам/уровням. |
| Уровни и переходы . | Динамическая система регулирования . |
|---|---|
| 1. От генома к транскриптому | Эпигенетическая регуляция экспрессии генов, включая пути, которые определяют уровни энергии (уровни окислительно-восстановительного потенциала) и подавляют транскрипцию ДНК при повышении уровня клеточного NADH |
| 2. Транскриптом | Регуляторные ограничения, включая посттрансляционную модификацию белков |
| 3. Протеом в динамическую систему | Метаболические сети гликолиза и восстановления митохондриального окисления являются динамическими системами, которые в настоящее время лучше всего изучены с точки зрения как механизма формирования, так и принципов работы.Они демонстрируют контроль над всеми ферментами сети, а их фенотип включает клеточный окислительно-восстановительный потенциал |
| 4. Динамические системы для фенотипа | и т. д.) или быть распределены по многим системам/уровням. |
Поэтому мы (41, 45–47) начали думать и исследовать способы оценки активности метаболических путей и сетей, зависящей от питательных веществ, и их связи с геномными, транскриптомными и протеомными локусами, такими как указанные в таблице 3.Общая или концептуальная основа подхода, который мы инициировали, проиллюстрирована на рисунке 1. Он включает в себя введение датчика или «метазонда», который при метаболизме высвобождает метаболит датчика, который затем можно обнаружить/измерить в моче, плазме и/или дыхание с использованием хорошо зарекомендовавших себя методов, таких как ELISA и масс-спектрометрия. Я считаю, что этот подход, в сочетании с более традиционными показателями статуса микроэлементов, предлагает новую и расширенную возможность для изучения динамической и функциональной связи между генотипом и фенотипом.Потребуется некоторое воображение относительно того, какой метаболический/физиологический путь можно исследовать и с помощью какого конкретного датчика; для меди это может быть датчиком катехоламинов или молибдена подходящим датчиком образования пуринов и катаболизма? Существует много возможностей для творческого интегративного мышления.
РИСУНОК 1
Каркас для динамического исследования метаболома. Датчик содержит метку высвобождения, которая под действием фермента в метаболическом пути высвобождает метку высвобождения.Это можно измерить в подходящем биологическом образце с помощью таких методов, как ELISA или масс-спектрометрия, в определенное время после введения сенсора (или метазонда). По материалам А. Аджами (личное сообщение).
РИСУНОК 1
Каркас для динамического исследования метаболома. Датчик содержит метку высвобождения, которая под действием фермента в метаболическом пути высвобождает метку высвобождения. Это можно измерить в подходящем биологическом образце с помощью таких методов, как ELISA или масс-спектрометрия, в определенное время после введения сенсора (или метазонда).По материалам А. Аджами (личное сообщение).
Возможно, было бы также полезно измерять концентрации метаболитов и множественных элементов в различных жидкостях организма. Например, как показано в таблице 4, измерение органических кислот, связанных с циклом Кребса, может быть полезным для оценки статуса железа (9) или определения уровней рибозы и дезоксирибозы в крови или клетках как показателей клеточного обмена и, возможно, поэтому статус цинка.
ТАБЛИЦА 4Возможные сигнатуры сенсора метаболитов функции/статуса микроэлементов
| Некоторые промежуточные метаболиты вместе с определениями микроэлементов для оценки метаболома |
| • Предшественники пуриновой и пиримидина и метаболиты |
| • Метаболиты мочевины |
| • PUFA и Hete Cascade (воспалительные) Продукты окисления |
| • Прочность на оксидант и антиоксидантность по отношению к уровням / функциям |
| • Рибоза и дезоксирибос как маркеры времени соторов сотора |
| Некоторые посреднические метаболиты вместе с определениями следовых элементов для оценки метаболома |
| • Органические кислоты в и вокруг циклов 60169 |
| • Предшественники пурина и пиримидина и метаболиты |
| • Метаболиты мочевины |
| • PUFA и Hete Cascade (воспалительное) Окисление Продукты |
| • Прочность окислителя и антиоксидантности по отношению к уровням / функциям / функциям |
| • Рибоза и дезоксирибоза как маркеры времени обновления клеток |
| • Органические кислоты в Krebs Cycles |
| • Предкуримы пуринового и пиримидина и метаболиты |
| • Метаболиты мочевины |
| • PUFA и Hete Cascade (воспаление) Окисление Продукты |
| • Прооксиданты и антиоксиданты Производительность Dant по отношению к уровням / функциям / функциям трассировки |
| • Рибоза и дезоксирибос как маркеры времени соторов соторов |
| Некоторые посреднические метаболиты вместе с определениями следования, для оценки метаболома |
| • Органические кислоты в циклах Krebs |
| • Предшественники пурина и пиримидина и метаболиты |
| • Метаболиты мочевины |
| • PUFA и Hete Cascade (воспалительное) окисление продукты |
| • Pro-окислитель и антиоксидантная способность по отношению к уровням/функциям микроэлементов |
| • Рибоза и дезоксирибоза как маркеры времени обновления клеток |
Кроме того, дополнительный подход к изучению метаболизма микроэлементов может включать измерения различных белков, особенно в ссылка на интим функциональные взаимосвязи между микроэлементами и множеством белков, которые были освещены в другом месте на этом симпозиуме.Например, существует множество белков, участвующих в функционировании и регуляции железа (48), меди (49) и цинка (25). Цинк является кофактором всех шести классов ферментов (25), включая матриксные металлопротеиназы (50, 51), и около 3% генов млекопитающих кодируют цинковые пальцы, которые опосредуют взаимодействия с ДНК и белок-белковые взаимодействия. Это открывает возможность для i ) проведения дифференциальных показов ферментов, когда можно измерить титр до 40–50 ферментов с помощью иммуноанализа и активность, измеренную с помощью флуоресцентных субстратов на легкодоступных матрицах, таких как кровь, слюна, моча, синовиальная жидкость, и/или ii ) разработка сигнатур ферментного сенсора, которые, например, оценивают воспалительную реакцию, где могут быть определены эктопептидазы лимфоцитов, и/или конвертазы, и ферменты апоптоза, и/или матрикс, и/или металлопротеазы.Вместе с информационными инструментами этот технологический и богатый данными подход может стать новой основой для изучения последствий измененного статуса и функции микроэлементов и для выявления лежащих в их основе механизмов.
Хотя все это требует разработки и тестирования, существует потенциально много новых проблем для метаболического фенотипирования и реальных возможностей для разработки и установления новых подходов и/или парадигм для характеристики метаболома, зависящего от микроэлементов. Таким образом, либо в настоящее время возможно, либо с некоторым дальнейшим развитием должно быть возможно: a ) исследовать компоненты метаболома со специфическими зависимыми от микроэлементов функциями, связанными с иммунной защитой, апоптозом и преобразованием энергии; b ) дополняет молекулярный, органелльный и другие редукционистские подходы существенно реконструктивными парадигмами; и c ) предоставляют информацию о потребностях в микроэлементах, их функциях и токсичности.Однако в настоящее время необходимы стратегические исследования для продвижения и улучшения этой структуры. Очень важно и, может быть, излишне подчеркивать важность этого исследования, но, как сказал Клод Бернар, «когда мы хотим приписать какому-либо физиологическому качеству его ценность и истинное значение, мы должны всегда соотносить его с его целым и обращать наше внимание». окончательные выводы только в отношении эффектов в целом».
Хотя наука о метаболизме питания находится в зачаточном состоянии, можно ожидать значительных успехов в развитии этой области.Короче говоря, разработка и эволюция технологий метаболического профилирования, включая масс-спектрометрию (52) и спектроскопию ядерного магнитного резонанса (53), в сочетании с достижениями в высокопроизводительных аналитических и вычислительных технологиях, произведут революцию в нашей способности открывать, как микроэлементы определяют питательные вещества. уровень и активность специфических генных продуктов и влияют на генетические пути. Особенно важной будет разработка общих методов, как это было сделано в молекулярной и клеточной биологии, для мониторинга многих сотен метаболитов, возможно, с помощью новых биосенсоров, таких как те, которые используют перенос энергии флуоресцентного резонанса (FRET) (54, 55).Кроме того, метаболомика проинформирует нас о том, как активность генов питательных микроэлементов интегрируется в мозаику глобальной активности генов. В отличие от генома и, как и протеома, метаболом не стабилен во времени. Таким образом, всестороннее изучение метаболомики требует, чтобы количественные динамические характеристики метаболома были определены и изучены в различных условиях и в определенное время с использованием множества методов, начиная от микрототальных аналитических систем (56) и индикаторных технологий (46) до метаболическая и функциональная визуализация (57–60), которая может предоставить анатомическое и поведенческое измерение для метаболической оценки пищевых реакций и потребностей в микроэлементах.Чтобы добиться полного успеха в этом контексте, потребуется разработка и сильная поддержка крупного междисциплинарного предприятия, что, на мой взгляд, и есть настоящая наука о питании.
Среди различных проблем, перечисленных ранее в Таблице 1, были способы улучшить потребление и баланс между микроэлементами и другими питательными веществами, чтобы повысить роль диеты в укреплении и поддержании здоровья. Недостаток места не позволяет подробно обсуждать эту тему, но я считаю, что потенциальный вклад сельскохозяйственной биотехнологии (61) особенно важен для улучшения питания людей микроэлементами.Для полного и эффективного использования этой технологии нам необходимы: i ) цель (критерий достаточности микроэлементов), ii ) информация о поступлении в организм отдельных лиц, iii ) информация о потребностях отдельных лиц, iv ) информация о факторы, влияющие на потребности, v ) информация о состоянии питания отдельных лиц, vi ) диетические характеристики (пищевые продукты, источники, приемы пищи), а также понимание социальных, культурных, экономических и политических детерминант благополучия.Большая часть этой информации зависит от успеха упомянутого выше типа исследовательской деятельности, с особым упором на системную биологию микроэлементов в организме человека и животных.
Многопрофильное предприятие для ТЕМА.
Мне становится ясно, когда мы рассматриваем связь генотипа с фенотипом через различные биологические уровни сложности, на которых микроэлементы проявляют свое влияние, нам предстоит столкнуться с многочисленными и разнообразными проблемами и решить их.Они связаны с исследованиями, их характером и институциональной структурой, в которой они проводятся; следует поощрять междисциплинарный подход, и это потребует инфраструктурных изменений в способах исследования науки, включая характер научного сотрудничества и необходимость приобретения новых навыков (ученые-биомедики в математике, статистике, кинетике) и т.д.
Что касается ценности междисциплинарного сотрудничества, я нахожу биологию и функцию бора интересным случаем; Недавно Совет Института медицины, пищевых продуктов и питания (IOM/FNB) (37) пришел к выводу, что до сих пор невозможно установить четкую биологическую функцию бора в организме человека.Тем не менее, недавно я узнал, что красное вино богато рамногалактуронаном II (RGII) (62). Это самый сложный полисахарид на Земле, он присутствует в клеточных стенках растений. Он состоит из 11 видов мономеров сахара и образует димеры через бор, что необходимо для роста растений. Кроме того, бор восстанавливает последствия дефекта содержания сшитого димера RGII у мутанта Arabidopsis, mur-1 (63). Поэтому можно задаться вопросом, какова связь между структурой углеводов клеточной поверхности у эукариот и доступностью/уровнями бора.Кроме того, если бор участвует в функции кальция (64, 65), должны ли мы исследовать отношения кальция и бора в мягких тканях с особым упором на отношения структура-функция.
Междисциплинарный подход также потребует духа сотрудничества как части процесса, необходимого для решения практических проблем питания микроэлементами. Такой дух поможет создать новые интересные междисциплинарные программы, в данном случае с упором на микроэлементы и правильное питание.Кроме того, теперь необходимо тщательно рассмотреть и переоценить характер обучения, предоставляемого грядущим поколениям выпускников и аспирантов в областях, имеющих отношение к цели ТЕМА. Это еще одна проблема, и ее нельзя недооценивать.
Код
В сущности, мне кажется, что для того, чтобы эта область двигалась вперед, мы должны быть менее замкнутыми как исследователи и даже более творческими как наставники. Всем участвующим сторонам, учителям, ученым, студентам и сторонникам необходимо понять и принять общие цели ТЕМА и мобилизовать необходимые интеллектуальные, физические и финансовые ресурсы.Позаимствовав идею у Брэдшоу (66), мне также кажется, что наука о микроэлементах и наука о питании в более широком смысле являются прекрасным примером «Слепых и слона». Это стихотворение американского поэта Джона Годфри Сакса (1816–1887), основанное на басне, рассказанной в Индии много лет назад, частично гласит:
Шесть человек из Индостана Намного наклон ,
Кто пошел посмотреть слон
(хотя все они были слепыми) ,
, что каждое из наблюдения
может удовлетворить его разум
и происходит на падение
против его широкой и крепкой стороне ,
сразу начали :
«Боже, благослови меня! Но Слон
Очень похож на стену!»
Первый приблизился к слоне ,
Второй , ощущение бивня ,
Кричал: «Хо! Что у нас здесь
Такой круглый, гладкий и острый?
Для меня это совершенно ясно
Это чудо Слона
Очень похоже на копье!
0- 7
Третий …… шестой …
и поэтому эти люди Indostan ,
Dispiled Druged и длинные ,
каждый в своем собственном мнение
Чрезвычайно жесткий и сильный ,
Хотя каждый был отчасти прав ,
9004 И все были неправы!
0- 7
Мораль
, так что OFT в богоротовых войнах ,
Disputants, I WEEN ,
Rail On в полном невежестве
О том, что друг друга значат
И болтают о Слоне
Ни один из них не видел!
Точно так же, как Брэдшоу (66) прокомментировал будущее журнала «Молекулярная и клеточная протеомика», редактором которого он был, похоже, что до тех пор, пока эти шесть слепых говорят и взаимодействуют мудро, слон будет в порядке. Заботился о.Достигая этого, наука о микроэлементах и питании будет эффективно развиваться на благо тех людей и групп населения, которые наиболее уязвимы к недостатку, избытку или дисбалансу микроэлементов. Будет интересно узнать, заслуживают ли какие-либо идеи, представленные здесь, или, возможно, даже место в организации и/или содержании ТЕМА 12, которая состоится примерно через три года в Колрейне, Северная Ирландия.
ЦИТИРОВАННАЯ ЛИТЕРАТУРА
1.Janbhorbani
,M.
&Young
,V. R.
(1980
)Использование стабильных изотопов для определения биодоступности минералов в рационе человека с использованием метода мониторинга фекалий
утра. Дж. Клин. Нутр.
33
:2021
–2030
.2.Джанбхорбани
,М.
,Тинг
,Б. Т. Г.
,Истфан
,С. В.
иЯнг
, В.R. (1981
)Измерение 68 Zn и 70 Zn в крови человека в связи с изучением метаболизма цинка
.утра. Дж. Клин. Нутр.
34
:581
–591
.3.Janghorbani
,M.
,Martin
,RF
,Kasper
,LJ
,Sun
,XF
&молодых
,VR
(1990
)Концепция селенитообменного метаболического пула у человека: новая концепция оценки статуса селена
.утра. Дж. Клин. Нутр.
33
:2021
–2030
.4.Young
VR
,VR
,LOLLEED
,GP
&LUICK
,JR
(1966
)Эффекты истощения фосфора и потребления кальция и фосфора, на эндогенную экскрецию этих элементы овцами
.руб. Дж. Нутр.
20
:795
–805
.5.Янг
,В.R.
,Luick
,J. R.
&Lofgreen
,G. P.
(1966
)Влияние потребления фосфора с пищей на скорость костного метаболизма у овец
руб. Дж. Нутр.
20
:727
–732
.6.Young
,VR
,Richards
,Richards
,WPC
,LOLLEEN
,GP
&LUICK
,JR
(1966
)Истопление фосфора в овцах и соотношении кальция до фосфора. в рационе с учетом усвоения кальция и фосфора
.руб. Дж. Нутр.
20
:783
–795
.7.Wachtershauser
,G.
(2000
)Происхождение жизни: жизнь, какой мы ее не знаем
.Наука
289
:1307
–1308
.8.CODY
,Г. Д.
,BOCTOR
,N. Z.
,N. Z.
,Filley
,T. R.
,Hazer
,R. M.
,SCOTT
,J.H.
,Sharma
,A.
&Yoder
,H. S.
, Jr. (2000
)Первичное карбонилирование соединений железа и серы и синтез 90 соединений железа и серы.
Наука
289
:1337
–1340
.9.Ross
,K. H.
&Eisenstein
,R. S.
(2002
)Дефицит железа снижает содержание митохондриальной аконитазы9 в три- и цитратном цикле крысы, не влияя на концентрацию митохондриальной аконитазы9 в трицикле и цитратном цикле.
Дж. Нутр.
132
:643
–651
.10.Walden
,WE
(2002
)От бактерий к митохондриям: аконитаза дает сюрпризы
.Проц. Натл. акад. науч. США
99
:4138
–4140
.11.Newman
,M.E.J.
(2001
)Структура сетей научного сотрудничества
.Проц. Натл. акад.науч. США
98
:404
–409
.12.Китано
,Х.
(2002
)Системная биология: краткий обзор
.Наука
295
:1662
–1664
.13.GIL
R
,R.
,Sabater-Munoz
,B.
,Latorre
,A.
,Silva
,FT
&MOYA
,A.
(2002
)Экстремальное сокращение генома у видов Buchnera .; к минимальному геному, необходимому для симбиотической жизни
.Проц. Натл. акад. науч. США
99
:4454
–4458
.14.Международный консорциум по секвенированию генома человека
(2001
)Первичное секвенирование и анализ генома человека
.Nature (London)
409
:860
–921
.15.Вентер
,Дж. К.
,Адамс
,М. Д.
,Майерс
,Э.W.
,LI
,PW
,PW
,,
,RJ
,Sutton
,GG
,Smith
,HO
,Yandell
,M.
,Evans
,КА
,Холт
,РА
,Gocayne
,J.D.
,Amanatides
,P.
и др. (2001
)Последовательность генома человека
.Наука
291
:1304
–1351
.16.Ю.
,Дж.
,Ху
,С.
,Ван
,Дж.
,Вонг
,Г.
,LI
,S.
,LIU
,B.
,DENG
,Y.
,DAI
,L.
,ZHOU
,Y.
,Чжан
,X.
,Cao
,M.
,Liu
,J.
, и др. (2002
)Черновая последовательность генома риса (Oryza sativa L.вид индика)
.Наука
296
:79
–92
.17.GOFF
,GOFF
,SA
,Ricke
,D.
,LAN
,TH
,Проставление
,G.
,Wang
,R
,Dunn
,м
,Glazebrook
,J.
,Sessions
,A.
,Oeller
,P.
,Varma
,,Hadley
,D.
иHutchison
,D.
(2002
)Черновая последовательность генома риса (Oryza sativa L. spp. 040 japonica)
Наука
296
:92
–100
.18.Аноним. (
2001
)Постгеномные культуры
.Nature (London)
409
:545
.19.Stortz
,G.
(2002
)Расширяющаяся вселенная некодирующих РНК
.Наука
296
:1260
–1263
.20.Деннис
,К.
(2002
)Дивный новый мир РНК
.Природа (Лондон)
418
:122
–124
.21.Riddihough
,G.
(2002
)Другой мир РНК
.Наука
296
:1259
.22.Донанжело
,С.M.
,Woodhouse
,LR
,King
,King
,SM
,Viteri
,Fe
&King
,JC
(2002
)Дополнительный цинк снижает меры статуса железа в молодые женщины с низкими запасами железа
.Дж. Нутр.
132
:1860
–1864
.23.Hess
,S. Y.
,Zimmermann
,M. B.
,Adou
,P.
,Torresani
,T.
&Hurrell
,R. F.
(2002
)Лечение дефицита железа у детей с зобом улучшает эффективность йодированной соли в Cô
утра. Дж. Клин. Нутр.
75
:743
–748
.24.Черный
,R.E.
иMiguel
,S.G.
(2001
)Новые роли цинка в питании, развитии и инфекционных заболеваниях младенцев: Часть 1
Нутр. Сегодня
36
:281
–290
.25.Каток
,L.
иGabriel
,P.
(2000
)Цинк и иммунная система
.Проц. Нутр. соц.
59
:541
–552
.26.Зеленый
,D.R.
иЧитать
,J.C.
(1998
)Митохондрии и апоптоз
.Наука
281
:1309
–1312
.27.Хенгартнер
,М. О.
(2000
)Биохимия апоптоза
.Nature (London)
407
:770
–776
.28.Clarke
,N.D.
иBerg
,JM
(1998
)Цинковые пальцы у Caenorhabditis elegans: поиск семейств и пути зондирования
Наука
282
:2018
–2022
.29.Лучи
,С.
(2001
)Три класса C 2 H 2 Цинковые пальчиковые ячейки
.Мол. Жизнь наук.
58
:625
–635
.30.Дреости
,J.E.
(2001
)Цинк и ген
.Мутация Рез.
475
:161
–167
.31.МакГлинн
,А. П.
,Уоссон
,Г.
,О’Коннор
,J.
,MCKERR
,G.
,McKelvey-Martin
,VJ
&Downes
,CS
(1999
): обнаружение созревания недавно реплицированной ДНК в отдельных клетках
.Рак Res.
59
:5912
–5916
.32.Касадеваль
,М.
иСакар
,Б.
(1998
)Влияние окислительно-восстановительных условий на эффективность связывания ДНК цинковым пальцем рецептора ретиноевой кислоты
.Дж. Неорг. Биохим.
71
:147
–152
.33.Hershfinkel
,M.
,M.
,MORAN
,A.
,Grossman
,N.
&Sekler
,J.
(2001
)рецептор цинкования высвобождение внутриклеточного Ca 2+ и регулирует транспорт ионов
.Проц. Натл. акад. науч.
98
:11749
–11754
.34.Maret
,W.
(2001
)Перекрестные помехи металлов группы 11a и 11b , кальций и цинк в сигнализации
.Проц. Натл. акад. науч. США
98
:12325
–12327
.35.Пирс
,Л. Л.
,Грандли
,Р. Е.
,Хан
,В.
,Вассерлоос
,,STITT
,M.
,Kanai
,AJ
,McLaughlin
,MK
,Pitt
,BR
&Leviton
,ES
(2000
)металлотионеина в передаче сигналов оксида азота, как показано зеленым флуоресцентным слитым белком
.Проц. Натл. акад. науч.
97
:477
–482
.36.О’Делл
,Б.L.
(2000
)Роль цинка в функционировании плазматической мембраны
.Дж. Нутр.
130
:14325
–14365
.37.Институт медицины/Совет по пищевым продуктам и питанию
(2001
)Справочные нормы потребления витамина А, витамина К, мышьяка, бора, хрома, меди, йода, железа, марганца, молибдена, никеля, кремния, ванадия и Цинк
.National Academy Press
,Вашингтон, округ Колумбия
.38.Институт медицины/Совет по пищевым продуктам и питанию
(2000
)Справочное потребление рациона: Применение оценки рациона питания
.National Academy Press
,Вашингтон, округ Колумбия
.39.Baker
,D.H.
(1986
)Проблемы и ловушки в экспериментах на животных, направленных на установление диетических потребностей в основных питательных веществах
.Дж. Нутр.
116
:2339
–2349
.40.Mckie
,по
,Барроу
,D.
,Latunde-Dada
,GO
,ROLFS
,A.
,Sager
,G.
,Mudaly
,E.
,E.
,Mudaly
,M.
,Richardson
,C.
,Barlow
,D.
,Bomford
,A.
,Peters
,TJ
,Раджа
,К.B.
,Shirali
,Shirali
,S.
,HEDIGER
,MA
,Farzaneh
,F.
&SIMPSON
,RJ
(2001
)Железная редуктаза связано с усвоением пищевого железа
.Наука
291
:1755
–1759
.41.Янг
,В.Р.
(2002
)2001 В.О. Мемориальная лекция Этуотера и лекция президента ASNS 2001 года: Потребности человека в питательных веществах: вызов постгеномной эры
.Дж. Нутр.
132
:621
–629
.42.Strohman
,R.
(2002
)Маневрирование на сложном пути от генотипа к фенотипу
.Наука
296
:701
–703
.43.Поланьи
,М.
(1968
)Непреодолимая структура жизни. Живые механизмы и информация в ДНК являются граничными условиями с последовательностью границ над ними
.Наука
160
:1308
–1312
.44.Voit
,EO
(2002
)Метаболическое моделирование как инструмент открытия лекарств в постгеномную эру
.Препарат Дисков. Сегодня
7
:621
–628
.45.Young
,VR
иAjami
,AM
(1999
)1999 Лекция Джонатана Э. Роадса. Изотопные метазонды, питание и перспективы
.Дж. Парентер. Энтеральный нутр.
23
:175
–194
.46.Young
,V. R.
,V. R.
,Borgonha
,S.
&AJAMI
,A. M.
(2000
)Тенденции в техниках трассера, включая использование позитронной эмиссионной томографии
.Диабет Нутр. Метаб.
13
:35
–45
.47.Янг
,В. Р.
иАджами
,А.М.
(2001
)Обмен веществ 2000: императору нужна новая одежда
.Проц. Нутр. соц.
60
:27
–44
.48.Burke
,W.
,Imperatore
,G.
&Reyes
,М.
(2000
)Дефицит железа и железная перегрузка: эффекты диеты и генов
.Проц. Нутр. соц.
60
:73
–80
.49.Эндрюс
,N.C.
(2001
)Транспортные гены добычи меди
.Проц. Натл. акад. науч.
98
:6543
–6545
.50.Coussens
,
Л. М.
,Л. Кынкол
,B.
&Матризиан
,Л. М.
(2000
)Матрица Металлопротеиназы Ингибиторы и рак: испытания и невца
.Наука
295
:2387
–2392
.51.McCawley
,L. T.
&Matrisian
,L. M.
(2001
)Матриксные металлопротеиназы: они больше не только для матрикса! Курс
.Заключение. Клеточная биол.
13
:534
–540
.52.Roesner
,V.
,V.
,Wagner
,C.
,KOPKA
,J.
,Trithwey
,R. N.
иWillmitzer
,L.
(2000
)Одновременный анализ метаболитов в клубнях картофеля методом газовой хроматографии-масс-спектрометрии
.Завод J.
23
:131
–142
.53.Lindon
,JC
,JC
,Nicholson
,JK
,Holmes
,E.
&Everett
иJR
(2000
)Метабонамика: метаболические процессы, изученные ЯМР-спектроскопией биоплеидов.
.Концепты Magn. Резон.
12
:289
–320
.54.Stitt
,M.
(2002
)Визуализация метаболитов с использованием слитого белка между периплазматическим связывающим белком и производными GFP. От химеры к взгляду на реальность
.Проц. Натл. акад. науч. США
99
:9614
–9616
.55.Фер
,М.
,Фроммер
,Вт.B.
иLalonde
,S.
(2002
)Визуализация поглощения мальтозы живыми дрожжевыми клетками с помощью флуоресцентных наносенсоров
.Проц. Натл. акад. науч. США
99
:9846
–9851
.56.Roberts
,M.
,Geiger
,W.
&немецкий
,J. B.
,J. B.
(2000
)Революция в микроаналитической химии: макросъемка для клинического питания
.утра. Дж. Клин. Нутр.
71
:434
–437
.57.Phelps
,ME
(2000
)Позитронно-эмиссионная томография обеспечивает молекулярную визуализацию биологических процессов
.Проц. Натл. акад. науч. США
97
:9226
–9233
.58.Лесли
,Р. А.
иДжеймс
,М. Ф.
(2000
)Фармакологическая магнитно-резонансная томография: новое приложение для функциональной МРТ
.Trends Pharmacol. науч.
21
:314
–318
.59.Shulman
,R.G.
иRothman
,DL
(1998
)Интерпретация исследований функциональной визуализации с точки зрения циклов нейротрансмиттеров
.Проц. Натл. акад. науч. США
95
:11993
–11998
.60.Weissleder
,R.
иMahmood
,U.
(2001
)Молекулярная визуализация
.Радиология
219
:316
–333
.61.Bouis
,H.E.
(2000
)Улучшение питания человека с помощью сельского хозяйства: роль международных сельскохозяйственных исследований. Итоги конференции и рекомендации
.Пищевые питательные вещества. Бык
21
:550
–567
.62.Хофте
,Х.
(2001
)Барочный остаток в красном вине
.Наука
294
:795
–797
.63.O’NEILL
,MA
,Eberhard
,Eberhard
,S.
,ALBERSHEIM
,P.
&DARVILL
,AG
(2001
)Требование бората рамногалактуронан II клеточной стенки для роста Arabidopsis
.Наука
294
:846
–849
.64.Nielsen
Nielsen
,FH
,Hunt
,CD
,Mullen
,LM
&Hunt
,JR
(1987
)Эффект диетического бора на минерал, эстроген, и метаболизм тестостерона у женщин в постменопаузе
.FASEB J.
1
:394
–397
.65.Nielsen
,F. H.
(1996
)Доказательства пищевой ценности бора.J. Микроэлементы Exp
.Мед.
9
:215
–229
.66.Бардшоу
,Р. А.
(2002
)Протеомика – бум или крах?
Молекулярная и клеточная протеомика
1
:177
–178
.© 2003 Американское общество наук о питании
(PDF) Основные микроэлементы и их жизненно важная роль в организме человека
Indian Journal of Advances in Chemical Science 5(3) (2017) 127-136
134
38.LE Murray-Kolbe, J. Beard, (2010) Iron.
В: PM Coates, JM Betz, MR Blackman,
GM Cragg, M. Levine, J. Moss, JD White,
(Ed.), Encyclopedia of Dietary Supplements, 2nd
ed. Лондон и Нью-Йорк: Informa Healthcare,
, стр. 432-438.
39. R. Casiday, F. Regina, (2007) Использование железа и
Хранение в организме: ферритин и молекулярные
Представительства, Сент-Луис, США: Кафедра химии
, Вашингтонский университет.
40. R. C. Hider, X. Kong, (2013) Iron: Effect of
перегрузки и дефицита. В: А. Сигель, Х. Сигель,
Р. К. О. Сигель, (ред.), Взаимосвязь между
важнейшими ионами металлов и болезнями человека,
Ионы металлов в науках о жизни, Vol. 13. Гл. 8.
Дордрехт: Springer, стр. 229-294.
41. Всемирная организация здравоохранения, (2008 г.) Worldwide
Распространенность анемии, 1993–2005 гг.: ВОЗ
Глобальная база данных по анемии, Женева: Всемирная организация здравоохранения
.
42. Э. С. Винтергерст, С. Маггини, Д. Х. Хорниг,
(2007) Вклад отдельных витаминов и
микроэлементов в иммунную функцию, Annals of
Nutrition and Metabolism, 51(4): 301-323.
43. SR D’Souza, A. George, (2007) Беспокойные ноги
синдром у индийских пациентов с дефицитом железа
анемия в больнице третичного уровня, Sleep Medicine,
8(3): 247- 251.
44. Ф.С. Аль-Фартуси, А.T. Marzook, TS Morad,
(2012) Исследование некоторых микроэлементов и
витаминов-антиоксидантов в сыворотке иракских женщин с токсоплазмозом
, Al-Mustansiriyah Journal of
Science, 23(3): 199-206.
45. Дж. Эмсли, (2001) Марганец. Nature’s Building
Blocks: A-Z Guide to the Elements, Oxford,
UK: Oxford University Press, стр. 249-253.
46. C. E. Housecroft, AG Sharpe, (2008) Неорганическая
Химия, 3-е изд.Харлоу: Прентис Холл,
, стр. 305-306.
47. IOM (Институт медицины), (1997) диетическое
справочное потребление: кальций, фосфор,
магний, витамин D и фторид. Еда и
Совет по питанию, Вашингтон, округ Колумбия: National
Academy Press.
48. Р. К. Руде, (2010) Магний. В:
P. M. Coates, JM Betz, M. R. Blackman,
G. M. Cragg, M. Levine, J. Moss, JD White,
(Ed.), Энциклопедия пищевых добавок, 2-е изд.
. Нью-Йорк, штат Нью-Йорк: Informa Healthcare, стр. 527–537.
49. Р. К. Руде, (2012) Магний. В: AC
Ross, B. Caballero, RJ Cousins, KL
Tucker, T.R. Ziegler, (Ed.), Modern Nutrition
in Health and Disease, 11th ed. Балтимор, Массачусетс:
Lippincott Williams & Wilkins, стр. 159-175.
50. М. П. Романи, (2013) Магний в здоровье и
болезни. В.Sigel, H. Sigel, RKO Sigel, (Ed.),
Взаимосвязи между ионами основных металлов и
Заболевания человека, Ионы металлов в науках о жизни,
Vol. 13. Гл. 3. Дордрехт: Springer, стр. 49-79.
51. Л. Г. Эбботт, Р. К. Руд, (1992) Клинические
проявления дефицита магния, Минерал
и метаболизм электролитов, 19(4-5): 314-322.
52. Министерство сельского хозяйства США, Сельскохозяйственная исследовательская служба
, (2012) Национальная база данных по питательным веществам USDA
для стандартной справочной информации, выпуск 25,
США: Лаборатория данных о питательных веществах, Белтсвилл, человек
Исследовательский центр питания, USDA-ARS .
53. П. А. Сарафидис, П. И. Джорджианос, А. Н. Ласаридис,
(2010) Диуретики в клинической практике. Часть II:
Электролитные и кислотно-щелочные расстройства, осложняющие
мочегонную терапию, Экспертное заключение о безопасности лекарственных средств,
9(2): 259-273.
54. R.K.Rude, M.E.Shils, (2006) Magnesium. В:
М. Э. Шилс, М. Шике, А. К. Росс, Б. Кабальеро,
Р. Дж. Казинс, (ред.), Современное питание в области здравоохранения
и болезни, 10-е изд.Балтимор: Lippincott
Williams & Wilkins, стр. 223-247.
55. SC Larsson, MJ Virtanen, M. Mars,
S. Männistö, P. Pietinen, D. Albanes, J. Virtamo,
(2008) Магний, кальций, калий и
потребление натрия и риск инсульта у курящих мужчин,
Archives of Internal Medicine, 168(5): 459-465.
56. С. М. Кобрин, С. Гольдфарб, (1990) Дефицит магния
, Семинары по нефрологии, 10(6):
525-535.
57. H. Geiger, C. Wanner, (2012) Магний при
заболеваниях, Clinical Kidney Journal, 5: 25-38.
58. Д. П. Чаудхари, Р. Шарма, Д. Д. Бансал,
(2010) Последствия дефицита магния
при диабете 2 типа: обзор, Biological Trace
Element Research, 134: 119-129.
59. Э. Ранке-Мадсен, (1975) Открытие элемента
, Centaurus, 19(4): 299-313.
60. C. Palacios, (2006) Роль питательных веществ в здоровье костей
, от А до Я, Critical Reviews in Food
Science and Nutrition, 46(8): 621-628.
61. К. Г. Фрага, (2005) Актуальность, эссенциальность
и токсичность микроэлементов для здоровья человека,
Молекулярные аспекты медицины, 26(4): 235-244.
62. Д. Сильва, П. Р. Луис, М. Ашнер, (2013)
Марганец в норме и болезни. В: A. Sigel,
H. Sigel, R.K.O. Sigel, (Ed.), Взаимосвязи
между основными ионами металлов и болезнями человека
, Ионы металлов в науках о жизни, Vol. 13.
Гл.7. Дордрехт: Springer, стр. 199-227.
63. C. Henn, AS Ettinger, J. Schwartz, M. M Téllez-
Rojo, H. Lamadrid-Figueroa, M. Hernández-Avila,
L. Schnaas, C. Amarasiriwardena, DC Bellinger,
H. Hu, RO Wright, (2010) Ранняя постнатальная кровь
Уровни марганца и развитие нервной системы у детей,
Epidemiology, 21(4): 433-439.
64. Н. Трейбер, П. Майти, К. Сингх, Ф. Флорентина,
В. Мейнхард, К.Scharffetter-Kochanek, (2012)
Роль супероксиддисмутазы марганца в старении кожи, Дерматоэндокринология, 4: 232-235.
65. N. Law, M. Caudle, V. Pecoraro, (1998)
Окислительно-восстановительные ферменты марганца и модельные системы:
Свойства, структуры и реакционная способность, Достижения в
Произошла ошибка при настройке файла cookie пользователя
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка браузера на прием файлов cookie
Существует множество причин, по которым файл cookie не может быть установлен правильно. Ниже приведены наиболее распространенные причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
- Ваш браузер не поддерживает файлы cookie. Попробуйте другой браузер, если вы подозреваете это.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Предоставить доступ без файлов cookie потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в файле cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только та информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, если вы не решите ввести его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступ к остальной части вашего компьютера, и только сайт, создавший файл cookie, может его прочитать.
Пищевые аспекты незаменимых микроэлементов при заболеваниях и здоровье полости рта: подробный обзор
Человеческому организму требуются определенные незаменимые элементы в небольших количествах, и их отсутствие или избыток может привести к серьезным нарушениям в работе организма и даже к смерти в крайних случаях, потому что эти незаменимые микроэлементы элементы непосредственно влияют на метаболические и физиологические процессы организма.Быстрая урбанизация и экономическое развитие привели к резким изменениям в рационе питания с развитием предпочтения в сторону изысканной диеты и нездоровой пищи, лишенной питательных веществ. Плохое питание может привести к снижению иммунитета, повышенной уязвимости к различным оральным и системным заболеваниям, нарушению физического и умственного развития и снижению работоспособности. Диета и питание по-разному влияют на здоровье полости рта, в том числе на черепно-лицевое развитие, рост и поддержание мягких тканей зубов и полости рта.Потенциально злокачественные заболевания полости рта (OPMD) лечат антиоксидантами, содержащими незаменимые микроэлементы, такие как селен, но даже повышенное потребление таких микроэлементов, как медь, может привести к подслизистому фиброзу полости рта. Дефицит или избыток других микроэлементов, таких как йод, железо, цинк и т. д., оказывает глубокое воздействие на организм, и такие состояния часто диагностируются по их ранним проявлениям в полости рта. В этом обзоре оцениваются биологические функции значимых микроэлементов и их роль в сохранении здоровья полости рта и прогрессировании различных заболеваний полости рта.
1. Введение
Правильное питание всех метаболически активных клеток и тканей необходимо для сохранения здоровья человеческого организма в целом. Микронутриенты, включая микроэлементы, витамины и антиоксиданты, играют жизненно важную роль в непрерывно протекающих регенеративных процессах, справляясь с продолжающимся окислительным стрессом в тканях организма и поддерживая достаточный иммунитет против патогенов [1, 2]. Проявления недостаточности питания, а также избыточного питания микронутриентами на здоровье полости рта обширны и могут приводить к дефектам твердых тканей зубов, а также слизистой оболочки полости рта [3, 4].
Под словом «микроэлементы» понимаются элементы, находящиеся в естественных и нарушенных средах в малых количествах, с избыточной биодоступностью, оказывающие токсическое действие на живой организм [5]. Микроэлементы представляют собой химические микронутриенты, которые требуются в довольно незначительных количествах, но играют жизненно важную роль в поддержании целостности различных физиологических и метаболических процессов, происходящих в живых тканях. Дефицит любого из микроэлементов может проявляться как сочетание различных клинических проявлений, а не как специфическая картина, поскольку каждый микроэлемент связан со многими ферментными системами.
Здоровое питание с регулярным приемом основных витаминов и минералов имеет огромное значение для общего здоровья и здоровья полости рта. Поскольку у врачей-стоматологов были ограниченные знания о значении микроэлементов в питании человека, текущий обзор сосредоточен на роли тех основных микроэлементов, которые имеют доказанную роль в поддержании здоровья полости рта и их влиянии на различные заболевания и расстройства полости рта.
2. Классификация микроэлементов
Предпринимались ограниченные попытки классификации исключительно микроэлементов.Перечислены классификации, учитывающие наличие микроэлементов.
2.1. Классификация ВОЗ, 1973 г. [6]
В соответствии с этой классификацией девятнадцать микроэлементов были разделены на три группы: (1) Эссенциальные элементы: цинк (Zn), медь (Cu), селен (Se), хром (Cr), кобальт (Co), йод (I), марганец (Mn) и молибден (Mo). (2) Вероятно, незаменимые элементы. (3) Потенциально токсичные элементы.
2.2. Классификация элементов Фридена
В 1981 году Фриден предложил биологическую классификацию микроэлементов, основанную на их количестве в тканях [7]: (1) Основные микроэлементы: бор, кобальт, медь, йод, железо, марганец, молибден и цинк. .(2) Вероятно, незаменимые микроэлементы: хром, фтор, никель, селен и ванадий. (3) Физически активные микроэлементы: бром, литий, кремний, олово и титан.
2.3. Категориальная классификация элементов Фридена [8]
Двадцать девять типов элементов, присутствующих в организме человека, были классифицированы в пять основных групп следующим образом: (i) Группа I: основные компоненты макромолекул, такие как углеводы, белки и липиды. Примеры включают углерод, водород, кислород и азот.(ii) Группа II: важные с точки зрения питания минералы, также называемые основными или макроэлементами. Суточная потребность в этих макроэлементах для взрослого человека составляет более 100 мг/сут. Примеры включают натрий, калий, хлорид, кальций, фосфор, магний и серу. (iii) Группа III: основные микроэлементы. Микроэлементы также называют второстепенными элементами. Элемент считается микроэлементом, если его потребность в день ниже 100 мг. Дефицит этих элементов встречается редко, но может оказаться фатальным.Примеры включают медь, железо, цинк, хром, кобальт, йод, молибден и селен. (iv) Группа IV: дополнительные микроэлементы. Их роль пока неясна, и они могут быть существенными. Примеры включают кадмий, никель, кремнезем, олово, ванадий и алюминий. Эта группа может быть эквивалентна эссенциальным микроэлементам в классификации ВОЗ. (v) Группа V: эти металлы не являются эссенциальными, и их функции неизвестны. Они могут вызывать токсичность в избыточных количествах. Примеры включают золото, ртуть и свинец.Эта группа эквивалентна потенциально токсичным элементам, определенным в классификации ВОЗ.
3. Обсуждение
В организме человека функционирует разветвленная и сложная система, которая управляет и поддерживает количество необходимых микроэлементов в пределах нормы. Микронутриенты из рациона транспортируются в кровь при их дефиците, проникают в клетки, если клеточные уровни недостаточны, или выводятся из организма, если уровни в крови и клетках удовлетворительны или повышены. Различные основные микроэлементы, а также требования к питанию и источники питания перечислены в таблице 1.
3.1. МедьМедь является третьим по распространенности микроэлементом, ее общее количество в организме человека составляет всего 75–100 мг [9]. Медь присутствует почти во всех тканях организма и хранится в основном в печени, а также в головном мозге, сердце, почках и мышцах [10]. Медь всасывается в кишечнике и транспортируется в печень. В крови человека медь преимущественно распределяется между эритроцитами и плазмой [11]. Он транспортируется в виде церулоплазмина в плазму, где его метаболизм контролируется, и выводится с желчью [12].Церулоплазмин составляет 90% содержания меди в крови и отвечает за перенос меди к клеткам с дефицитом [13]. Медно-цинковый металлофермент супероксиддисмутаза содержит 60% меди в эритроцитах, а остальные 40% слабо связаны с другими белками и аминокислотами. 3.1.1. Биологические функцииЗначительное количество метаболических ферментов правильно функционирует благодаря меди [13–16]. Перечислены биологические функции меди [14–16]: (1) Фермент цитохром-с-оксидаза, включающий медь и железо, играет жизненно важную роль в выработке энергии во время аэробного дыхания.(2) Медь также присутствует в супероксиддисмутазе, которая обезвреживает супероксиды, превращая их в кислород и перекись водорода. (3) Медь также является компонентом лизилоксидазы, которая принимает участие в синтезе коллагена и эластина. Медь также необходима для поддержания прочности кожи, волос, кровеносных сосудов, эпителиальных и соединительных тканей по всему телу. (4) Cu играет значительную роль в производстве гемоглобина. Церулоплазмин катализирует окисление железа, которое впоследствии необходимо для связывания с его транспортным белком трансферрином [12].(5) Производство меланина: медьсодержащий фермент тирозиназа превращает тирозин в меланин. (6) Производство миелина: Cu также необходима для синтеза фосфолипидов, находящихся в миелиновых оболочках периферических нервов [13, 16]. (7) Медь также необходима. для производства гормона щитовидной железы тироксина [13]. (8) Медь может действовать как антиоксидант и прооксидант. В качестве антиоксиданта Cu поглощает или нейтрализует свободные радикалы и может уменьшить или помочь предотвратить некоторые повреждения, которые они вызывают [16–19]. Медь способствует повреждению тканей свободными радикалами, когда действует как прооксидант [20]. 3.1.2. Роль в здоровье и заболеваниях полости ртаСимптомами дефицита меди являются гипохромная анемия, нейтропения, гипопигментация волос и кожи, аномальное формирование костей с хрупкостью скелета и остеопорозом, боль в суставах, снижение иммунитета, сосудистые аберрации и курчавые волосы [21]: (1) Дефицит Cu в рационе в течение длительного периода, особенно на стадиях активного роста, приводит к анемии и нарушению ороговения в ротовой полости [22]. Анемический эффект объясняется снижением ферроксидазной активности церулоплазмина и снижением окисления железа [5].(2) Инфекции: снижение иммунитета может привести к различным инфекциям полости рта, сопровождающимся нейтропенией [23]. Были отмечены нарушения созревания гранулоцитов в костном мозге и вакуолизация нейтрофилов [5]. (3) Аномалии костей и боль: изменения костей при дефиците меди включают потерю трабекулярного образования с истончением коры. Может быть остеопороз и образование затылочных рогов из-за функционального нарушения ферментов, требующих меди, таких как аскорбатоксидаза и лизилоксидаза в случае дефицита меди [10].(4) Оральные поражения: различные исследования показали, что средние уровни меди в сыворотке были значительно выше в сыворотке пациентов с потенциально злокачественными заболеваниями полости рта, такими как лейкоплакия полости рта и подслизистый фиброз полости рта, а также со злокачественными опухолями, такими как плоскоклеточный рак. Среднее потребление меди в Индии составляет 2,1-3,9 мг/день, тогда как из-за жевания орехов арека оно превышает 5 мг/день. Было высказано предположение, что медь, выделяемая из орехов ареки при жевании, вступала в непосредственный контакт с эпителием ротовой полости и растворялась в слюне.Сообщается, что медь присутствует в слюне в течение 30 минут. Чем дольше медь находится в слюне, тем выше вероятность ее поглощения эпителием полости рта [24]. Утверждается, что медь появляется в крови через 15 минут после употребления ореха арека и продуктов его переработки [25]. У пациентов с подслизистым фиброзом полости рта уровни Cu в сыворотке постепенно увеличиваются по мере прогрессирования клинической стадии заболевания. Однако местный эффект повышенного содержания меди в слюне может играть более важную роль, чем повышенный уровень меди в сыворотке.Другие школы оценивают снижение концентрации меди в сыворотке крови из-за использования меди для активизации лизилоксидазы, что приводит к чрезмерному перекрестному связыванию коллагена [26]. (5) Считается, что медь также обладает свойством, способствующим развитию кариеса [27]. 3.2. ЦинкВ организме человека распределено 2–4 грамма цинка [28]. Цинк хранится в предстательной железе, частях глаза, головном мозге, мышцах, костях, почках и печени [29]. Это второй наиболее распространенный переходный металл в организмах после железа и единственный металл, который присутствует во всех классах ферментов [28, 30].В плазме крови Zn связывается и транспортируется альбумином (60%) и трансферрином (10%) [31]. Поскольку трансферрин также транспортирует железо, избыток железа может снижать абсорбцию цинка и наоборот [32]. Концентрация цинка в плазме крови остается относительно постоянной независимо от приема цинка. 3.2.1. Биологические функцииФункции цинка в биологии многочисленны, но их можно разделить на три основные категории: каталитические, регуляторные и структурные роли. Он необходим для каталитической активности большого числа ферментов [33, 34].Он играет важную роль в иммунной функции, заживлении ран, синтезе белка, синтезе ДНК и делении клеток [34–36]. Цинк необходим для правильного восприятия вкуса и запаха [37, 38]. Он также поддерживает нормальный рост и развитие во время беременности, детства и подросткового возраста [39–42]. Предположительно, он также обладает антиоксидантными свойствами и, таким образом, может играть роль в ускорении процесса заживления после травмы и защите от ускоренного старения [40, 43]. Ионы цинка являются эффективными антимикробными агентами даже при низких концентрациях. 3.2.2. Роль в здоровье и заболеваниях полости ртаРоль цинка в здоровье и заболеваниях полости рта резюмируется следующим образом: (1) В полости рта цинк естественным образом присутствует в зубном налете, слюне и эмали. Цинк превращается в продукты для ухода за полостью рта, чтобы контролировать зубной налет, уменьшать неприятный запах и замедлять образование зубного камня. Повышенные концентрации цинка могут сохраняться в зубном налете и слюне в течение длительного времени после приема ополаскивателей для полости рта и зубных паст. Хотя низкие концентрации цинка могут как снижать деминерализацию эмали, так и модифицировать реминерализацию, антикариозная эффективность остается спорной и не подтверждается различными исследованиями [44].(2) Нарушения вкуса: роль цинка во вкусовых функциях заметна на различных уровнях организации, таких как вкусовые рецепторы, нервная передача вкусовых ощущений и мозг. Цинк играет важную роль в архитектуре клеточной структуры, поддерживая целостность клеточной мембраны и функции различных цитоплазматических и мембранных ферментов. Ранние исследователи пришли к выводу, что дефицит цинка, вторичный по любой этиологии, приводит к нарушениям вкуса, и, таким образом, истощение цинка корректируется у пациентов, сообщающих о дисбалансе вкуса [45].(3) Исследование, проведенное на грызунах, показало, что диета с дефицитом цинка может привести к паракератозу обычно ортокератинизированной слизистой оболочки полости рта. Следовательно, дефицит цинка может быть потенциальным фактором риска заболеваний полости рта и пародонта. Паракератотические изменения на щеках, языке и пищеводе являются признаком дефицита цинка. Утолщение слизистой оболочки щек является распространенным проявлением наряду с потерей нитевидных сосочков [46]. (4) Как указано выше, цинк является кофактором для фермента супероксиддисмутазы, и различные исследования показали более низкие уровни цинка в сыворотке у пациентов с потенциально предраковыми заболеваниями. как лейкоплакия полости рта.Это может быть связано с потреблением цинка в ответ на высокое содержание меди в орехе арека или оксиданты, высвобождаемые при употреблении табака [47]. (5) Точно так же концентрация цинка в сыворотке значительно снижается при плоскоклеточном раке полости рта и подслизистом раке полости рта. фиброз у пациентов с историей употребления табака по сравнению с контрольной группой и постепенно уменьшался с увеличением продолжительности привычки. Сообщалось, что уровень цинка в сыворотке был ниже у пациентов с плоскоклеточным раком полости рта, чем у пациентов с подслизистым фиброзом полости рта [25, 48].(6) Поскольку трансферрин переносит как железо, так и цинк, уровень цинка увеличивается по мере снижения уровня железа у пациентов с дефицитом железа. Так, у пациентов с ОСМФ, также страдающих железодефицитной анемией, отмечается более высокий уровень цинка в сыворотке крови [25, 48]. (7)Супероксиддисмутаза, являющаяся естественным антиоксидантом организма, представляет собой белковый комплекс Cu-Zn, обладающий антиканцерогенным действием при ОСМФ. . Во-вторых, цинк снижает активность медьсодержащего фермента лизилоксидазы и, таким образом, вызывает ингибирование перекрестного связывания коллагеновых пептидов.Он также играет важную роль в содействии деградации коллагена посредством коллагеназы и металлопротеиназы матрикса. Таким образом, цинк находится в обратной зависимости от меди и тем самым препятствует всасыванию меди слизистой оболочкой. Избыток цинка особенно ухудшает всасывание меди, так как оба металла всасываются через металлотионеины. Соотношение меди и цинка также считается надежным биомаркером развития и прогрессирования канцерогенеза [48]. (8) Вопреки распространенному мнению о защитной функции цинка, ограниченное количество литературы предполагает канцерогенный эффект цинка [49]. ]. 3.3. ЖелезоЖелезо является наиболее распространенным незаменимым микроэлементом в организме человека. Общее содержание железа в организме составляет около 3-5 г, причем большая его часть находится в крови, а остальная часть в печени, костном мозге и мышцах в виде гема [50]. Железо всасывается в кишечнике из пищи в случае истощения и транспортируется в виде ферритина. Гемосидерин представляет собой пигмент золотисто-коричневого цвета, который является побочным продуктом метаболизма ферритина и откладывается в клетках ретикулоэндотелиальной системы [51].Гомеостаз железа поддерживает уровень железа в сыворотке в пределах нормы только за счет повышения или понижения механизма абсорбции железа, который уникален тем, что поддерживает гомеостаз, регулируя абсорбцию, а не экскрецию. 3.3.1. Биологические функцииГем является основным железосодержащим веществом в двухвалентном или трехвалентном состоянии, которое присутствует в гемоглобине, миоглобине и цитохроме. С железом связаны многочисленные ферменты, а именно цитохром а-с, р450, цитохром с-редуктаза, каталазы, пероксидазы, ксантиноксидазы, триптофанпирролаза, сукцинатдегидрогеназа, глюкозо-6-фосфатдегидрогеназа и холиндегидрогеназа.Гем образует ковалентные связи с глобиновым белком с образованием гемоглобина, который является основным переносящим кислород пигментом в эритроцитах млекопитающих. Он принимает участие во множестве метаболических циклов, например, в реакциях выработки энергии (цитохромы цикла Кребса) во всех клетках и активирует вырабатывающие энергию окислительные ферменты. Помимо участия в поддержании бесчисленных физиологических и метаболических процессов, он также необходим для синтеза ДНК, РНК, коллагена, антител и т. д. [52].Биологическая роль железа в организме человека выходит за рамки этой статьи, и были перечислены лишь некоторые важные из них. 3.3.2. Роль в здоровье и заболеваниях полости ртаРоль железа в здоровье и заболеваниях полости рта резюмируется следующим образом: (1) Железодефицитная анемия является наиболее распространенным проявлением низкого уровня этого важного микроэлемента в сыворотке крови. Микроцитарные гипохромные эритроциты, утомляемость, ахлоргидрия, атрофия эпителия, потеря внимания, раздражительность, одышка и снижение памяти — вот некоторые из признаков железодефицитной анемии [25].Оральные проявления железодефицитной анемии можно резюмировать как ангулярный хейлит, атрофический глоссит, генерализованную атрофию слизистой оболочки полости рта, кандидозные инфекции, бледность и стоматит. Синдром Пламмера-Винсона или синдром Патерсона-Келли или сидеропеническая дисфагия — это редкое состояние, характеризующееся железодефицитной анемией, дисфагией и койлонихией, при этом женщины страдают чаще, чем мужчины. Дисфагия возникает в результате наличия аномальных перепонок пищевода, которые имеют предрасположенность к злокачественной трансформации [53].(2) Предраковые поражения и состояния полости рта: у пациентов с OSMF было обнаружено значительное снижение концентрации железа в сыворотке крови с повышенной общей железосвязывающей способностью. Снижение уровня железа у пациентов с OSMF может быть связано с использованием железа в синтезе коллагена. Кроме того, дефицит железа в тканях полости рта приводит к снижению васкуляризации, что еще больше способствует просачиванию ареколина (побочный продукт ореха арека). Дальнейшее повреждение вызывается усиленной перколяцией ареколина, которая усиливает пролиферацию фибробластов и образование коллагена [25].Хотя большая часть литературы предполагает, что OSMF приводит к дефициту железа из-за нарушения пищевых привычек, Bhattacharya et al. сообщили об интересном случае, когда железодефицитная анемия в первую очередь привела к развитию подслизистого фиброза полости рта, который был успешно вылечен пероральным введением добавок железа и антиоксидантов [54]. Аналогичным образом низкие уровни железа в сыворотке были оценены у пациентов, страдающих оральной лейкоплакией. (3) Также было отмечено, что уровни ферритина в сыворотке повышаются, а концентрации железа в сыворотке снижаются по мере прогрессирования опухоли при карциномах головы и шеи, и, таким образом, гем может быть используется в качестве инструмента наблюдения за пациентами наряду с оценкой питания [47]. 3.4. КобальтПрисутствие кобальта в тканях животных было впервые установлено Бертраном и Машебёфом в 1925 г., что впоследствии было подтверждено различными исследованиями спектрографическими методами [55, 56]. Кобальт является важным микроэлементом для человеческого организма и может встречаться в органических и неорганических формах. В органической форме он составляет неотъемлемую часть витамина B12 и играет существенную роль в образовании аминокислот и нейротрансмиттеров. Неорганические формы кобальта токсичны для человеческого организма, и чем дольше они остаются в организме, тем больше вредного воздействия они вызывают в клетках.Ионы кобальта всасываются в организм человека несколькими путями: во-первых, с пищей; во-вторых, дыхательной системой; в-третьих, кожей; и, наконец, как компонент биоматериалов. Ионы кобальта попадают в организм любым из вышеупомянутых путей, связываются с белками в кровотоке и транспортируются с кровью для отложения в тканях и клетках. Общее содержание кобальта в организме оценивается между 80 и 300 мкг витамина B12 [57–59]. 3.4.1. Биологические функцииВитамин B12, также известный как кобаламин, является водорастворимым витамином и содержит биохимически редкий элемент кобальт в центре плоского кольца тетрапирролкоррина. Витамин B12 вырабатывается в виде гидроксокобаламина внутри бактерий, и в организме происходит превращение в метилкобаламин и 5′-дезоксиаденозилкобаламин, ферментативно активные формы кофактора. Цианокобаламин, четвертый витамер витамина B12, может метаболизироваться в организме в активную форму кофермента и использоваться в пищевых добавках.Эритропоэтин, необходимый для образования эритроцитов, стимуляция осуществляется витамином В12, содержащим соли кобальта, и, таким образом, дефицит кобальта тесно связан с нарушением синтеза витамина В12, что приводит к анемии и гипофункции щитовидной железы с повышенным риском аномалий развития и недостаточности у детей раннего возраста. [59]. Помимо того, что он является важным компонентом этих различных форм витамина B12, присутствие кобальта необходимо для эффективного образования аминокислот и различных белков для образования миелиновой оболочки.Кобальт также играет решающую роль в выработке нейротрансмиттеров, необходимых для правильной работы организма. С другой стороны, избыток ионов кобальта в организме может усиливать действие щитовидной железы и костного мозга, что приводит к перепроизводству эритроцитов, фиброзу легких и астме [60]. 3.4.2. Роль в гигиене полости ртаРоль кобальта в гигиене полости рта резюмируется следующим образом: (1) Кобальт, часть витамина B12, также называемый внешним фактором, необходим для образования эритроцитов.Таким образом, наиболее известным проявлением дефицита кобальта в полости рта является пернициозная анемия, которая характеризуется глосситом, ощущением жжения, мясистым красным языком в виде пятен или полностью красным языком, который также называют глосситом Хантера или Меллера. , и редко неглубокие язвы [61]. (2) Помимо эритропоэза, витамин B12 также играет важную роль в восстановлении и регенерации нервов. Следовательно, дефицит кобальта может иметь побочные эффекты, такие как периферическая невропатия.(3) Красный плоский лишай и лихеноидные реакции полости рта связаны с воздействием на них хрома, кобальта, никеля и сплавов амальгамы, которые высвобождаются из металлических сплавов, обычно используемых в стоматологии, в ротовой полости. Эти микроэлементы при высвобождении из металлических сплавов вступают в непосредственный контакт со слизистой оболочкой полости рта, что приводит к иммуноопосредованному повреждению базальных эпителиальных кератиноцитов и впоследствии вызывает реакции чувствительности в форме OLR. Некоторые исследования связывают OLR с риском злокачественной трансформации [62]. 3.5. ХромСлово «хром» в переводе с греческого означает «цвет». Хром существует в двухвалентной [Cr(II)], трехвалентной [Cr(III)] и шестивалентной [Cr(VI)] степенях окисления, причем Cr(VI) и Cr(III) являются наиболее стабильными формами, среди которых Cr( III) и Cr(VI) – нерастворимая и растворимая формы соответственно. Общее содержание хрома в организме относительно низкое и составляет около 0,006 г у среднего здорового взрослого человека. Трехвалентный Cr является важным микроэлементом и играет важную роль в метаболизме глюкозы, выступая в качестве кофактора действия инсулина.Шестивалентный хром является токсичным промышленным загрязнителем и классифицируется как канцероген, обладающий мутагенными и тератогенными свойствами. Воздействие хрома через профессию при вдыхании было связано с различными видами рака легких, желудочно-кишечного тракта и центральной нервной системы. Хром выводится в основном с мочой и фекалиями и в небольших количествах с волосами, потом и желчью [63]. 3.5.1. Biological FunctionsХром является важным микроэлементом для людей с избыточным весом, поскольку он является одним из ключевых минералов, регулирующих уровень сахара и липидов в крови.Хром [Cr(III)] повышает эффективность инсулина и стимулирует поглощение глюкозы из мышц и других тканей, являясь основным компонентом фактора толерантности к глюкозе (GFT). При низком уровне хрома в сыворотке уровень циркулирующего (GFT) также ниже, и, следовательно, инсулин менее эффективен в снижении уровня сахара в крови. В результате высокий уровень сахара в крови стимулирует дальнейший выброс неэффективного инсулина [64, 65]. Считается, что хром подавляет p53, белок-супрессор опухолей, инактивация которого в результате мутаций связана со многими типами рака человека.Хромовые язвы, коррозионные реакции на носовой перегородке, острый дерматит раздражения и аллергический экзематозный дерматит были зарегистрированы среди лиц, подвергшихся воздействию соединений шестивалентного хрома. Документально подтверждено, что промышленные рабочие, подвергшиеся воздействию хроматов, подвергаются чрезмерному риску рака легких. Поскольку хром присутствует в организме в очень малых количествах, трудно определить состояние дефицита. Считается, что если концентрация хрома ниже нормального значения 0.14–0,15 нг/мл в сыворотке, это будет свидетельствовать о наличии тяжелого дефицита хрома. Несмотря на это, повышенные уровни в плазме могут сосуществовать с отрицательным тканевым балансом. Гипергликемия может сочетаться с повышенным содержанием хрома в плазме и повышенной экскрецией с мочой. Концентрация хрома в моче, волосах и жидкостях организма не может отражать истинный статус хрома в организме [65]. 3.5.2. Role in Oral Health and DiseasesРоль хрома в OLR обсуждалась ранее [62].Гипергликемический статус больных сахарным диабетом при невыявленном дефиците хрома может привести к широкому спектру проявлений в полости рта, отмечаемых у диабетиков, таких как замедленное заживление ран, гнойный пародонтит, различные грибковые инфекции полости рта, преждевременные заболевания пародонта и гипосаливация [66]. 3.6. СеленСелен является жизненно важным микроэлементом, который является важным компонентом антиоксидантных ферментов, таких как пероксиды глутатиона и тиоредоксинредуктаза [67]. Соли селена, необходимые для различных клеточных функций в организме человека, токсичны в избыточных количествах.Сообщается, что микроорганизмы имеют несколько селенсодержащих ферментов, и наиболее вероятно, что селенопротеины, отличные от глутатионпероксидазы, еще предстоит обнаружить у высших животных. Исторически эндемичная для детей в возрасте 2–10 лет и женщин детородного возраста болезнь Кешан имела географическое распространение вдоль широкой лентовидной области материкового Китая, с северо-востока на юго-запад. Типичными проявлениями были утомляемость даже после легкой физической нагрузки, сердечная аритмия и учащенное сердцебиение, потеря аппетита, сердечная недостаточность, кардиомегалия и застойная сердечная недостаточность.Заболевание было распространено среди людей, получавших диету с дефицитом селена, и состояние пациентов быстро улучшалось после обогащения. Точно так же чувствительные к селену заболевания костей и суставов, болезнь Кашина-Бека, также были обнаружены у детей в возрасте 5–13 лет в Китае и в меньшей степени в юго-восточной Сибири. Болезнь Кашина-Бека также встречается в районах с низким содержанием селена в обрабатываемой почве. 3.6.1. Биологические функцииИзвестно, что селен обладает иммуномодулирующими и антипролиферативными свойствами и может влиять на иммунный ответ, изменяя экспрессию цитокинов и их рецепторов или делая иммунные клетки более устойчивыми к окислительному стрессу [68, 69].В составе фермента глутатионпероксидазы, наряду с витамином Е, каталазой и супероксиддисмутазой, селен является компонентом одной из императивных систем антиоксидантной защиты организма. Имеются также убедительные доказательства того, что неизвестный селеноферментный белок играет некоторую роль в синтезе трийодтиронинового гормона из тироксина [70, 71]. 3.6.2. Роль в здоровье и заболеваниях полости ртаУровни селена в сыворотке показали прогрессивное снижение от здоровых субъектов до пациентов с предраковыми поражениями, такими как лейкоплакия полости рта, и дальнейшее снижение у пациентов, страдающих раком полости рта.Также наблюдалось снижение уровня селенсодержащей глутатионпероксидазы и одновременное увеличение окислительного стресса в том же порядке [72]. Таким образом, совершенно очевидно, что снижение концентрации селена приведет к усилению окислительного стресса в тканях организма с непреднамеренными вредными последствиями. Таким образом, пищевые добавки с микроэлементами, такими как селен, являются важным обоснованием при лечении предраковых поражений, таких как лейкоплакия, состояний, таких как OSMF, и у пациентов с раком полости рта для снижения окислительного стресса внутри организма [54]. В недавнем исследовании оценивали противовоспалительный и антиоксидантный эффект селена при его введении пациентам, страдающим оральным мукозитом, вторичным по отношению к химиотерапии высокими дозами. Исследователи утверждали, что адекватное добавление селена может оказывать цитопротекторное действие и противоязвенную активность, и пришли к выводу, что селен может эффективно уменьшать продолжительность и тяжесть орального мукозита у этих пациентов [73]. 3.7. МолибденМинералы молибдена были известны на протяжении всей истории, но этот элемент был открыт Карлом Вильгельмом Шееле в 1778 году и впервые выделен в 1781 году Петером Якобом Хьельмом. 3.7.1. Биологические функцииМолибден, как компонент молибдопротеина, принимает участие в формировании активных центров различных ферментов. Тремя основными молибденсодержащими ферментами являются ксантиндегидрогеназа/оксидаза, альдегидоксидаза и сульфитоксидаза. Молибденсодержащий фермент играет определенную роль в катаболизме пуринов. Он также влияет на синтез белка и рост организма [74]. Молибден оказывает антагонистическое действие на медь; таким образом, высокие концентрации молибдена могут снижать абсорбцию меди и впоследствии приводить к дефициту меди [75]. 3.7.2. Роль в здоровье и заболеваниях полости ртаСчитается, что бор, ванадий и молибден обладают кариостатическим эффектом. Различные исследования из Венгрии и Новой Зеландии убедительно показали, что взаимодействие молибдена с фторидом имеет сильный кариостатический эффект. Однако кариостатический эффект молибдена подвергся критическому обзору в литературе с неубедительными результатами. Тем не менее, зубная эмаль накапливает значительное количество молибдена. Необходимы дальнейшие исследования или расследования для получения надежных наблюдений [76]. 3.8. ФторФтор составляет незначительную часть массы тела и поступает в организм в основном с питьевой водой и в меньшей степени с пищей. 3.8.1. Биологические функцииФтор в форме кристаллов фторапатита является важной частью организованного матрикса твердых тканей, таких как кости и зубы. Также считается, что фтор в сочетании с кальцием стимулирует активность остеобластов [64]. 3.8.2. Роль в здоровье полости рта и заболеванияхНизкий уровень фтора в питьевой воде связан с кариесом.Чрезмерная концентрация фтора на стадии кальцификации зубов может привести к своего рода гипоплазии эмали, называемой флюорозом зубов. Клинически флюороз зубов может варьироваться от небольших белых помутнений на эмали до сильной крапчатости тканей зуба с нарастающей степенью выраженности. Общий эффект чрезмерного потребления фтора на структуру зубов зависит от многих факторов, таких как концентрация фтора в питьевой воде, стадия кальцификации зубов при воздействии, продолжительность воздействия и степень воздействия [61]. 3.9. ЙодЙод является жизненно важным микроэлементом, необходимым на всех этапах жизни, особенно в период формирования. Важно поддерживать повседневные функции человеческого организма, а дефицит или избыток может иметь серьезные неблагоприятные последствия для организма. 3.9.1. Биологические функцииЙод является важным компонентом гормонов щитовидной железы, то есть тетрайодтиронина (Т4 или тироксина) и трийодтиронина (Т3). Он играет значительную роль в функционировании паращитовидных желез.Йод играет важную роль в общем росте и развитии организма наряду с поддержанием метаболических процессов [64]. 3.9.2. Роль в здоровье полости рта и заболеванияхМогут быть бесчисленные симптомы дефицита или избытка йода. Чаще проявляется дефицит йода. Наиболее часто сообщаемыми симптомами дефицита йода являются сильная усталость, раздражительность, психические расстройства, увеличение веса, отечность лица, запор и вялость. У нелеченных младенцев существует риск развития кретинизма и в конечном итоге они страдают от плохого роста и умственной отсталости [64]. Также было высказано предположение, что недостаток или избыток йода в пище играет важную роль в физиологии слизистой оболочки полости рта и слюнных желез. Слюнные железы могут защищать собственные клетки от перекисного окисления за счет способности концентрировать йод через симпортер йодистого натрия и активность пероксидазы. Йодид, по-видимому, выполняет примитивную антиоксидантную функцию в организмах, концентрирующих йод. Значительная роль йода в механизме иммунной защиты полости рта может быть подтверждена высокой концентрацией йода в тимусе.S. Venturi и M. Venturi также предположили, что эти действия йодидов могут быть важны для профилактики различных заболеваний полости рта и слюнных желез [77]. Исследование, проведенное Литтлтоном и Фролихом в 1993 году, также показало, что скелетные останки из зон мира, богатых йодом, демонстрировали большую истираемость, меньшую степень кариеса и меньшую преждевременную потерю зубов. Ранняя потеря зубов может быть основным фактором недостаточного питания, потери здоровья и снижения качества жизни [78]. Дефицит йода не является чем-то необычным в различных частях мира. Во всем мире было предпринято обогащение пищевой соли, чтобы компенсировать дефицит йода. Гипотиреоз характеризуется снижением уровня гормонов щитовидной железы. Что касается поражения ротовой полости, может наблюдаться явное утолщение губ из-за отложения гликозаминогликанов в подкожных тканях. Точно так же по той же причине можно увидеть макроглоссию языка. У детей может наблюдаться задержка прорезывания зубов без какого-либо влияния на формирование зубов [53]. Гипертиреоз у взрослых может привести к диффузной коричневой пигментации десен, слизистой оболочки щек, неба и языка, сходной с болезнью Аддисона. Механизм, с помощью которого происходит стимуляция синтеза меланина, еще неясен, но пигментация, как правило, исчезает при лечении аномалий щитовидной железы [79]. 4. Обнаружение микроэлементов и оценка состояния питанияЭто было сделано следующим образом: (1) Хотя для определения присутствия микроэлементов использовались различные методы, это трудоемкая и бесплодная работа из-за их широкого распространения. в живых тканях и ферментных системах.Колориметрические и спектрографические методы обычно используются для анализа количества микроэлементов. Как правило, спектроскопия и электрохимические методы предпочтительны для анализа отдельных элементов, тогда как нейтронно-активационный анализ и спектроскопические методы используются для определения более чем одного элемента [11]. тесты [80]. Мазок костного мозга, не содержащий окрашиваемого железа, является окончательным. Повышенная общая железосвязывающая способность, низкий уровень железа в сыворотке и низкая концентрация ферритина в сыворотке считаются диагностическими признаками дефицита железа.Недавно новые подходы, такие как анализ порфирина цинка в эритроцитах, также использовались в первичных скрининговых тестах для оценки статуса железа [81]. (3) Сообщалось, что оптимальное соотношение меди и цинка в плазме или сыворотке составляет 0,70–1,00. Как упоминалось ранее в статье, диагностика дефицита цинка является постоянной проблемой. Уровни цинка в плазме или сыворотке являются наиболее часто используемыми показателями для оценки дефицита цинка. Серьезный дефицит Cu может быть обнаружен путем тестирования на низкий уровень меди в плазме или сыворотке, низкий уровень церулоплазмина и низкий уровень супероксиддисмутазы, но эти тесты не очень чувствительны и не могут определить предельный дефицит меди [16, 82].(4) Оценка йодного статуса питания населения или группы, проживающей в районе или регионе, который предположительно является йоддефицитным, может быть выполнена путем оценки частоты зоба, измерения экскреции йода с мочой и определения уровня йододефицита. Т3, Т4 или ТТГ в крови. (5) Запасы хрома в тканях, по-видимому, не совсем отражают содержание хрома в крови; таким образом, концентрация хрома в сыворотке не является хорошим индикатором состояния хрома. Было высказано предположение, что уровень хрома в сыворотке ниже 0.14–0,15 нг/мл указывают на наличие тяжелого дефицита хрома. Чрезмерное воздействие хрома на человека в результате занятий или несчастного случая может отражаться повышенным содержанием хрома в сыворотке. (6) Различные ткани, такие как кровь, волосы и ногти, были проанализированы для определения пищевого статуса селена. Как правило, эти ткани могут дать надежную оценку статуса селена, если потребление селена с пищей относительно однородно. (7) Состояние уровней других микроэлементов в тканях у нормальных людей трудно определить. 5. ЗаключениеДиагностика дефицита микроэлементов как в питании, так и в клинических условиях является одной из самых сложных задач. Недостаточное потребление незаменимого микроэлемента может снизить важные биологические функции в тканях, а восстановление физиологических уровней этого элемента облегчит нарушенную функцию или предотвратит ухудшение. Организм человека имеет сложную систему управления и регулирования количества основных микроэлементов, циркулирующих в крови и хранящихся в клетках.Аномальные уровни этих микроэлементов могут развиться, когда организм не функционирует должным образом или в диетических источниках содержится неправильный уровень. Существуют убедительные доказательства того, что диета, богатая антиоксидантами и необходимыми минералами, необходима для здорового духа и тела. Профилактическая медицина в последние годы привлекла к себе больше внимания, чем что-либо еще, как метко сказано: «Профилактика лучше, чем лечение». Выборочное воспроизведение связи профилактической медицины с различными микроэлементами представлено в табл. 2 [5].Здоровье полости рта и общее состояние здоровья нельзя рассматривать независимо друг от друга, и на самом деле полость рта может эффективно отражать системное здоровье. Комбинация различных питательных микроэлементов и микроэлементов использовалась в качестве стратегии лечения заболеваний полости рта, таких как лейкоплакия полости рта, подслизистый фиброз полости рта, рак полости рта и т. д., поскольку их совокупный результат более благоприятен по сравнению с изолированным применением. Следовательно, знание клинических аспектов микроэлементов становится обязательным как для врачей общего профиля, так и для врачей-стоматологов.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||


 В природе встречается в виде мягкого металла. Легко рассыпается и растворяется в воде, не образуя при этом видимого невооруженным глазом осадка.
В природе встречается в виде мягкого металла. Легко рассыпается и растворяется в воде, не образуя при этом видимого невооруженным глазом осадка. Именно в воде попадает в клетки организмов и помогает поддерживать в них баланс.
Именно в воде попадает в клетки организмов и помогает поддерживать в них баланс.
 Легко вступает в реакции и образует соли под названием хлориды. Именно в таком виде поступает с пищей в желудок человека.
Легко вступает в реакции и образует соли под названием хлориды. Именно в таком виде поступает с пищей в желудок человека. Если не хватает в организме фтора, человек сталкивается с элементарным развитием кариеса зубов.
Если не хватает в организме фтора, человек сталкивается с элементарным развитием кариеса зубов. В результате этот элемент препятствует развитию аллергии, воспалению и прочим патологическим процессам;
В результате этот элемент препятствует развитию аллергии, воспалению и прочим патологическим процессам;
 По подсчетам ученых, в человеческом организме кислород является одним из наиболее потребляемых и расходуемых веществ.
По подсчетам ученых, в человеческом организме кислород является одним из наиболее потребляемых и расходуемых веществ. Вещество защищает от разрушения красные кровяные тельца – основной «транспорт» для кислорода.
Вещество защищает от разрушения красные кровяные тельца – основной «транспорт» для кислорода.

 Все образуют одноатомные ионы (Na + , Mg 2+ , K + , Ca 2+ , Cl — ), за исключением фосфора, который находится в виде иона фосфата (PO 4 9 − ). Напомним, что соли кальция используются многими организмами в качестве структурных материалов, например, в костях [гидроксиапатит, Ca 5 (PO 4 ) 3 OH]; соли кальция есть также в морских раковинах и яичной скорлупе (CaCO 3 ), а в растениях они служат хранилищем для Ca 2+ (оксалат кальция).
Все образуют одноатомные ионы (Na + , Mg 2+ , K + , Ca 2+ , Cl — ), за исключением фосфора, который находится в виде иона фосфата (PO 4 9 − ). Напомним, что соли кальция используются многими организмами в качестве структурных материалов, например, в костях [гидроксиапатит, Ca 5 (PO 4 ) 3 OH]; соли кальция есть также в морских раковинах и яичной скорлупе (CaCO 3 ), а в растениях они служат хранилищем для Ca 2+ (оксалат кальция). Селективность этих ионных насосов основана на различиях в ионном радиусе (раздел 7.2) и ионный заряд.
Селективность этих ионных насосов основана на различиях в ионном радиусе (раздел 7.2) и ионный заряд.